病史简介
患者:女,20岁,左枕叶脑出血2月半余,发现左枕叶占位7天。
患者2个半月前出现头痛呕吐,伴右侧视野视物不清,当地医院经CT检查考虑左侧枕叶脑出血,予以对症治疗。7天前复查头部CT并做增强显示:左侧枕叶占位性病变(图1)。
查体:右侧视野缺损。视野检查见右侧视野同向性偏盲(图2)。
术前影像
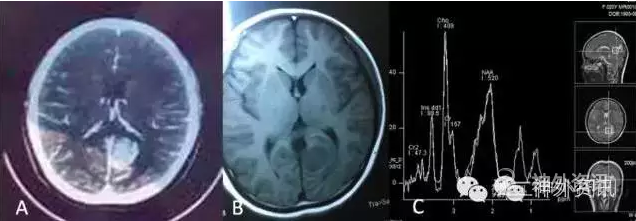
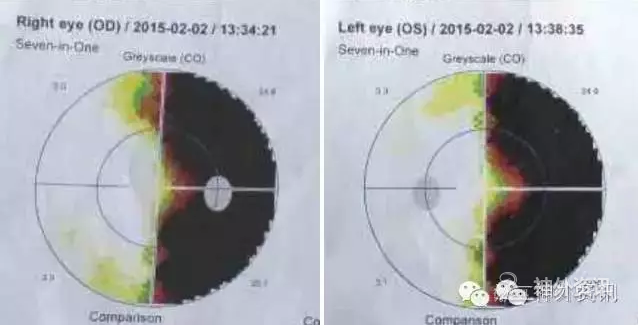
图1. 术前影像资料 A:当地医院头部增强CT显示左枕叶占位性病变,伴明显强化,B:当地医院头部磁共振平扫显示肿物同周围组织分界不清,C:我院头部磁共振波谱显示肿瘤内部Cho峰升高,NAA峰降低,考虑胶质瘤可能性大。
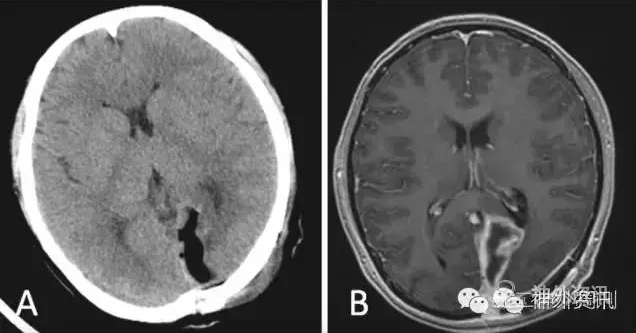
图2. 术前视野检查显示双眼右侧视野同向性偏盲。
诊疗经过
手术
等待增强磁共振检查期间,患者头痛、呕吐等颅高压症状明显。于2014-09-02日全麻下行左枕叶病变切除术,术中冰冻提示(左枕叶)恶性肿瘤,考虑高级别胶质瘤。
术后过程
术后患者颅高压症状缓解,术后CT显示肿瘤全切,术后20日CT显示瘤腔周边线样强化,考虑瘤腔周边炎症反应(术后2.3个月后强化消失)(图3)。术后病理提示(左枕叶)胶质母细胞瘤,WHO IV级。分子检测提示MGMT启动子甲基化,1p19q无共缺失。
图3. 术后影像学表现。A:术后第2日头部CT,B:术后第20日,放疗前头部磁共振增强。
辅助治疗
术后于2014.9.29和2014.10.27分别行左枕叶原瘤区6MV-X线PTV1 D95/4600cGy/23F、PTV2 D95/1400cGy/7F辅助放疗。放疗期间另予替莫唑胺120mg(75mg/m2) 每晚1次口服同步化疗(因经济条件较差,患者拒绝进一步辅助化疗)。
后续治疗
患者放疗后2.3个月、5.1个月、8.6个月头部磁共振显示病灶稳定(图4)。术后11个月后,患者感后颈,腰背针刺样疼痛,向右下肢放射,行走或坐位时较明显,休息后可缓解。头部磁共振显示左侧侧脑室三角区的脑室壁线样强化(图4),脊髓磁共振显示脊髓表面多发线样、结节样强化,考虑脑脊液播散转移性肿瘤(图5)。
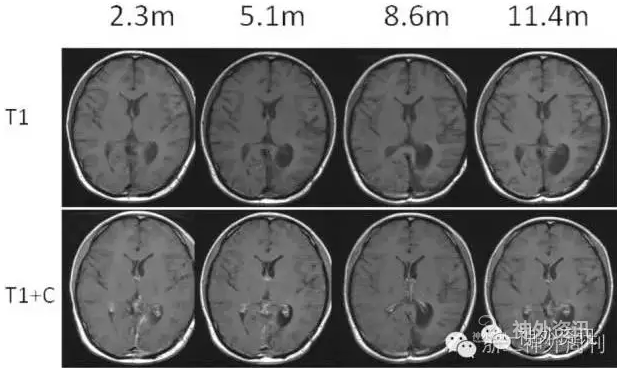
图4. 患者手术后序贯磁共振增强扫描。术后第11个月,患者出现颈部及腰背部疼痛时,侧脑室三角区脑室壁轻度线样强化。
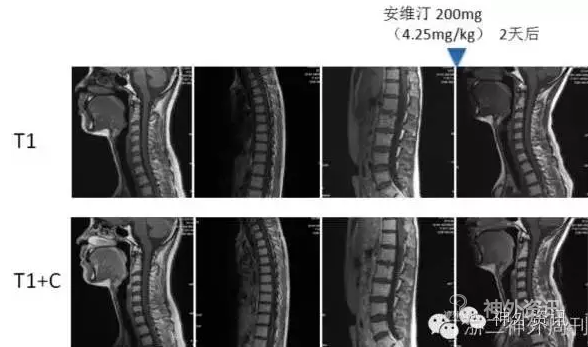
图5. 术后11.4个月,患者出现颈部及腰背部疼痛时,脊髓表面多发线样、结节样强化,考虑脑脊液播散转移性肿瘤
建议患者行替莫唑胺治疗,患者拒绝,给予贝伐单抗200mg(4.25mg/kg)一次,静滴后患者自觉症状明显缓解,2日后复查脊髓磁共振,显示脊髓表面强化范围减小(图6)。
出院后患者失访。
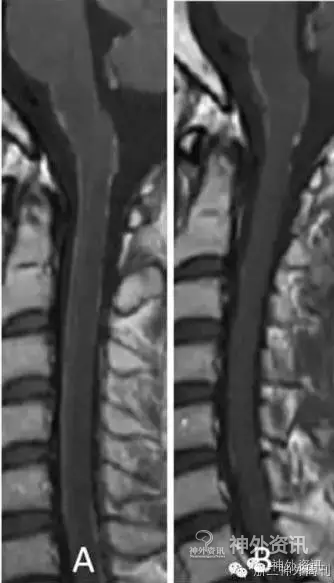
图6. 应用贝伐单抗前后,脊髓增强磁共振对比,应用贝伐单抗后2天,脊髓表面增强病灶范围减小。
讨论
本病例是一例伴有广泛脑脊液播散的胶质母细胞瘤病例。脑脊液播散的肿瘤的早期诊断和治疗都是具有挑战性的。
哪些肿瘤容易发生脑脊液播散?
最容易发生脑脊液播散的原发脑肿瘤有:
髓母细胞瘤
原始神经外胚层肿瘤(PNET,WHO 2016版分类称为:伴有多层菊型团的胚胎性肿瘤)
室管膜瘤
生殖细胞瘤
脉络丛癌
胶质母细胞瘤
间变性星形细胞瘤
最容易发生脑脊液播散的转移性肿瘤包括:
乳腺癌
肺癌
黑色素瘤
淋巴瘤
白血病
自:Radiopaedia:https://radiopaedia.org/articles/leptomeningeal-metastases。
本期病例讨论主要讨论伴有脑脊液播散的胶质母细胞瘤的诊断方法和治疗原则。
胶质母细胞瘤发生脑脊液播散的危险因素
胶质母细胞瘤发生脑脊液播散的几率约是14%[1]。通常认为,胶质母细胞瘤发生脑脊液播散的主要危险因素是肿瘤距离软脑膜较近以及术中脑室系统开放。但是也有学者通过单中心数据说明:术中脑室开放和(或)肿瘤接近脑室系统对脑脊液播散的发生以及术后生存率均没有显著影响[2]。
是否容易发生脑脊液播散主要取决于肿瘤的细胞成分[3],并且年轻的胶母患者容易发生脑脊液播散[1]。既往文献及浙医二院的病例显示,原发于脊髓的胶质母细胞瘤几乎都发生脑脊液播散(浙二神外周刊第44期)。
目前用于分型和判断预后的常用分子标记物,如IDH突变、MGMT甲基化、1p19q共缺失等分子标记物并不能预测脑脊液播散的几率。但有报道,GFAP表达率比较低的胶质瘤更容易发生脑脊液播散[4]。具有脑脊液播散和侵袭性的肿瘤的增殖指数反而较低[5]。
判断胶质母细胞瘤脑脊液播散的方法
目前尚无针对胶质母细胞瘤脑脊液播散的专门指南可供参考。在高度怀疑有脑脊液播散的可能时,诊疗流程参考《NCCN中枢神经系统肿瘤》2015版[6],柔脑膜转移性肿瘤(LEPT)章节。其判断的方法主要有影像学和病理学两类。一般而言,影像学方法方法相对简单、无创,但特异性较低,病理学方法往往需要侵入性操作,特异性很高,但是敏感性往往不够。
目前研究比较多的“液体活检”技术,主要是利用体液里或者体液中的外分泌体的游离DNA判断肿瘤的发生或者复发,是一种判断脑脊液播散的潜在方法,不仅可以判断肿瘤的存在与否,还可以根据肿瘤标记分子判断肿瘤的性质以及同原发肿瘤的区别,但目前尚未广泛用于临床[7]。浙医二院已拟立项的浙江省自然科学基金项目旨在探讨此技术的临床应用。
脑脊液播散的治疗
伴有脑脊液播散的高级别胶质瘤,从脑脊液播散的时间为起点,中位生存期为10.2个月。医学干预会明显增加其生存时间(11.7 vs. 3.3个月)。因此,对于脑脊液播散,合理的医学干预是十分必要的。建议的干预方案包括:全脑放疗30Gy,全脊髓放疗40-50Gy,替莫唑胺口服,静脉应用贝伐单抗,鞘内化疗(推荐阿糖胞苷或甲氨蝶呤或thiotriethylenephosphoramide)[8, 9]。
值得注意的是:由于伴有脑脊液播散的胶质母细胞瘤通常做过放射治疗,发生脑脊液播散时候,医生和患者往往选择单独化疗,但单中心的数据显示,单独化疗是没有生存获益的,因此针对转移部位的再程放疗是应该首先考虑的。
鞘内治疗通常需要埋植Omaya储液囊以便给药,通过皮下输液港连进行鞘内持续给药也是一种选择[10]。
参考文献
[1] Arita N, Taneda M, Hayakawa T. Leptomeningeal dissemination of malignant gliomas. Incidence, diagnosis and outcome.[J]. Acta Neurochirurgica, 1994, 126(126):84-92.
[2] 韩武, 郝淑煜, 谢坚,等. 成人恶性胶质瘤术中脑室开放和肿瘤接近脑室系统与肿瘤脑脊液播散的相关性研究[J]. 中国微侵袭神经外科杂志, 2016(7).
[3] 孙崇然.神经系统肿瘤精准医疗专家论坛会议报道[C].上海:[神外资讯],2016.
[4] Onda K, Tanaka R, Takahashi H, et al. Cerebral glioblastoma with cerebrospinal fluid dissemination: a clinicopathological study of 14 cases examined by complete autopsy.[J]. Neurosurgery, 1989, 25(4):533-40.
[5] Giese A, Bjerkvig R, Berens M E, et al. Cost of migration: invasion of malignant gliomas and implications for treatment.[J]. Journal of Clinical Oncology Official Journal of the American Society of Clinical Oncology, 2003, 21(8):1624-36.
[6] Nabors L B, Portnow J, Ammirati M, et al. Central Nervous System Cancers, Version 1.2015 Featured Updates to the NCCN Guidelines[J]. Journal of the National Comprehensive Cancer Network Jnccn, 2015, 13(10):1191-1202.
[7] Santiagodieppa D R, Steinberg J, Gonda D, et al. Extracellular vesicles as a platform for 'liquid biopsy' in glioblastoma patients.[J]. Expert Review of Molecular Diagnostics, 2014, 14(7):819-825.
[8] Dardis C, Milton K, Ashby L S, et al. Leptomeningeal Metastases in High-Grade Adult Glioma: Development, Diagnosis, Management, and Outcomes in a Series of 34 Patients[J]. Frontiers in Neurology, 2014.
[9] Witham T F, Fukui M B, Meltzer C C, et al. Survival of patients with high grade glioma treated with intrathecal thiotriethylenephosphoramide for ependymal or leptomeningeal gliomatosis[J]. Cancer, 1999, 86(7):1347–1353.
[10] Shinoura N, Tabei Y, Yamada R, et al. Continuous intrathecal treatment with methotrexate via subcutaneous port: implication for leptomeningeal dissemination of malignant tumors.[J]. Journal of neuro-oncology, 2008, 87(3):309-316.
(本文由浙二神外周刊原创,浙江大学医学院附属第二医院神经外科孙崇然副主任医师总结,石键副主任医师审校,张建民主任终审。)
往期回顾
浙二神外周刊(三十七)--垂体瘤伴发鞍结...
浙二神外周刊(三十六)--脑膜血管瘤病...
更多资讯请关注神外资讯微信公众号:neurosurgerynews



