今天为大家分享的是来自广州医科大学附属第二医院何伟文教授团队翻译、点评的《脑缺血后早期再灌注:除挽救神经元之外的更多疗效 》,欢迎阅读。
【Ref: Tachibana M, et al. Stroke. 2017 Aug. doi:10.1161/STROKEAHA.117.016689.】
摘要
背景与目的:最近研究显示,卒中发病后6~12小时成功血管内取栓可改善患者3个月后的功能预后。在本研究中,我们采用小鼠卒中模型,研究缺血性卒中后再灌注在缺血区域修复过程及功能恢复中的作用。
方法:使用具有较差的侧枝血流的小鼠品种CB-17(CB-17/lcr-+/+Jcl)作为研究对象, 观察不同持续时间大脑中动脉闭塞后(包括永久性大脑中动脉闭塞),时间依赖性的组织学改变及功能恢复。
结果:实验动物接受超过60 min缺血后再灌注,在1d后产生较大的神经元坏死区域, 该区域的微管相关蛋白2(microtubuleassociated protein 2,MAP2)呈现阴性表达; 而在45 min内接受缺血再灌注的实验动物中,神经元坏死区域局限。给予早期再灌注的小鼠,7d后MAP2阴性表达的神经元坏死区域明显缩小,并与更好的功能恢复相关。1d后的Klüver-Barrera(KB)染色显示小鼠脑白质损伤在再灌注的动物中明显更少。免疫组织化学检测及电子显微镜下可见:早期再灌注的小鼠在梗死区域中有更大量的内皮细胞存在,更快的血小板衍生生长因子受体β(platelet- derived growth factorreceptor β,PDGFRβ )阳性血管周细胞的募集和随后的梗死灶内纤维化。早期再灌注产生更大量的胶原纤维酸性蛋白(glialbrillary acidic protein,GFAP)表达阳性的星形胶质细胞在梗死周边区域聚集。梗死周边星形胶质细胞增生的情况在PDGFRβ杂合敲除小鼠中减弱。
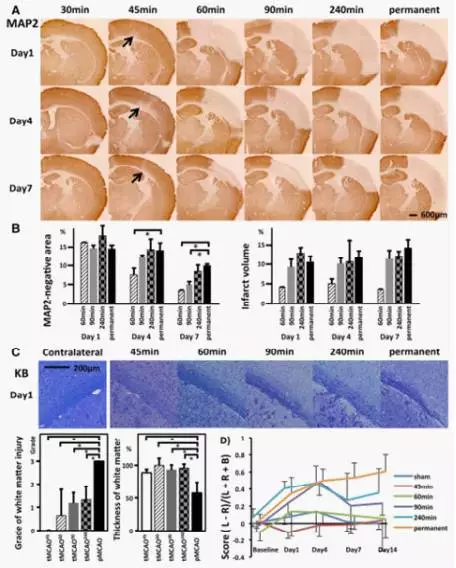
图1A. tMCAO 30、45、60、90、240 min及pMCAP后第1、4、7dMAP2染色;B.左图显示MAP2阴性表达区域,tMACO60、90、240 min及pMACO后1、4、7d。右图显示,tMCAO 60、90、240min以及pMCAO后第1、4、7d的梗死容积; C.通过KB染色显示,tMCAO(45、60、90、240 min)及pMCAO后1d;左侧为对侧的对照; D.运动功能评估假手术组、tMCAO 45、60、90、240min及pMACO后1、4、7d。
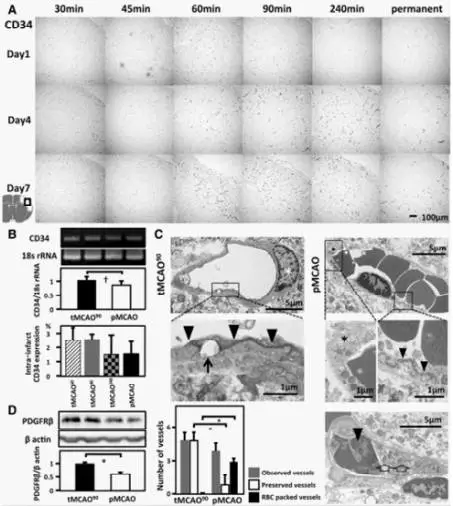
图2A. CD34 免疫染色显示tMCAO(30、45、60、90、240 min)及pMCAO后第1、4、7 d; B.上图显示,定量PCR检测CD34mRNA,缺血半球MCAO后第1d。下图显示,使用ImageJ行梗死灶内CD34表达的定量密度测定, tMCAO(60、90、240 min)及pMCAO后第4 d。C. tMCAO(90 min)及pMCAO后第1d,梗死核心中毛细血管的电子显微镜下观。D. 免疫印迹分析显示,PDGFRβ在MCAO后第1d在梗死大脑半球组织的表达。
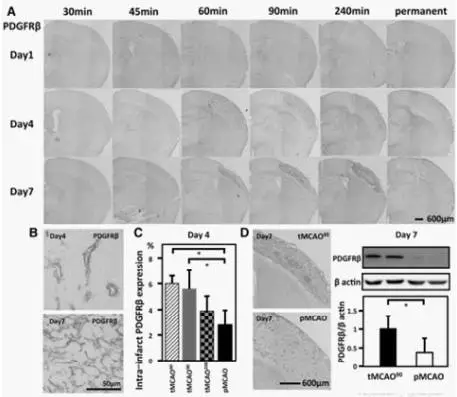
图3A,PDGFRβ免疫染色,tMCAO(30、45、60、90、240min)及pMCAO后第1、4、7 d)。B, tMCAO(90 min)后第4、7d的放大图像。C,tMCAO(60,90, 240 min)及pMCAO后第4d使用ImageJ对梗死灶内PDGFRβ 进行定量密度测量。D,左, tMCAO(90 min)和pMCAO后第7d的纤维化。右,免疫印迹分析缺血半球在MCAO后第7 d的PDGFRβ 表达。
图4 A. tMCAO(30、45、60、90、240 min)及pMCAO后第1、4、7 d的GFAP免疫染色;B. MCAO后第7 d缺血半球GFAP的免疫印迹分析;C. 90 mintMCAO和pMCAO后第7d MAP2和GFAP双标记免疫荧光;D. MCAO后第7d的巢蛋白免疫染色及免疫荧光。
结论: 即使已形成梗死,早期再灌注也可增加缺血区域内皮细胞和血管周细胞的存活, 导致有效的梗死灶内纤维化和梗死周边星形细胞增生。这些效果可能与梗死周边重构及功能恢复相关。
结果:
(1) 早期再灌注导致梗死区域快速收缩,白质损伤减少, 导致更好的功能预后。 通过MAP2染色及KB染色显示, 60 min或以上的短暂性大脑中动脉闭塞(transientMCAO, tMCAO)和永久性大脑中动脉闭塞(permanentMCAO, pMCAO)在第1d均产生显著的梗死区域,但第7d,缺血时间较短的tMCAO梗死灶收缩。KB染色显示,第1 d时的白质损伤在pMCAO明显严重于tMCAO。
(2) 早期再灌注可维持梗死区域内毛细血管结构。免疫组织化学和定量PCR显示, tMCAO较pMCAO在梗死灶内有更多的CD34+内皮细胞。电子显微镜显示,tMCAO小鼠的毛细血管结构保留, 有接近完整的紧密连接,基底膜被周细胞覆盖。而pMCAO小鼠的内皮细胞和紧密连接破坏,无周细胞覆盖。免疫印迹分析显示,周细胞标记物PDGFRβ的表达水平在tMCAO中明显高于pMCAO。
(3) 早期再灌注诱导梗死灶内纤维化。免疫组化显示,梗死灶内PDGFRβ阳性细胞的聚集tMCAO多于pMCAO。使用缺血半球匀浆进行的免疫印迹分析显示,第7d时PDGFRβ的表达在tMCAO显著高于pMCAO。
(4) 早期再灌注可诱导MAP2阴性区域内星形胶质细胞增生。在30与45分钟tMCAO的梗死范围内,出现GFAP阳性星形胶质细胞聚集,缺血60分钟或更长的tMCAO和pMCAO,只出现梗死周围星形胶质细胞增生。同样的,缺血半球匀浆的免疫印迹分析显示, tMCAO(缺血90分钟)比pMCAO表达更多的GFAP。
(5) 梗死周边星形胶质细胞增生在PDGFRβ杂交敲除鼠中减弱。pMCAO后第7d在PDGFRβ+/-鼠缺血半球的PDGFRβ表达明显降低。伊文思蓝(Evans blue)染料渗漏(与紧密连接破坏相关)于第7 d在PDGFRβ+/-小鼠更为明显。免疫组织化学显示血管周围区域GFAP阳性细胞的密度, pMCAO后第7 d, PDGFRβ +/-小鼠明显降低。 使用缺血半球匀浆行免疫印迹分析显示,PDGFRβ+/-小鼠的GFAP表达减少。 早期再灌注即使不能避免缺血区域的神经元死亡,但再灌注可以诱导血管细胞存活(梗死区域内的内皮细胞、 周细胞) 、PDGFRβ阳性细胞快速聚集、 缺血区域纤维化; 从而导致缺血区域快速缩小。 早期再灌注可诱导MAP2阴性区域内及其周边星形胶质细胞反应性增生, 帮助轴突生长及再髓鞘化, 重构神经网络, 导致功能恢复。 短暂的缺血对白质的损伤较皮质更少, 早期再灌注介导的白质伤后重构与梗死周围星形细胞反应性增生可协同促进功能恢复, 改善卒中预后。
何伟文:广州医科大学附属第二医院神经外科
缺血性卒中闭塞血管急性期再开通已是公认的标准治疗方式, 并且缺血区域越早实现血流再灌注, 将挽救越多的缺血脑组织, 从而改善患者预后。 然而, 对于缺血性卒中后早期再灌注后对于挽救神经元以外的疗效还较少被临床医生所关注。
该研究通过对啮齿类动物(小鼠) 脑缺血模型实验, 首次提出缺血后早期再灌注可促进MAP2阴性区域组织修复和功能恢复, 并对其机理进行了初步的阐述。 早期再灌注可使MAP2阴性区域缩小, 而MAP2阴性区域的缩小与运动功能恢复相关。 该实验无疑拓宽了我们对卒中急性期血管开通治疗价值的认识, 即使再灌注不能挽救缺血的神经组织, 但是早期改善神经功能仍可能通过诱导血管细胞存活(梗死区域内的内皮细胞、 周细胞) 、 PDGFRβ阳性细胞快速聚集、 纤维化及梗死周边星形胶质细胞增生等一系列病理生理变化, 最终促进神经功能恢复。 这一实验结果将为“延长时间窗”及“侧枝循环差”的血管开通治疗提供理论依据。
但是, 该实验的结果仍有待验证, 其中机制亦有待进一步阐明。 无论是“延长时间窗”还是“侧枝循环差”的卒中急性期血管再通治疗, 其主要的制约因素是“再灌注后出血转化”及“无效开通”, 前者可导致病情加重, 后者患者无法从中获益。因此对于上述情况下进行血管开通治疗一直非常谨慎。 既往我们考虑行卒中急性期血管再通时, 执着于“能否挽救缺血脑组织”; 如今这个实验提出了卒中急性期的血管再通即使“不能挽救缺血脑组织”, 仍可“促进组织修复”的新问题, 促使我们对卒中急性期血管再通治疗进行更深入思考。 在发病后6~8 h或更长的时间窗内, 如果能将再灌注后症状性或严重的出血转化控制在一定范围, 是否所有的开通都将有利于病人的长期康复呢? 这个问题仍然有待进一步研究给出答案。

何伟文
广州医科大学附属第二医院神经外科教授、 主任医师、 硕士研究生导师。 现任广东省医学会神经外科分会副主任委员、 脑血管病学组组长。 中华医学会神经外科分会神经介入学组委员、 国家卫计委脑卒中防治专家委员会出血性卒中介入专业委员会委员、 中国卒中学会神经介入分会常委, 中国老年学会心脑血管专业委员会常委, 广东省药理学会神经药理专业委员会常委, 广州市医师协会理事。 《当代介入医学电子杂志》 、 《中国神经介入资讯》 编委。长期致力于脑血管病的防治工作, 对出血和缺血性脑血管病的手术及血管内介入治疗均有较深的造诣.
(广州医科大学附属第二医院何毅华编译,伍健伟校译,何伟文教授点评,神经介入资讯主编、上海长海医院神经外科主任刘建民教授终审)




