术前讨论:按照现有《中国颈部动脉夹层诊疗指南2015》及AHA/ASA2014指南,颅外段颈动脉夹层在未出现急性大血管闭塞性卒中时首选使用抗凝或者抗血小板治疗。血管内介入治疗或手术治疗经过评估后同时也是一种可以选择的手段。经与患者充分详细沟通后,选择采取血管内治疗方式。
手术过程:术前阿司匹林100mg qd,氯吡格雷75mg qd,充分双抗7天。全麻下行右侧股动脉穿刺,置入6F长鞘,插入5F造影管行双侧颈总动脉造影及3D造影,造影提示双侧颈内动脉C1段夹层动脉瘤伴局部管腔重度狭窄。静脉全身肝素化后,将6F导引导管超选至右侧颈内动脉,路图下微导丝超选至右侧颈内动脉海绵窦段,沿微导丝导入6.0*60mm Xpert pro自膨支架,确认位置良好释放支架。即刻造影显示右侧颈内动脉病变段支架贴壁良好,血流明显改善,造影剂通畅,颅内血管未见栓塞征象(I-L)。再将导引导管超选至左侧颈内动脉,微导丝通过病变段血管远端至颈内动脉海绵窦段,先后沿微导丝导入6*40mm、8*40mm支架于病变血管,确认位置良好,释放支架,术后即刻造影显示病变段支架贴壁良好,血流明显改善,造影剂通畅(M-P)。术毕XperCT未见明显造影剂渗外渗。拔除导管,缝合器封闭右侧股动脉穿刺点。手术过程顺利,术中患者生命体征平稳。
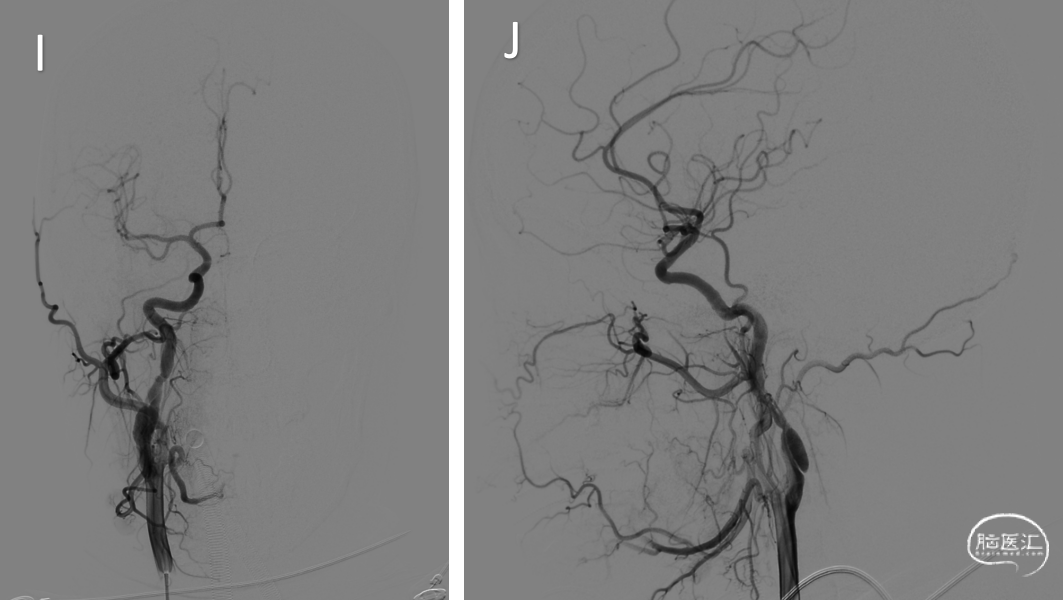
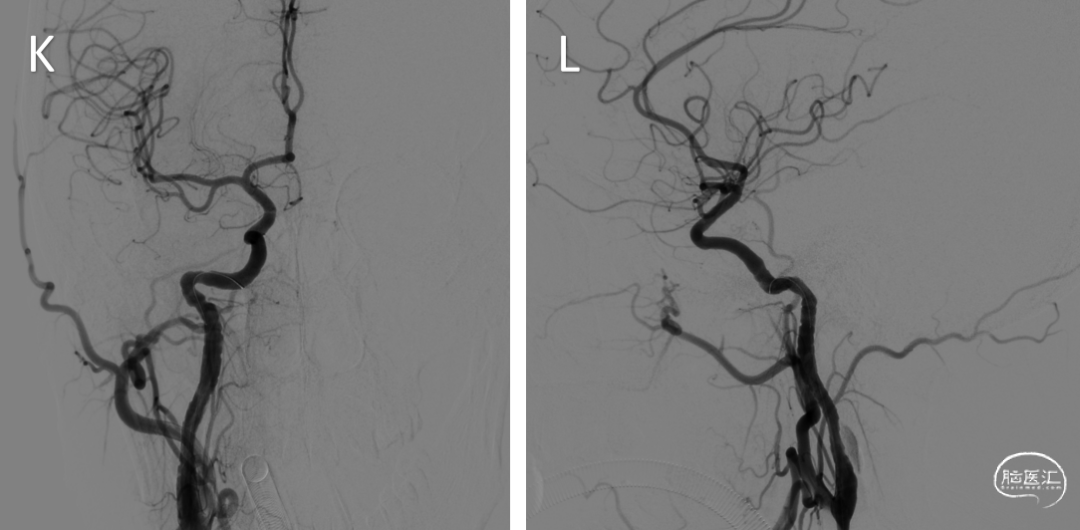
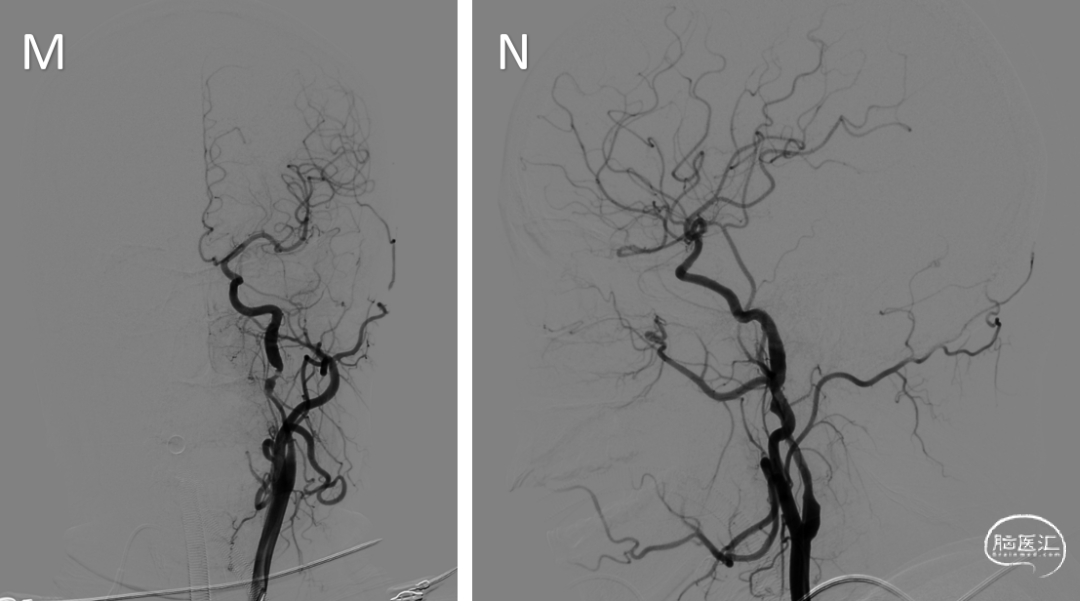
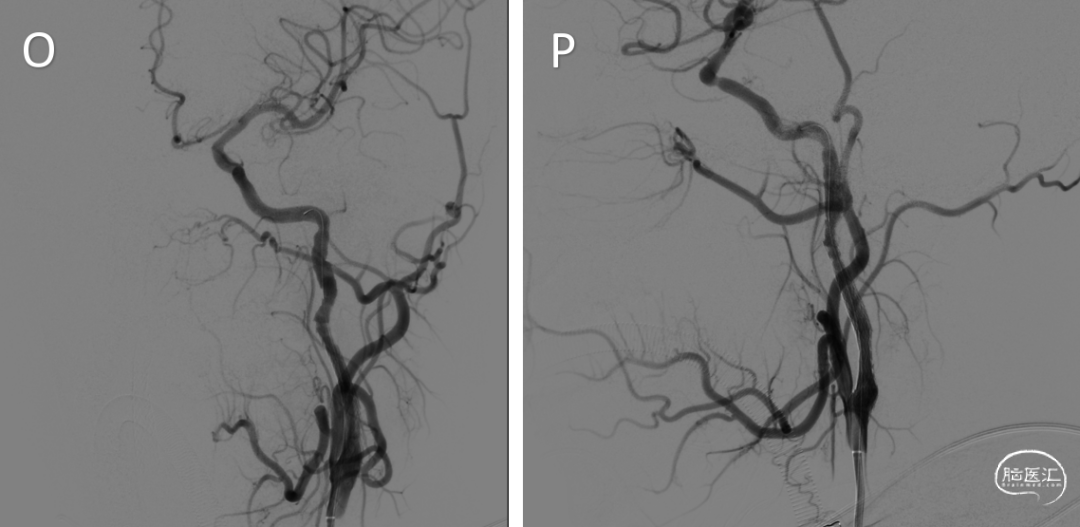
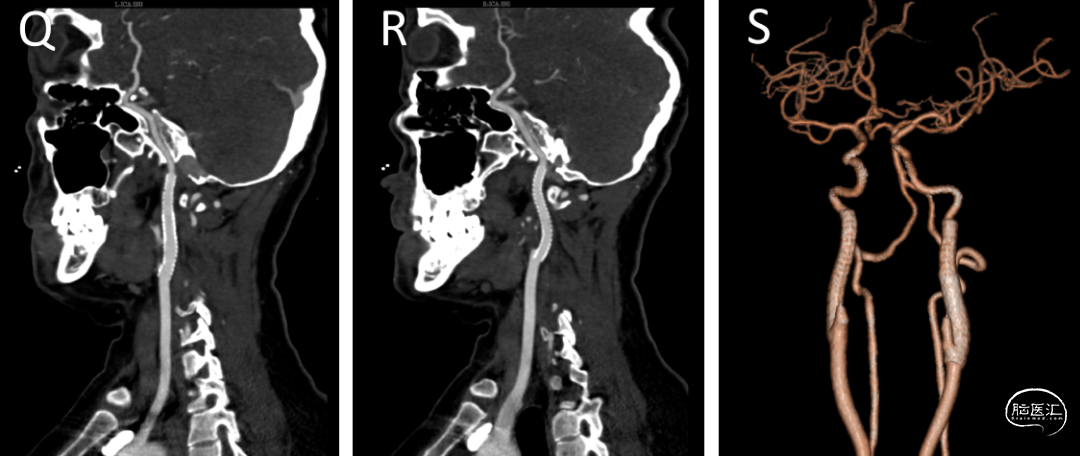
术后1个半月左右复查颈动脉CTA(2023-01-31)提示双侧颈内动脉C1段支架植入术后改变,支架贴壁良好,血管腔未见明显狭窄。
讨论
颈动脉夹层在普通人群的发病率很低,大约为2.6/10万人年。在北美的研究中颈动脉夹层发病平均年龄为45.8岁,欧洲的两个研究报道夹层的发病平均年龄分别为44.0和45.3岁。在北美研究中,50-52%的患者为女性,而在欧洲的研究中,男性占到53%-57%。
颈动脉夹层的病因有很多,首先分为外伤性夹层与非外伤性(自发性)夹层两大类。外伤性夹层往往具有明确的颈部受伤史,包括撞击、剪切、拉伸、旋转等多种方式,甚至颈部按摩也是可能的原因。自发性夹层可以与高血压、高同型半胱氨酸血症、Ehlers-Danlos综合征、Marfan综合征、感染、肌纤维发育不良、弥漫性甲状腺肿等相关。此外肥胖、吸烟也是不容忽视的因素。
颈动脉夹层主要的临床表现有以下几点: ①局部症状和体征。颈动脉夹层可单独或联合出现霍纳综合征;颈部疼痛或头痛;脑神经麻痹;耳鸣;以及少见的颈神经根损伤。突发的霍纳综合征,伴随头痛、颈部疼痛或同侧颈内动脉缺血性脑卒中等症状,被认为是颈内动脉夹层的特征性症状。少数时候疼痛可能是唯一的症状,这些疼痛有时类似于偏头痛,有时是丛集性头痛。②缺血性事件。颈动脉夹层引起的脑缺血(短暂性缺血发作或脑梗死)的临床表现与其他因素引起的脑缺血的临床表现一致。但颈内动脉夹层会导致视网膜缺血,椎动脉夹层会导致颈髓梗死。③其他症状。约1%的颈动脉夹层患者会发生蛛网膜下腔出血,通常是夹层延伸到血管的颅内部分,伴发了假性动脉瘤并破裂。约6%的颈动脉夹层患者无临床症状,通过体检时偶然发现。
颈动脉夹层往往存在以下的影像学改变。颈动脉夹层可表现为长锥形狭窄、锥形闭塞或夹层动脉瘤。研究表明在夹层患者中以狭窄型最为常见,其次为闭塞型和动脉瘤型。颈动脉夹层最典型、最特殊的征象是在颈MRI T1加权像上表现为动脉腔的增大,在缩小的管腔周围有一个新月形的高强度信号边缘。其他特征有动脉腔内游离的内膜瓣,假腔,长锥形狭窄和夹层动脉瘤。当没有动脉粥样硬化的证据时,长锥形狭窄通常提示夹层(通常在颈总动脉分叉以上2cm和椎动脉V3段出椎间孔后)。影像学阴性不能完全排除夹层的诊断,因为夹层血管可能会发生早期再通。
颈动脉夹层可以通过多种影像学方法诊断。彩色多普勒超声是诊断夹层的无创检查技术,但只能作为筛查工具,因为它高度依赖操作者的技巧 ,且对颅底和在横间孔附近处的夹层诊断率较差。高分辨增强磁共振成像可以提高急性期夹层壁间血肿的检出率。MRA和CTA是目前主要的检查手段。MRA结合MRI T1加权轴位扫描和黑血序列具有高灵敏度和特异性。CTA对于诊断夹层也非常具有价值,它可以比MRA显示更多的夹层特征。MRA与CTA经常互补协同使用。DSA是一种有创的检查方式,夹层通常在DSA上表现为串珠样狭窄或闭塞(火焰征),血管平滑或者不规则变细(鼠尾征、线样征),假性动脉瘤,游离的内膜瓣等特征,但DSA对 “双腔征”的检出率较低。
根据现有指南,颅外段颈动脉夹层的急性期通常给予抗凝或抗血小板治疗,以防止缺血事件发生和复发。多中心随机对照研究CADSIS研究证实两种治疗方法在缺血事件复发或者死亡的风险上没有明显统计学差异。当颈动脉颅外段有严重的狭窄、闭塞(有栓塞的风险)或假性动脉瘤时,抗凝药物可能优于抗血小板药物。当对抗凝药物有禁忌症或当夹层合并大面积脑梗死时,此情况有较高的出血转化风险,建议给予抗血小板治疗。当夹层患者仅有局部症状的情况下,是否应该选择抗血小板治疗仍然是一个争论的焦点。
抗栓治疗的最佳时间尚不清楚,后续的影像随诊对于指导治疗持续时间很重要。抗凝治疗通常不超过6个月,当夹层血管存在残余狭窄或闭塞,或动脉瘤的情况下,推荐长期给予抗血小板治疗。对于有潜在结缔组织疾病、颈动脉夹层家族史或肌纤维发育不良的患者,由于夹层复发的风险较高,建议进行更长、更密切的随访。
目前研究表明,在经严格评估后的颈动脉夹层患者中开展介入治疗(主要是支架置入)也是目前可以选择的办法。但血管内治疗循证医学证据有限,多为少量的队列研究或者个案报道。通常情况下针对颈动脉夹层的血管内治疗,目前能够使用的支架选择较为有限。单纯夹层不伴动脉瘤样扩张时,可以选择WallStent、Xact、Acculink、Xpert Pro等颈动脉支架,上述支架在开环闭环、金属覆盖率、柔顺性、支撑性等方面有所差别。当夹层伴动脉瘤样扩张膨出明显的时候,Pepline等血流导向装置也被用于临床治疗。在此例患者中,我们经过评估选择采用了目前较新的Xpert Pro自膨式支架,该支架到位性好,顺应性佳,尺寸选择丰富,尤其颈内动脉长节段病变,可能是颈内动脉长段夹层血管重塑血管内治疗较为适合的支架。结论
以颈动脉支架植入为主的血管内治疗是目前颈动脉夹层治疗的一种可以选择的方式。谨慎的评估,充分的沟通,合适的支架选择可能对部分患者带来益处,但是这种益处需要大样本,高质量的临床研究来进一步证实。
参考文献
[1] Debette S, Leys D. Cervical-artery dissections: Predisposing factors, diagnosis, and outcome. The Lancet. Neurology. 2009;8:668-678[2] Markus HS, Levi C, King A, et al. Antiplatelet Therapy vs Anticoagulation Therapy in Cervical Artery Dissection in Stroke Study (CADISS) Randomized Clinical Trial Final Results. J Vasc Surg. 2019; 70(6): 2098-2099;[3] Markus HS, Hayter E, Levi C, Feldman A, Venables G, et al. Antiplatelet treatment compared with anticoagulation treatment for cervical artery dissection (cadiss): A randomised trial. The Lancet. Neurology. 2015;14:361-367[4] Peng J, Liu Z, Luo C, et al. Treatment of Cervical Artery Dissection: Antithrombotics, Thrombolysis, and Endovascular Therapy. Biomed Res Int. 2017;10.1155/2017/3072098;[5] Pham M, Rahme R, Arnaout O, et al. Endovascular Stenting of Extracranial Carotid and Vertebral Artery Dissections: A Systematic Review of the Literature. Neurosurgery. 2011; 68(4): 856-66;[6] Traenka C, Jung S, Gralla J, et al. Endovascular Therapy versus Intravenous Thrombolysis In Cervical Artery Dissection Ischemic Stroke-Results From the SWISS registry. Eur Stroke J. 2018; 3(1): 47-56.
(本文由浙二神外周刊原创,浙江大学医学院附属第二医院神经外科徐丁主治医师整理,陈贤谊主任医师修改,许璟主任医师审校,张建民主任终审)
声明:脑医汇旗下神外资讯、神介资讯、神内资讯、脑医咨询、AiBrain 所发表内容之知识产权为脑医汇及主办方、原作者等相关权利人所有。
投稿邮箱:NAOYIHUI@163.com
未经许可,禁止进行转载、摘编、复制、裁切、录制等。经许可授权使用,亦须注明来源。欢迎转发、分享。















