
【大家说】栏目,关注脑疾病转化医学前沿,综合研究成果概述、研究作者自述和国内权威专家解读。本期栏目,我们特别邀请到来自首都医科大学附属北京天坛医院神经外科江涛教授、张伟教授,为我们解读并分享最新发表在Nature Medicine上的一项溶瘤病毒疗法联合帕博利珠单抗治疗复发性胶质母细胞瘤的I/II期临床试验结果。
一、研究概述
胶质母细胞瘤(GBM)是最常见且最致命的成人原发性脑肿瘤。新诊断GBM患者的标准治疗包括手术切除、术后同步放化疗以及替莫唑胺辅助治疗。虽然目前可最大限度地采用多模式治疗方法,但患者平均在确诊后7个月内仍会出现复发。更不幸的是,GBM的复发治疗选择寥寥无几,现行挽救疗法的疗效也非常有限,肿瘤进展后的中位生存期仅为6-8个月。因此,寻找有效的复发性GBM治疗方法迫在眉睫。
虽然抗PD-1或抗PD-L1抗体的免疫检查点抑制剂疗法已在其他癌症(包括脑内的转移性黑色素瘤)中实现了预后改善和客观缓解,但其作为单一疗法对复发性GBM的疗效有限,因为GBM的微环境具有固有的免疫抑制作用(即免疫“冷”肿瘤)。溶瘤病毒能够使肿瘤微环境重新调节至“热”表型,为免疫检查点抑制剂联合疗法提供了理论基础。
DNX-2401是一种在特定条件下进行复制并用于治疗高级别恶性胶质瘤的溶瘤腺病毒。该病毒在腺病毒dsDNA基因组中包含两个稳定的基因变化,使其在癌细胞中进行选择性有效复制。一项I期剂量递增研究表明,立体定向注射DNX-2401对高级别胶质瘤患者具有安全性,并分别在起初和后来通过直接溶瘤作用以及免疫浸润细胞的抗肿瘤反应诱导细胞死亡;瘤内使用单剂量DNX-2401后可带来持久性反应。

2023年5月15日,《Nature Medicine》(IF:87.241/Q1)刊登的一篇研究文章,报道了一项由两部分组成的、多中心、开放标签的I/II期临床试验(CAPTIVE)结果。该研究同时在美国神经外科医师协会(AANS)年会上作为最新摘要发表。这是首个将溶瘤病毒疗法联合免疫检查点阻断疗法用于治疗复发性胶质母细胞瘤的人体研究,试验中使用的溶瘤病毒正是DNX-2401,试验中使用的PD-1/PD-L1免疫检查点抑制剂则是帕博利珠单抗(Pembrolizumab、Keytruda)。

该研究共纳入了来自13个中心的49名患者(中位年龄为53岁,41%为女性),大多数患者(80%)在首次复发后就诊。
首先,患者接受了单剂量DNX-2401的治疗。研究组采用立体定向技术准确定位肿瘤,并通过一个小孔和特制导管注射病毒,由此递送溶瘤病毒。而后,自术后1周起,患者每3周接受一次抗PD-1抗体静脉输注。研究未观察到剂量限制性毒性反应,患者接受DNX-2401及帕博利珠单抗治疗的中位持续时间为153天,其中3名患者完成了完整的2年帕博利珠单抗疗程。
研究结果显示,在接受DNX-2401联合帕博利珠单抗治疗的49名患者中,客观缓解率(ORR)为10.4%(90% CI 4.2-20.7),高于预先设定的历史缓解率(5%),但未达到统计终点;患者在12个月的总生存率(OS)为52.7%(95% CI 40.1-69.2),高于预先设定的控制率(20%)。
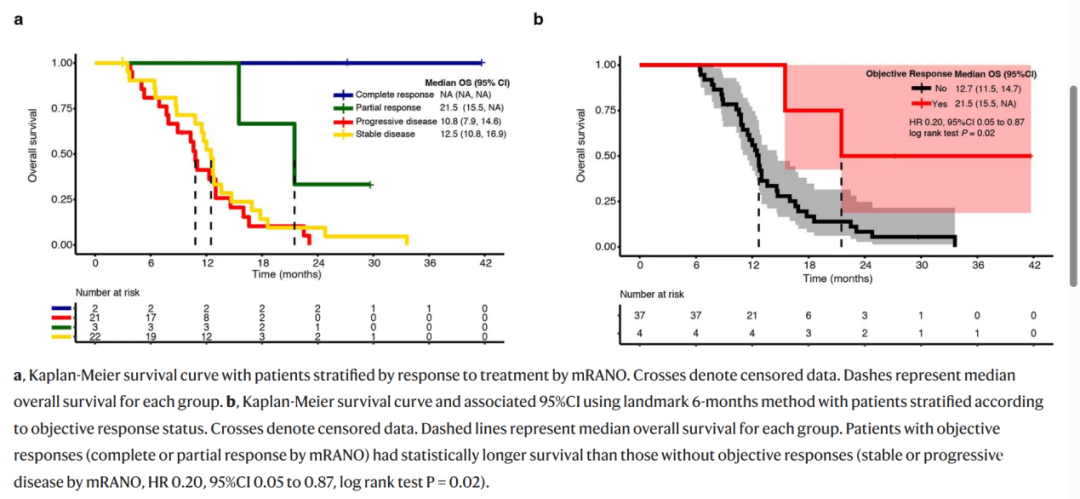

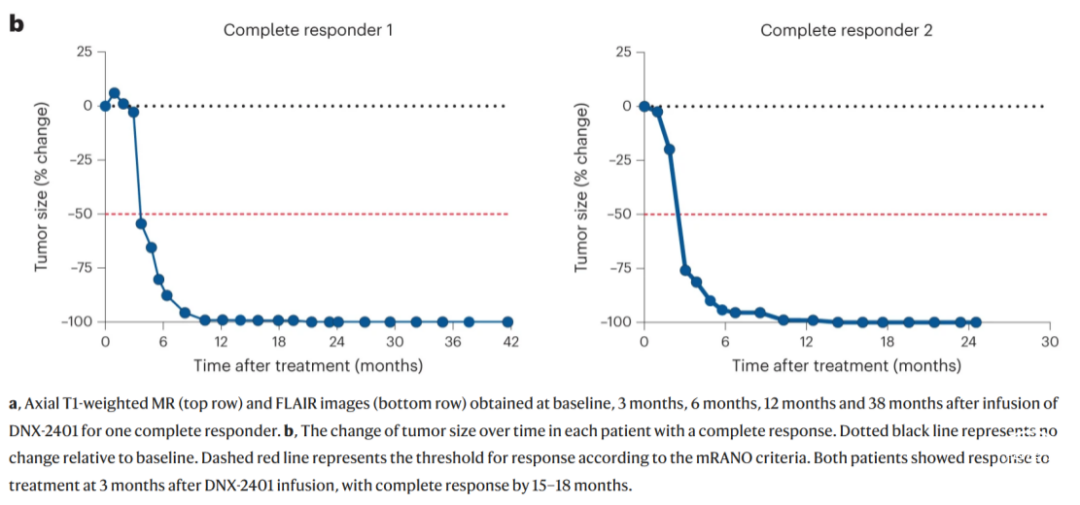
此外,客观缓解的结果进一步延长了患者的生存期(HR 0.20,95% CI 0.05-0.87);3名患者完成了治疗并有持久的治疗反应,其在术后45、48和60个月时仍存活。中位OS为12.5个月,出现治疗反应的平均时间为3个月;获得客观缓解的患者,其中位缓解时间为9.4个月。在有意向接受治疗的患者中,另有22名患者的病情稳定时间超过28天,因此临床获益率达到了56.2%(95% CI 41.1-70.5)。
综上,DNX-2401溶瘤病毒疗法联合帕博利珠单抗(Keytruda)未能达到I/II期研究的主要终点(复发性GBM患者的ORR),但这一联合疗法确实在选定患者中显示出了“显著的生存获益”。
此外,大多数被认为与治疗相关的不良事件(AE)为1级或2级事件,最常见的是脑水肿(37%)、头痛(31%)和疲劳(29%)。超过1名患者出现与治疗相关的严重AE,包括脑水肿(16%)、言语障碍(6%)和偏瘫(6%)。出现严重脑水肿的患者接受短疗程的地塞米松(89%)和/或其他伴随的支持性药物治疗,且均无需手术治疗。
同时,研究团队探索了用于GBM免疫疗法的潜在生物标志物,并通过使用基因表达数据发现,客观缓解仅发生于治疗前有PD-1中度表达伴炎症的肿瘤患者,且这些患者的生存时间更长。
为确定每位患者的肿瘤突变情况、基因表达和免疫特征,研究团队还进行了相关实验。在此当中,他们发现了关键的免疫特征,其最终可以帮助临床医生预测治疗反应并了解GBM的耐药机制。
接下来,研究团队将在随机临床试验中测试这一联合疗法相对于其他疗法的有效性。
+ + + + + + + + + + +
文章来源
二、作者自述
通讯作者、多伦多大学神经外科和玛格丽特公主癌症中心的高级科学家、Kembil脑研究所联合主任Gelareh Zadeh博士介绍说,“在接受标准治疗,即手术切除、同步放化疗和替莫唑胺辅助治疗之后,GBM患者最终的平均肿瘤复发时间为确诊后7个月。虽然免疫检查点抑制剂疗法改善了多种癌症的预后,但对复发性GBM的疗效有限,因为其肿瘤微环境具有固有的免疫抑制作用。”
资深作者、德克萨斯大学MD安德森癌症中心Frederick Lang博士补充道,“我们先前的试验显示,单用DNX-2401的患者在12个月的OS率为32%,而单用DNX-2401或PD-1抑制剂的患者,其OS中位数分别为9.3个月和9.8个月。研究表明,这种病毒不仅能直接杀死癌细胞,还能有效地激活患者的固有免疫系统,将免疫“冷”肿瘤转化为“热”肿瘤。因此,我们进一步评估了DNX-2401联合免疫检查点抑制剂疗法,我们现在看到该疗法可以改善部分患者的生存结果。
“这些药物(PD-1/PD-L1免疫检查点抑制剂)通过防止癌症躲避人体自身免疫反应来发挥作用,因此当肿瘤免疫不活跃时,这些药物几乎没有益处,正如GBM的情况,”Zadeh博士解释说,“溶瘤病毒可通过创造更有利的肿瘤微环境来克服这一限制,从而增强抗肿瘤免疫应答。溶瘤病毒联合免疫检查点抑制剂疗法会对肿瘤造成‘双重打击’;该病毒不仅会导致癌细胞直接死亡,而且可激发局部免疫活性并引起炎症,从而使癌细胞更易受到靶向免疫疗法的攻击。”
关于这项新的研究成果,研究团队在文中写道,“虽然研究结果未达到主要终点OS率,但其达到了12个月存活率的次要终点,这更具临床意义且比OS率更可靠。有客观缓解的患者的存活率令人振奋,这表明肿瘤控制改善了患者的生存。本项研究的结果很有应用前景,对这类未接受重复切除且缺乏有效和无毒疗法的患者而言尤其如此。”
Zadeh博士则表示,“本项研究的结果特别有意义,因为试验中的患者在复发时未接受肿瘤切除,而是仅仅接受了溶瘤病毒注射,这是GBM的一种新型疗法。所以能够在这项研究中看到这样的缓解效果是非常令人惊叹的。初步的临床试验结果展现出了很大的前景,我们对患者的长期临床获益保持谨慎乐观的态度。
第一作者、多伦多大学神经外科的高级住院医师Farshad Nassiri博士也表示,“这些结果给予我们莫大的鼓舞。近半数患者在临床上获益,他们的病情稳定或有所改善。我们也观察到了一些显著的治疗反应,包括肿瘤缩小,甚至有部分患者的肿瘤完全消失。3名患者分别在临床试验启动后45、48和60个月时仍然存活。我们认为,本项试验成功的关键是在使用全身免疫疗法之前将病毒直接递送至肿瘤。我们的研究结果清晰地表明,这种治疗方法是安全有效的。”
Zadeh博士最后总结道,“一般说来,癌症治疗中使用的药物并不适用于所有患者,但我们认为,部分GBM患者亚群会对该疗法产生良好的反应。我相信,这项结合基础科学和临床试验的转化研究工作,对推动GBM个性化治疗的发展具有关键意义。”
三、江涛教授、张伟教授的权威解读
先前的研究证明,依赖使用以免疫检查点分子为靶点的免疫治疗药物来治疗免疫“冷”肿瘤(如GBM)具有挑战性;此类“冷”肿瘤的特点,是微环境抑制T细胞活性并削弱随后的免疫应答,从而使免疫检查点抑制剂失效。事实上,有别于常规对免疫检查点抑制剂有应答的肿瘤微环境(如黑色素瘤或肺癌),GBM的微环境中富含髓源性抑制细胞和肿瘤相关的巨噬细胞,而不是淋巴细胞。新型疗法已经转用免疫疗法和协同作用机制的联合策略,希望由此克服GBM的免疫抑制微环境。具体来讲,就是首先激活这些髓系细胞,诱导抗肿瘤免疫应答。
目前为止,DNX-2401的数据支持这一溶瘤病毒可在免疫“冷”肿瘤内引发免疫应答的观点。这项新研究显示,接受DNX-2401联合经典的PD-1免疫检查点抑制剂治疗的患者,其12个月OS率为52.7%,OR率为10.4%。
这项研究还提出了GBM免疫治疗的潜在生物标志物。研究者发现,只有PD-1表达和炎症程度中等(基于治疗前免疫细胞浸润水平)的肿瘤患者获得了客观缓解。此外,具有这些肿瘤特征的患者比该试验中其他接受治疗的患者存活时间更长。
本项研究结束后,下一步应开展随机对照临床试验,从而对DNX-2401联合帕博利珠单抗疗法进行对照评估。
专家介绍
江涛 教授
首都医科大学附属北京天坛医院
医学博士,主任医师
首都医科大学教授,博士生导师
首都医科大学附属北京天坛医院神经外科学中心主任,北京市神经外科研究所所长,北京脑重大疾病研究院脑肿瘤研究所所长
担任中国医师协会脑胶质瘤专业委员会首任主任委员,中国抗癌协会脑胶质瘤专委会首任主任委员,中国脑胶质瘤协作组首任组长等
作为首席专家主持国家科技部“十一五”支撑计划重点项目、国家科技部“863”重大科技专项项目、国家重大研发计划精准医学专项等;中国脑胶质瘤基因组图谱计划(CGGA)与亚洲脑胶质瘤基因组图谱计划(AGGA)的发起人和创建者
以通讯作者在Cell、Genome Research、PNAS、Clinical Cancer Research、Neuro-Oncology等SCI期刊发表论文200余篇;连续入选Elsevier高被引学者榜,在我国神经外科领域学术影响力排名第一
2019年入选北京学者;以第一完成人获得国家科技进步二等奖、教育部科学技术进步一等奖等,成果获评2018年“中国生命科学十大进展”、2021年“中国生物信息学十大进展”
主持制定国家卫健委《脑胶质瘤诊疗指南(2022年版)》等多部行业指南
张伟 教授
首都医科大学附属北京天坛医院
医学博士,美国MD安德森癌症中心博士后
主任医师、教授、博士生导师
首都医科大学附属北京天坛医院神经外科学中心副主任兼神经肿瘤外科5病区主任
青年北京学者,北京市百千万人才工程,北京市青年拔尖人才,北京市科技新星,第三届“国之名医-青年新锐”荣誉称号
中国抗癌协会青年理事会理事,国家神经疾病医学中心脑胶质瘤MDT专科联盟常务理事,国家神经系统疾病医疗质量控制中心神经外科亚专业质控工作组秘书,中国医师协会脑胶质瘤专业委员会青年委员会副主任委员,中国抗癌协会脑胶质瘤专业委员会常务委员,中国神经科学学会神经肿瘤分会常务委员,中国抗癌协会脑胶质瘤专业委员会国际学术交流与合作学组秘书长,北京抗癌协会青年理事会理事等
以通讯/第一作者在国际知名期刊Brain、Proc Natl Acad Sci USA、Neuro-Oncology、Journal of Pathology、Neurosurgery等发表SCI收录论文52篇,H指数34,FWCI值2.75;被Nature Review Neurology等他引3546次,单篇最高被引273次,入选Wiley中国开放科学2022年度作者
主编/副主编中文专著4部,参编专著10部,参译专著2部。授权国家发明专利9项,计算机软著1项,申请美国及欧盟专利各4项,其中4项已实现转化
参与制定国家卫健委《脑胶质瘤诊疗指南2022版》等临床指南与专家共识12部,作为主要执笔人完成亚洲首个发布的脑胶质瘤国际指南,作为编写组组长完成《中国脑胶质瘤临床管理指南》。以主要完成人获国家科技进步二等奖、教育部科技进步一等奖等国家及省部级科技奖励6项
声明:脑医汇旗下神外资讯、神介资讯、神内资讯、脑医咨询、AiBrain 所发表内容之知识产权为脑医汇及主办方、原作者等相关权利人所有。








