
【大家说】栏目,关注脑疾病转化医学前沿,综合研究成果概述、研究作者自述和国内权威专家解读。本期栏目,我们特别邀请到来自复旦大学附属华山医院神经外科的张荣教授和来自上海交通大学医学院附属上海儿童医学中心血液肿瘤科的高怡瑾教授,为我们解读并分享最新发表在The NEW ENGLAND JOURNAL of MEDICINE上的一项将CAR-T细胞疗法应用于神经母细胞瘤患儿的研究成果。
一、研究概述
神经母细胞瘤(Neuroblastoma,NB)是最常见的交感神经系统肿瘤(97%),也是婴儿期最常见的恶性肿瘤,患儿确诊时中位年龄17个月。NB可以发生在交感神经系统的任何部位,包括肾上腺和从颈部到骨盆的椎旁神经组织。美国癌症协会(American Cancer Society)的数据显示,美国每年约有650名儿童被诊断为神经母细胞瘤,其中约半数儿童疾病在确诊时已存在远处转移,称之位高危组病例。高危NB的标准治疗方案包括诱导化疗、手术、自体干细胞移植和放疗,最后接受抗双唾液酸神经节苷脂(GD2)单克隆抗体联合细胞因子和异维A酸的免疫维持治疗。尽管如此,仍有很多儿童因NB死亡,占所有儿童癌症相关死亡的15%。

最近,来自罗马Bambino Gesù儿童医院的研究人员尝试了“CAR-T细胞疗法”,该策略对一些侵袭性血癌患者非常有效,但尚未被证明适用于其他类型的癌症。该项研究的结果发表在4月6日的《新英格兰医学杂志》(The NEW ENGLAND JOURNAL of MEDICINE)上。

CAR-T细胞疗法利用免疫系统创造出能够寻找和消灭肿瘤的“活药”。研究人员在实验室收集并加强了患者血液中的T细胞,再将其静脉输注回患者体内继续增殖。美国食品和药物管理局(FDA)目前已经批准了6种用于治疗血癌的CAR-T细胞疗法;部分早期患者已经获得治愈。但是,CAR-T细胞疗法在实体瘤中的成功率一直未被阐明。罗马Bambino Gesù儿童医院的研究者们开发了一种靶向GD2的第三代基因编辑自体CAR-T细胞疗法(GD2-CART01),并包含2个共刺激结构域(CD28和4-1BB),以此提高该新型疗法的效能和效力。他们进行了一项单中心I / II期剂量递增研究,以确定GD2-CART01的安全性、可行性以及II期试验的推荐剂量。

在2018年1月至2021年10月期间,共有27名患者入组并接受CAR-T治疗,中位年龄6.7岁,2/3(67%)为男性。26%的患者进行了MYCN扩增。既往治疗中位数为3次,范围为1-6次。约半数患者(52%)接受了抗GD单抗治疗。入组时,44%为难治性患者,51%为复发患者。
研究团队报告称,所有患者体内均成功生成了CAR-T细胞;在I期试验剂量中,未出现剂量限制的毒性作用,后推荐剂量定为10×106个CAR阳性T细胞/千克。
虽然有74%的患者出现了细胞因子释放综合征(输注T细胞使血液中充斥着一种被称为“细胞因子”的化学物质,可导致例如高烧、血压急剧下降等问题,严重者可能致命),但95%为轻型病例。仅1名患者出现3级并发症,给药托珠单抗后快速消失。1名患者出现意识状态的改变,后证明是因为脑出血;该患者接受了2次利米多赛(Rimiducid)输注,以诱导Caspase 9并破坏过继转移的GD2-CART01,进而导致T细胞迅速消除。
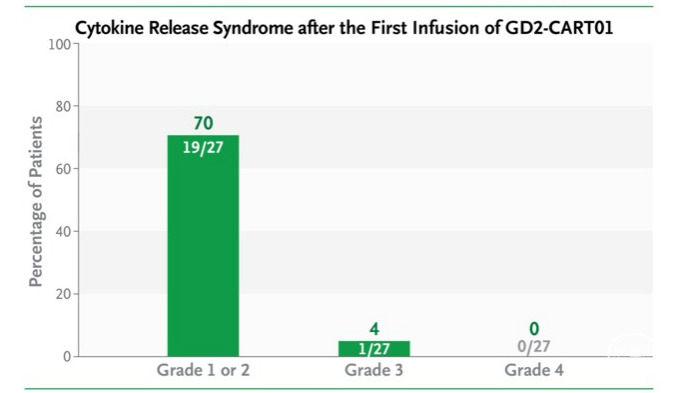
至关重要的是,研究结果显示有96%的患者在输注后30个月时,其外周血液中可检测到针对GD2的CAR-T细胞,中位持续时间为3个月。17名患儿(17/27)对治疗有反应。在这项研究中,总缓解率为63%,完全缓解率为33%,部分缓解率为30%。在接受推荐剂量CAR-T细胞的患者中,3年总生存率为60%,无事件生存率为36%。
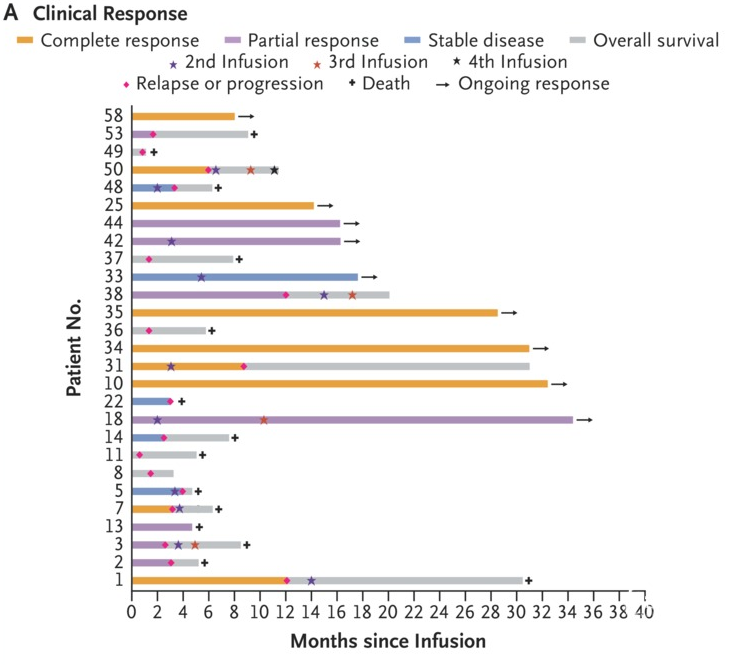

综上,CAR-T细胞疗法在这项小型试验中显示出了治疗NB的前景。
+ + + + + + + + + + +
文章来源
二、作者自述
通讯作者、罗马IRCCS耶稣儿童医院儿科血液学和肿瘤学系主任、天主教圣心大学儿科教授Franco Locatelli博士表示:“我们的研究结果表明,CAR-T细胞不仅是血液系统恶性肿瘤患者的有效治疗选择,对实体瘤患者也是如此。”
根据Locatelli教授的说法,先前的研究已经证实双唾液酸神经节苷脂GD2可在神经母细胞瘤的肿瘤细胞表面高度表达,使其成为一个具有吸引力的治疗靶点。“另一方面,我们还在编码序列中添加了自杀基因或安全开关,从而改善这一疗法的安全性。”Locatelli教授说:“事实上,这种自杀基因可以在药物疗法无法控制的严重病例或危及生命的毒性环境中被激活。”
“我们将致力于增加对GD2-CART01有反应的患者比例,并延长其治疗反应的持久性。”据Locatelli教授称,未来的研究拟对GD2-CART01作为神经母细胞瘤患者的早期治疗手段进行评估。他表示,“我们期待该疗法可转化为更好的结果”。

三、张荣、高怡瑾教授的权威解读
神经母细胞瘤(Neuroblastoma,NB)属于胚胎性神经内分泌肿瘤,是儿童最常见的颅外实体肿瘤,约占所有儿童肿瘤的10%。中枢神经系统(CNS)神经母细胞瘤属于罕见颅内胚胎性肿瘤,确切起源仍然未知,其特征是通过染色体重排导致转录因子叉头盒R2(FOXR2)基因表达增加。
即使接受目前标准一线治疗,儿童高危NB 5年无事件生存率(Event-free survival,EFS)仍仅徘徊于40%~50%之间。如果一线治疗失败,挽救治疗选择非常有限,长期存活率仅5%~10%,且伴随严重远期不良事件,包括听力丧失、矮小,无生育力和二次肿瘤的风险。颅内CNS神经母细胞瘤尚无标准治疗方案,手术最大限度安全切除病灶,然后及时接受类似高危髓母细胞瘤的放疗和化疗方案是目前较多采用的治疗策略。
通过特异性细胞疗法——包括嵌合性抗原受体T细胞(CAR T细胞)、自然杀伤细胞、树突状细胞和半相合干细胞等,治疗高危和难治/复发NB一直非常令人感兴趣,但既往临床研究显示效果有限。此种状况却随着2023年4月6日发表于《新英格兰医学杂志》(The NEW ENGLAND JOURNAL of MEDICINE)上一项采用表达可诱导Caspase 9自杀基因的自体第三代GD2-CART01治疗复发/难治高危NB的单中心I/II期临床研究而发生改变。
该研究亮点,包括以下几个方面:
1
自体第三代GD2-CART01制备工艺可行;
2
GD2-CART01相关细胞因子释放综合症轻微并可逆;
3
单次输注GD2-CART01可在体内存在至少3月,病人可接受多次输注;
4
即使激活Caspase 9自杀基因,GD2-CART01仍具备重新扩增能力;
5
接受推荐剂量GD2-CART01的病人(之前已经接受过2~6种治疗),3年总体生存率(Overall survival,OS)和EFS分别可达60%和36%;
6
GD2-CART01分布广泛,可通过血脑屏障进入脑脊液,但无中枢神经毒性发生。
近年,也有GD2 CAR-T治疗H3K27M突变型儿童弥漫中线胶质瘤的成功报道,这些均提示,CAR-T细胞疗法未来对颅内CNS神经母细胞瘤患者有极大的应用前景。
另一方面,也应看到研究结果未来临床应用前景的不确定性:
1
进入筛选的30例病人中,2例在计划接受GD2-CART01前疾病已经进展;
2
既往治疗(尤其是已经成为标准一线治疗的抗GD2单克隆抗体)是否会干扰GD2-CART01疗效,尚不明确;
3
GD2-CART01远期疗效,有待延长随访时间;
4
GD2-CART01对软组织、骨骼和淋巴结病灶(尤其是大病灶)疗效欠佳,肿瘤高负荷病人,3年OS和EFS均为0%。
这些不确定性也提示,无论是目前研究中的NB还是未来具有潜在应用前景的颅内CNS神经母细胞瘤,CAR-T细胞疗法都需要结合其他治疗手段才能发挥其最大作用。
我们还应该注意到这项试验中的局限性。首先,神经母细胞瘤是一种高度异质性癌症,从惰性到侵袭性不等,任何相关的单臂、单中心试验结果均需仔细解读。其次,作为一项小型研究,在CAR-T细胞疗法成为NB“广受认可”的疗法之前,我们还需要进行更大规模的试验。目前,人们尚不清楚CAR-T细胞疗法是否比现行标准疗法更有效,也未阐明为何仅部分神经母细胞瘤儿童患者可通过CAR-T细胞获得缓解。
即使存在这些不确定性和局限性,作为迄今最大的实体瘤CAR-T细胞治疗的病例系列,且60%的患者获得了客观缓解,其中半数为完全缓解,此研究对NB乃至颅内CNS 神经母细胞瘤治疗都具有“里程碑式”意义,它不仅为高危NB治疗模式和预期结果从传统细胞毒药物时代向靶向精准“新治疗”时代转变增添了新“证据”,更表明CAR T细胞治疗不仅适用于B细胞血液肿瘤,也可使实体肿瘤病人获益。
专家介绍
张荣 教授
复旦大学附属华山医院
医学博士,复旦大学附属华山医院神经外科教授,小儿神经外科组长
国际小儿神经外科协会(ISPN)委员
中国医药教育协会小儿神经外科(互联网)副主任委员
上海市医学会小儿外科学会委员
上海市抗癌协会儿童肿瘤专业委员会副主任委员
曾任中华医学会神经外科学会小儿神经外科学组副组长,上海医学会神经外科学会小儿神经外科学组副组长,中国医师协会小儿神经外科专家委员会委员,中国医师协会胶质瘤委员会生殖细胞肿瘤组副组长,中国医师协会胶质瘤专业委员会小儿组委员
长期从事神经外科临床工作,擅长小儿神经系统肿瘤和先天性畸形的诊断和治疗
高怡瑾 教授
上海交通大学医学院附属上海儿童医学中心
血液肿瘤科主任医师
中国抗癌协会小儿肿瘤专业委会副主任委员(8th、9th),中华医学会儿科学分会肿瘤学组副组长,中国研究型医学院儿童肿瘤专业委员会副主任委员
上海市抗癌协会儿童肿瘤专业委员会主任委员
先后在香港中文大学威尔斯亲王医院、奥地利Tyrolean肿瘤研究所、美国MD Anderson肿瘤中心、美国Common Wealth University Virginia和美国St. Jude儿童研究院访学;并于2018年4月-2019年4月在美国Cincinnati Children‘s Hospital Medical Center肿瘤血液病研究所(CBDI)工作一年
擅长领域:主要兴趣淋巴瘤和组织细胞疾病,并负责各种实体肿瘤(包括神经肿瘤)治疗
声明:脑医汇旗下神外资讯、神介资讯、神内资讯、脑医咨询、AiBrain 所发表内容之知识产权为脑医汇及主办方、原作者等相关权利人所有。








