原创首发于【神内资讯】微信公众号
本文带来上海交通大学医学院附属新华医院神经内科干静教授在<第十二届东方神经病学会议·青年论坛(二)>分享的《帕金森病步态障碍的诊治》内容,欢迎大家阅读、分享。
✦
✦ ✦
步态评估方法
常用评估方法
» 观察性量表或问卷
» 行为测试(eg,Timed Up&Go Test,mini-BESTest,10-MWT)
» 仪器化步态分析(基于传感器的方法对步态的更精细测量进行评估)
利用高速摄影,三维动作捕捉系统、压力测试设备;可穿戴传感器;VR等


lansek R, et al. Mov Disord. 2006
Bouça-Machado R, et al. J Parkinsons Dis. 2020
NO.1
帕金森病步态障碍临床特征
✦
✦ ✦
帕金森病步态障碍
帕金森病步态障碍
» 帕金森病患者存在不同程度的步态障碍,运动和非运动特征对步态的影响
• 拖曳步态、慌张步态、冻结步态、姿势不稳、跌倒
• 限制日常活动、增加照料者负担
» 这些步态障碍症状对PD患者生活质量造成负面影响

Giladi N, et al. Mov Disord.2008
PD患者的步态障碍随着病情进展
表现出不同的特征

Lancet Neurol 2019
PD患者的步态障碍在疾病早期的特征
» 不对称性是PD早期重要特征
» 步长和步速与疾病进展程度相关


中华神经科杂志2020;53:7
PD患者步态参数在疾病进展过程中
出现特征性演变
» 步态参数众多,尚未确定病程中变化敏感的步态参数
» 需要明确PD步态异常在不同阶段的特征性表现及动态演变过程

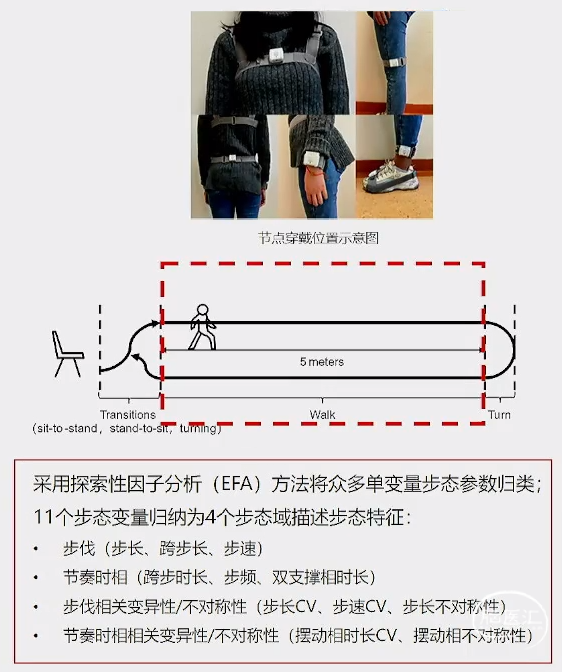
中华神经科杂志2022;7:706
研究结果:
帕金森病患者的步态异常贯穿疾病全过程,不同时期步态受损特征不同:
H-Y分级1级时节奏时相相关变异性/不对称性即表现出与健康对照组的差异;
至H-Y 分级2级步伐开始出现明显受损,并随着疾病进展而加重;
至HI-Y分级3级时步伐相关变异性/不对称性到出现明显受损。
结论:PD患者在疾病进展过程中步态参数出现特征性演变:
» 与运动分型无明显相关
» 节奏时相相关变异性/不对称性可能是区分早期帕金森病与健康人群的标志;
» 步伐和步伐相关变异性/不对称性是评估帕金森病疾病进展的重要步态指标。
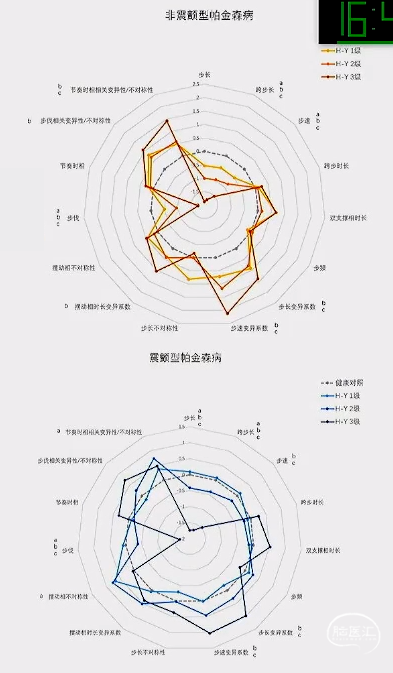
中华神经科杂志2022;7:70
NO.2
帕金森病冻结步态特点
✦
✦ ✦
冻结步态
帕金森病冻结步态 (FOG)
» 步态冻结指患者在起步、转弯以及接近目标/即将到达目的地时突然出现某些异常的下肢运动阻滞动作。“尽管有步行的意愿,但是脚步的前向运动出现短暂性、发作性缺失或明显减少”
» 易发生于:起步、转弯、靠近目的地、穿过狭窄空间、紧张;
» 目前对于评估冻结步态的“金标准”是运动障碍学家对冻结发作临床表现的视觉识别。
Giladi N, et al. Mov Disord.2008
帕金森病冻结步态分型
» 按多巴反应分型:多巴反应型、多巴抵抗型、多巴诱导型
» 按照临床特点分型:原地颤抖型、小步伐拖足行进型、完全运动不能型
» 按触发因素分型:运动型、认知型、边缘系统型(存在明显的网络特征和异常)

Movement Disorders 2019
Espay AJ,Neurology 2012
✦
✦ ✦
冻结步态流行病学
» H&Y分级越高,冻结步态发生率越高;
» 临床异质性明显
» 冻结步态严重程度影响患者生活质量

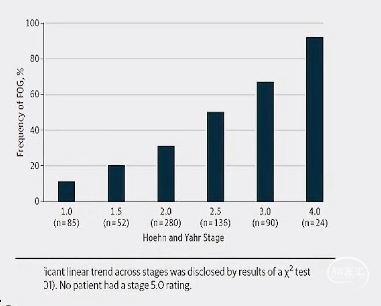
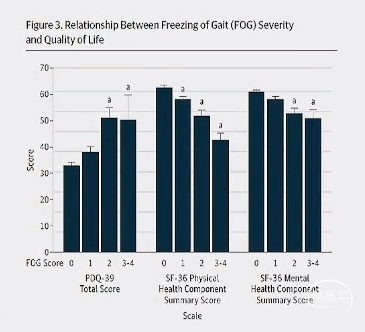
JAMA Neurol 2014:71(7):884-90.
» 来自中国的研究 (中国6大区域12个分中心)
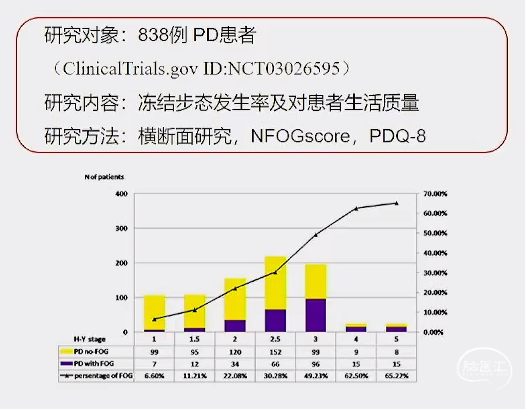
中国PD-FOG发生率约30%,并随着疾病严重程度的增加而升高。直接降低患者生活质量,在所有对PD患者可能造成负面影响的因素中占比为第三位,仅次于抑郁和肢体运动症状。
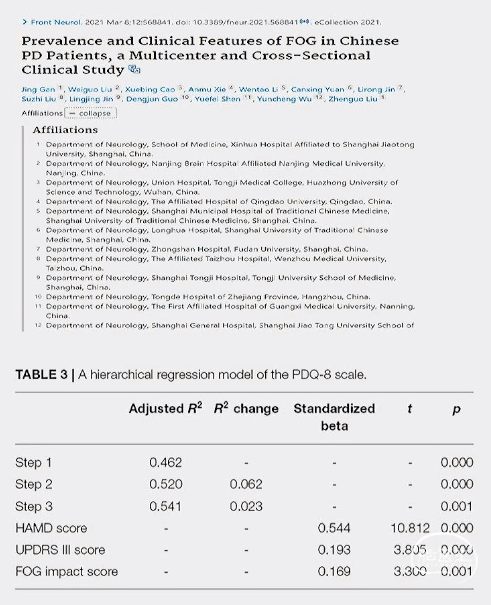
Front Neural.2021;12:568841.
✦
✦ ✦
冻结步态发生的预测因素
帕金森病冻结步态预测因素
» 冻结步态的特点,早期隐匿,是否预测冻结步态的发生
» 已有一些研究报告了预测FOG发病的危险因素
• 来自于小型的、单中心的开发数据集
• 代表性和可信度是有限
• 纵向随访研究较少,横断面研究并无预测能力
• 未提供可供临床操作的预测工具
Snijders A H, et al. Parkinsonism Relat Disord. 2012
Martens K A E, et al. Mov Disord. 2018
Fontiers in Neurology 2022
✦
✦ ✦
冻结步态特点
帕金森病冻结步态异质性明显
» 基因背景
• LRRK2 G2019S突变携带者表现步态障碍为最初症状多,PIGD亚型概率明显增高,突变携带者步态运动学异常 (快速步态或双任务步态条件下,增加步幅时间的可变性,步态变异性增加)
• GBA杂合突变携带者,PD易感性增加,步态障碍、FOG和姿势不稳的发生率更高;5年纵向随访后与FOG进展率相关,GBA突变是FOG的独立风险。
» 神经递质
多巴胺能、肾上腺素能、谷氨酸能、y-氨基丁酸能、胆碱能系统的不同异常
去甲肾上腺素转运体 (NET)-PET: 与NO-FOG组相比,OFF-FOG组的全脑NET结合显著降低,在额叶、左右丘脑、颞叶和蓝斑区域性分布,在右侧丘脑的影响最强
» 神经网络异常
Neurobiol Dis.2023:106048.
Neuroimage Clin.2023;37:103342.
J Neurol.2023.doi: 10.1007/s00415-023-11612-6
✦
✦ ✦
冻结步态预测模型
本课题组:基于多中心随访队列,建立临床风险预测模型,预测PD患者未来出现FOG的风险
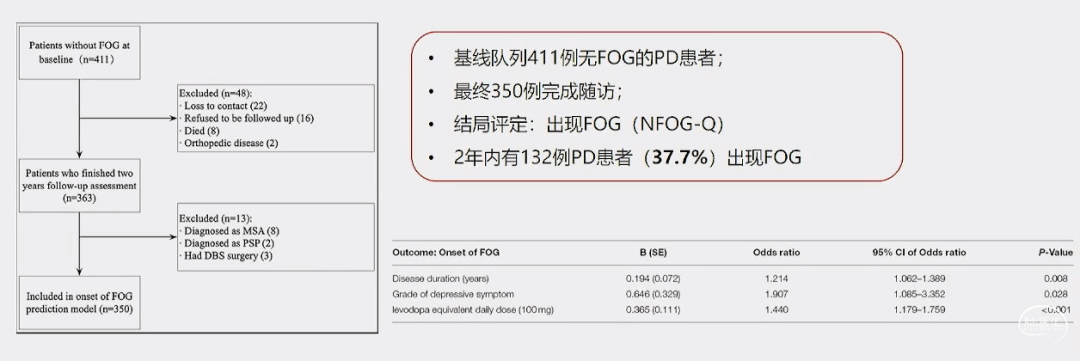
Front Neurol.2022;12:758580.

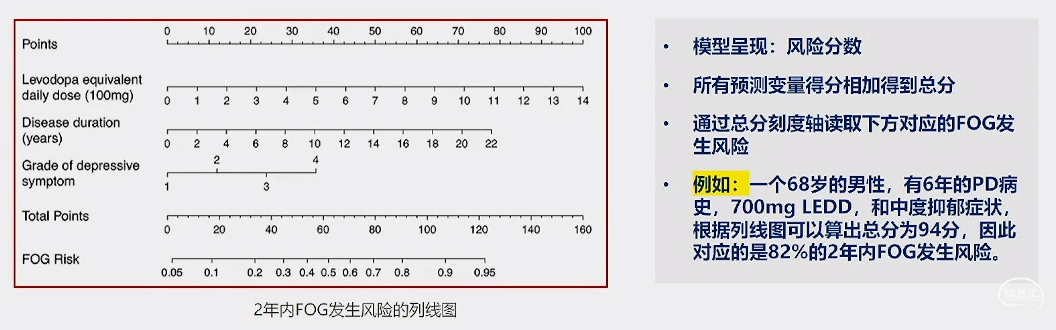
• 基于三个易于获得的临床参数建立了未来FOG发生风险的预测模型:较长的病程,更高的抑郁症状严重程度,以及更高剂量的LEDD与未来FOG的发生有关
Front Neurol.2022;12:758580.
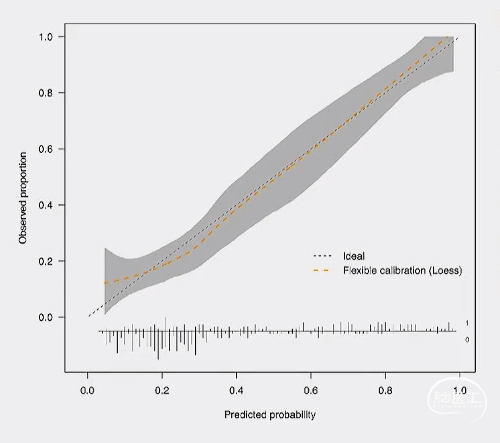

• 模型经过合理的校准与内部验证,拥有较好的预测性能
意义:早期识别出有发生FOG风险的个体,有助于对个体患者的预后进行判断和及早干预,并使临床医生能够更好地全程管理PD。
Front Neurol.2022;12:758580.
NO.3
帕金森病步态障碍的神经影像改变
✦
✦ ✦
帕金森病步态障碍的神经影像改变
脑结构改变
» 与健康人相比,步态受损的帕金森病患者在几个大脑区域出现萎缩,并有偏侧化变化的证据
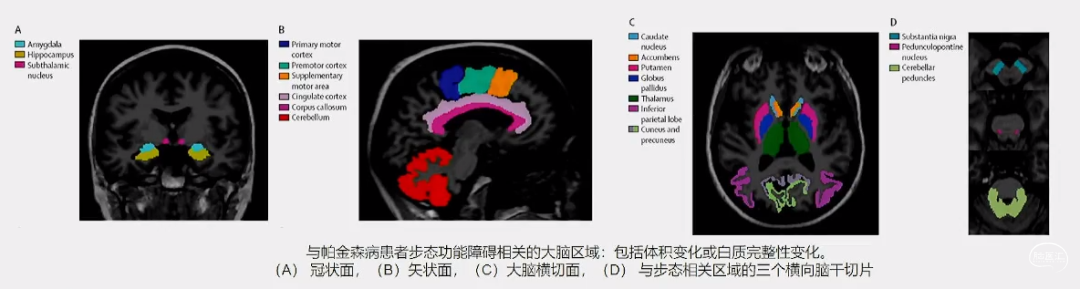
灰质变化:在特定的皮质区域以及额叶和顶叶区域显著缺失。皮质运动区(初级运动区、运前动区和辅助运动区)以及扣带回、皮质非运动区(顶下小叶、楔部和楔前叶)、皮质下结构(杏仁核、海马和丘脑底核)出现萎缩;小脑;脑干(脑桥脚核和黑质)、基底节(尾状核和壳核)和丘脑;背外侧、额叶和内侧皮质厚度减少
白质完整性变化:胼胝体白质扩散张量变化;黑质和PPN核的扩散张量变化(如各向异性分数FA降低和平均扩散率MD增加)与步态冻结的严重程度有关。广泛的长WM束的损伤,以及皮质和皮质下脑区中与运动相关的结构连接障碍。
Lancet Neurol 2019
» PD-FOG广泛皮质/皮质下萎缩,涉及多个皮质和皮质下结构的白质损伤
» PD-FOG转换较未转换者在感觉运动区和基底节中表现出萎缩,顶叶萎缩为明显
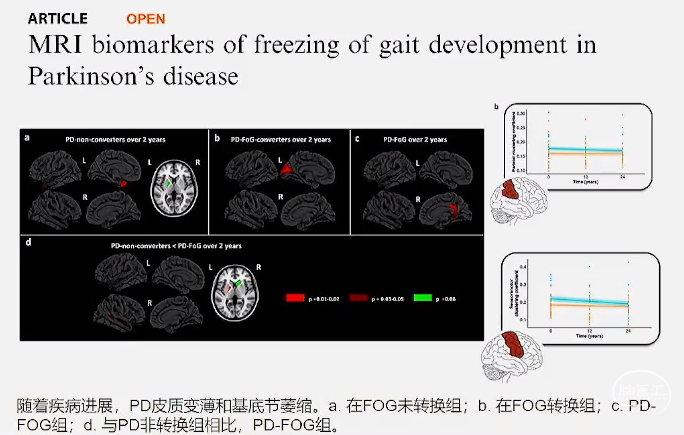
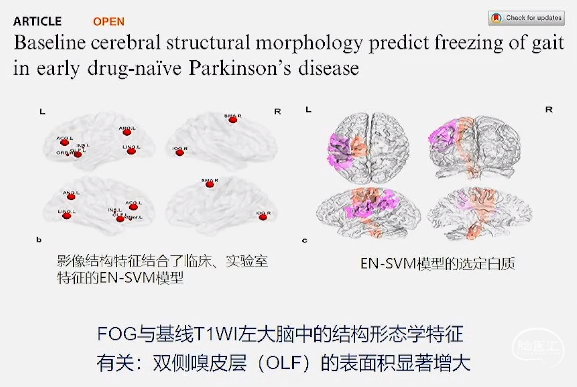
NPJ Parkinsons Dis.2022;8(1):158.
NPJ Parkinsons Dis.2022;8(1):176.
脑功能不同研究及分析方法
» 研究方法:静息态、任务态 (包括运动想象、虚拟现实刺激、运动任务和作为步态功能替代物的双任务范式)
» 分析方法: 全脑分析、感兴趣区分析、拓扑网络......
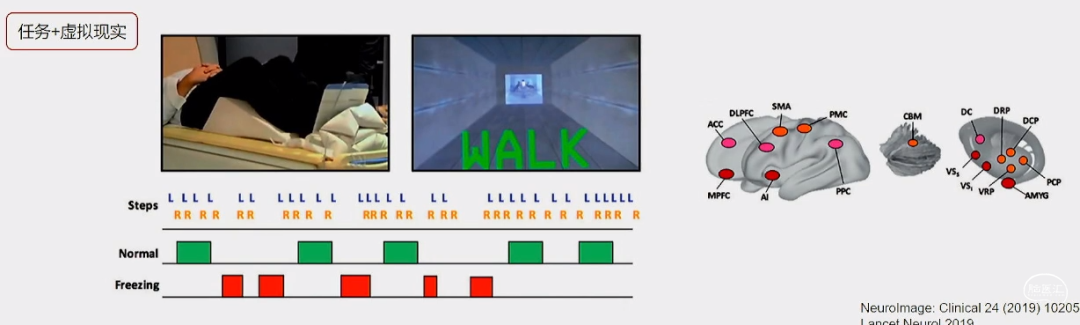
Neurolmage: Clinical 24 (2019) 102059
Lancet Neurol 2019
Brain 2018;1:1-16
脑功能改变
» 负责额叶执行和注意能力的大脑区域(即额叶和额叶纹状体网络)存在异常的功能激活和连通性。
» 大脑后部而非前部区域的功能激活和连通性异常,特别是负责视觉空间能力的区域(即顶枕网络)
» 涉及运动网络(即MLR和CLR)的大脑皮层下区域的功能失连接
Lancet Neurol 2019
Plos One 2014;e100291
步态联合神经影像学研究+探索性ALE荟萃分析:
• 步态需SMA参与,但在PD组行走期间 SMA的激活较老年对照组减少,PD中SMA激活较低可能是多巴胺能失神经后纹状体功能减低的结果。SMA激活减少可能是PD步态控制受损的标志。
• PD患者的步态始终与整个小脑,特别是小脑运动区(CLR)的激活增加相关,表明CLR激活可能在运动中起补偿作用。
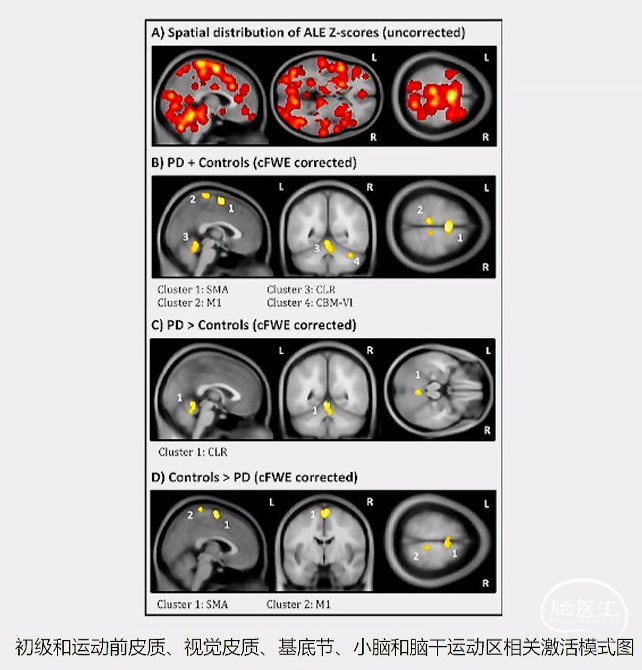
Curr Neurol Neurosci Rep 2019;19(8):49.
脑代谢改变
» PET/SPECT:神经递质活性、脑灌注和葡萄糖代谢的脑变化
» PET/SPECT:多巴胺能、胆碱能和去甲肾上腺素能传递的异常模式以及PD-FOG的灌注和代谢变化
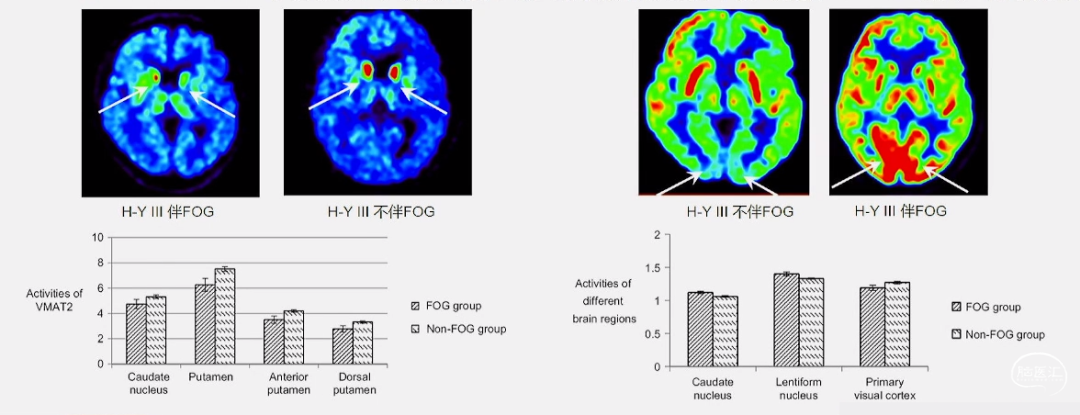
Neuropsychiatric Disease and Treatment 2019:15
NO.4
帕金森病步态障碍的机制
✦
✦ ✦
行走和步态
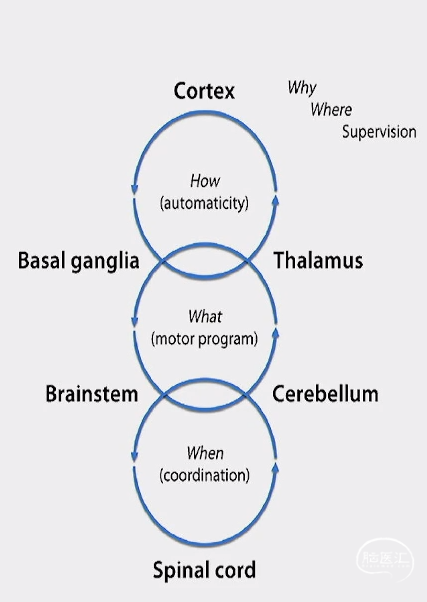
步态相关解剖基础
» 运动皮层和运动皮层前区发出行走的冲动通过神经纤维传至基底节;
» 由基底节核团发放去抑制信号经过神经纤维传递至脑干运动负责区域;
» 中脑通过脑桥延髓网状结构 (PMRF) 发放起始或更改行走特征的信号至脊髓运动前脚执行;
» 小脑负责协调
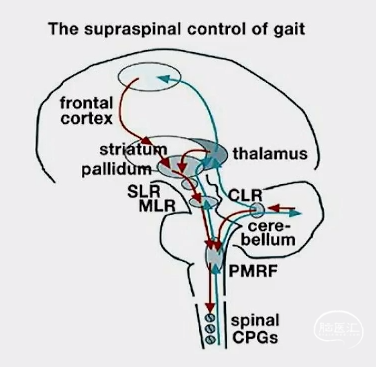
✦
✦ ✦
帕金森病步态障碍可能机制
冻结步态机制模型假说
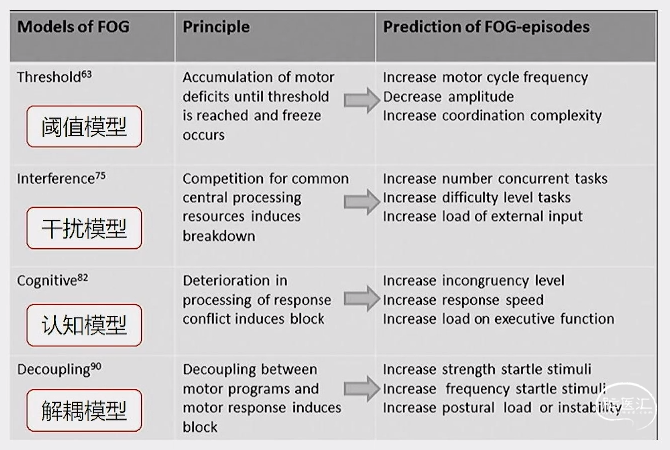
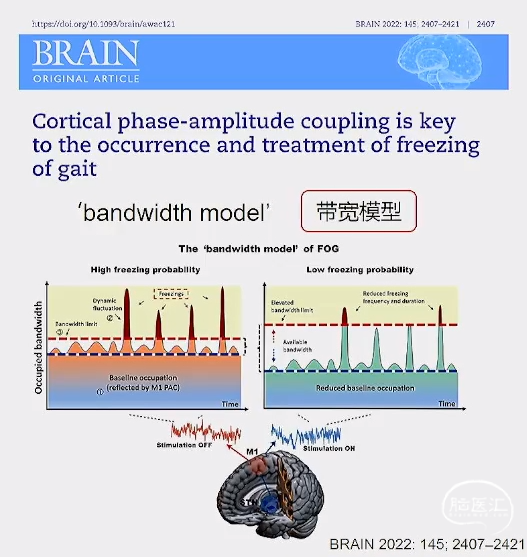
BRAIN 2022:145;2407-2421
Mov Disord 2013; 28 (11) : 1509
步态障碍神经机制 (跨多个层次的神经网络)
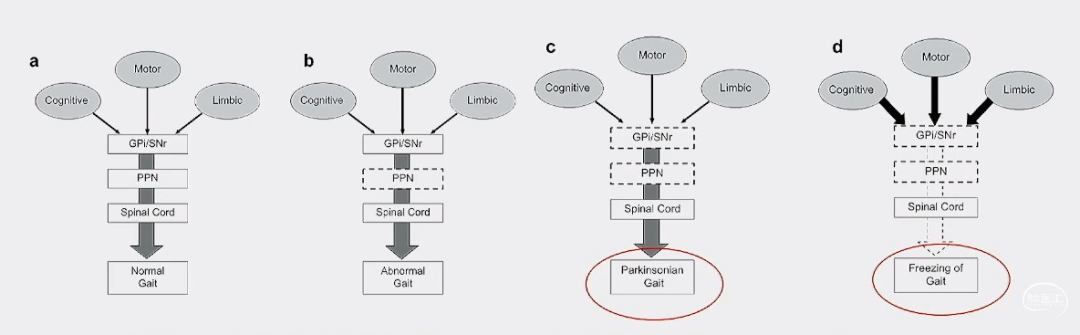
• 正常步态依赖于皮层和皮层下区域的正常运行;PPN损伤(非多巴胺能机制)干扰正常步态;
• 基底节输出增加对PPN过度抑制,临床上表现为帕金森病步态;在PD中,GPi /SNr中可逆的过度活动周期会导致PPN的阵发性失活,从而触发FOG发作 (cross-talk model)
Parkinsonism and Related Disorders 15(2009) 333-338
NO.5
帕金森病步态障碍的治疗
✦
✦ ✦
帕金森病步态障碍的治疗共识推荐
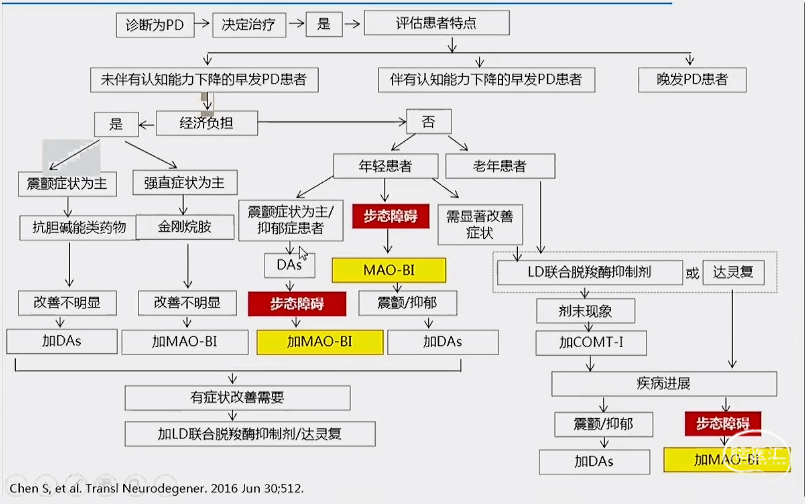

Mov Disord.2018 Aug;33(8):1248-1266.
✦
✦ ✦
帕金森病冻结步态的治疗
药物
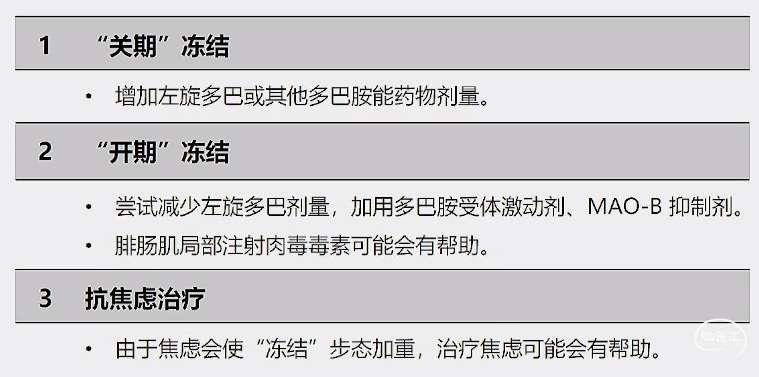
手术
» STN-DBS对关期冻结可能有效
» 经药物调整,治疗效果仍不满意者,建议可尝试桥脚间核DBS (PPN-DBS) 治疗。
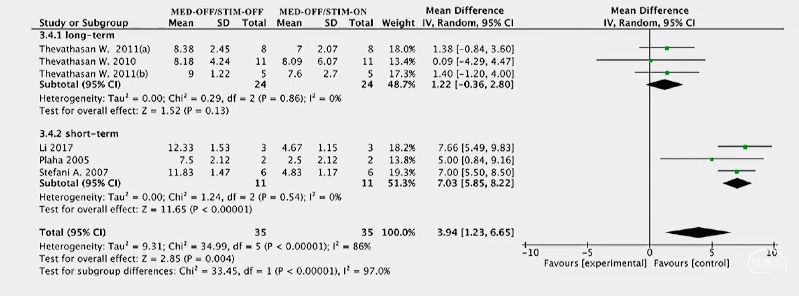
系统评价及Meta分析:PPN-DBS手术可能改善术后“冻结”步态的严重程度
Neurochem Res,2020,45(4): 709-719.
非药物非手术治疗

治疗目标:
• 诱导皮质纹状体通路发生永久性变化的疗法;
• 引起运动执行网络(所有形式的提示)暂时改变的疗法
» 感觉提示
» 非侵袭性电刺激:tDCS、rTMS、外周刺激
» 认知训练
» 运动和体育锻炼
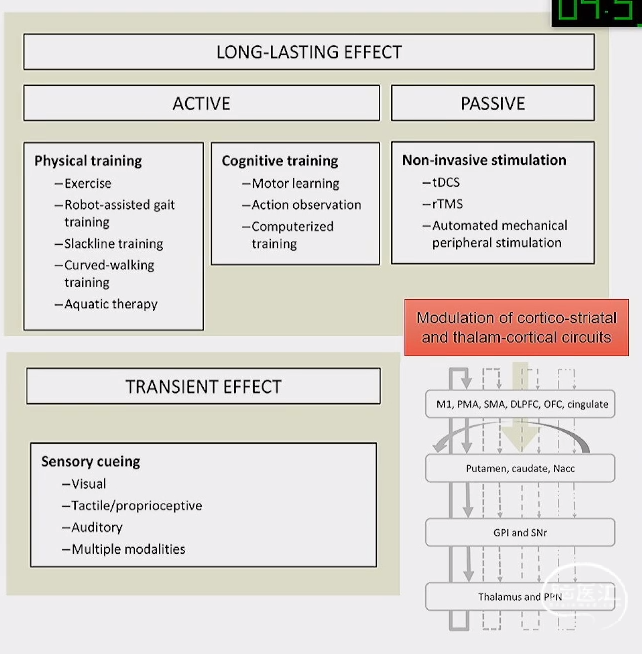
Movement Disorders 2019
感觉刺激/线索提示:
» 视觉刺激:在患者行走前方地面设置间隔小于平均步伐的平行线。
» 声音刺激:在患者行走起始和行进中,给予与行走步伐匹配的有节奏的声音提示。
» 振动觉刺激:在患者行走起始和行进中,给予下肢有节奏的振动提示。
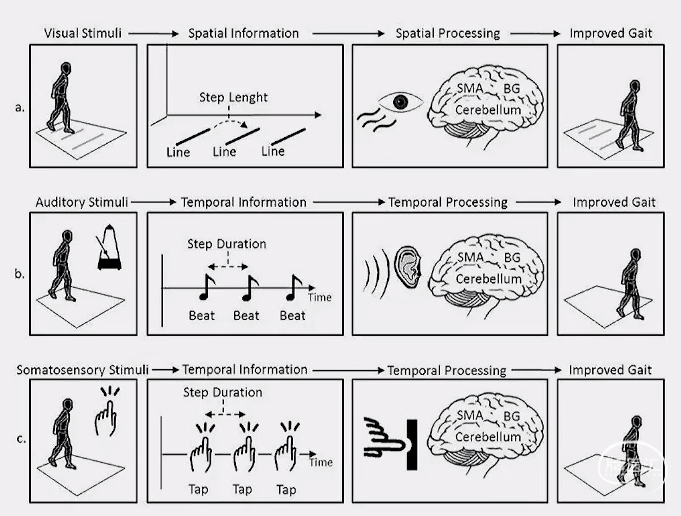
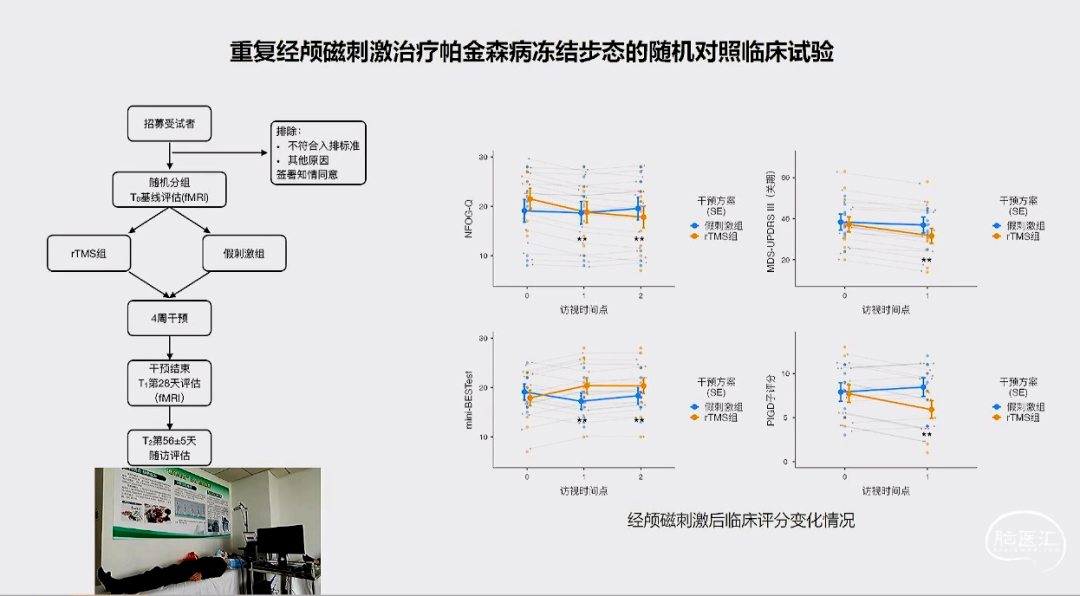
非药物非手术治疗:重复经颅磁刺激
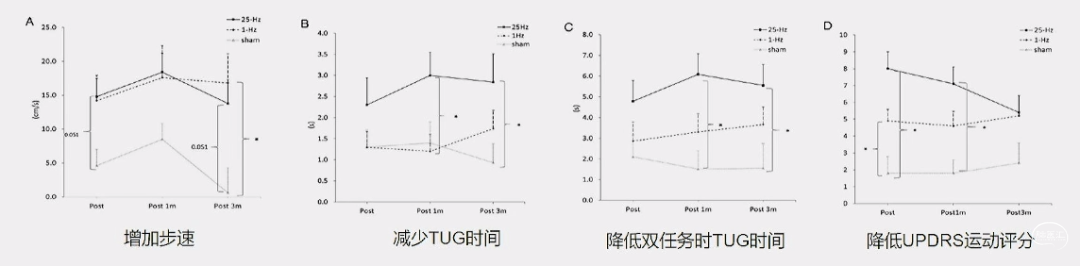
1Hz和25Hz rTMS辅助治疗可以使患者获益,运动症状改善可以持续到治疗后3个月。
与rTMS平衡皮层兴奋性和可塑性有关。
ANN NEUROL 2020;88:933-945

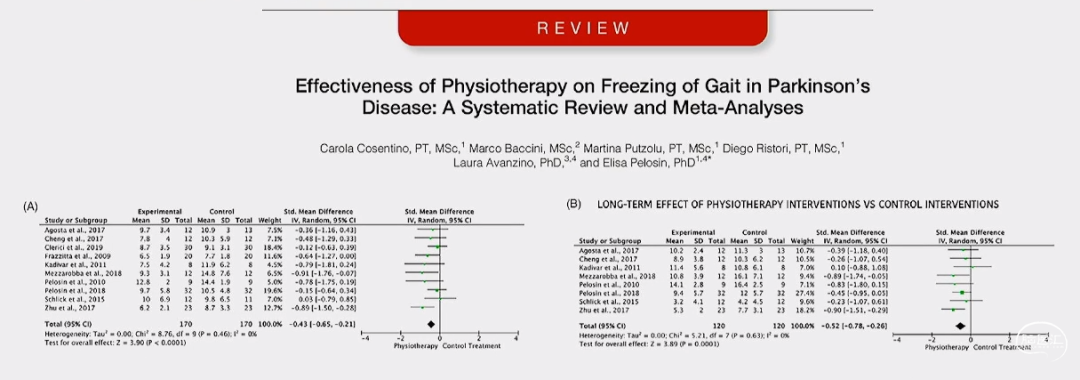
共纳入26篇,其中6篇研究TMS对于PD步态障碍患者的运动皮层反应性和可塑性,20篇评估rTMS治疗对PD患者步态功能改善情况。
结论:多次高频M1区,尤其是双侧M1区rTMS 可能改善PD步态障碍。

Neurophysiologie Clinique/Clinical Neurophysiology (2020)
非药物非手术治疗:运动和体育锻炼
运动锻炼可能改善PD-FOG,包括居家锻炼、跑步机锻炼可能有效降低“冻结”步态严重程度
Mov Disord.2020,35(4): 523-536
《帕金森病运动处方专家共识》
现代科技进展技术

讲者简介

干静 教授
上海交通大学医学院附属
新华医院神经内科
医学博士,硕士研究生导师。
上海交通大学医学院附属新华医院神经内科 副主任
现任上海市医学会神经内科第十届委员会青年委员;上海医学会神经病学分会帕金森病及运动障碍学组成员。
主持国家自然科学基金1项,上海市科委基金项目1项。
发表SCI论文十余篇;曾获2016年上海医学科技奖二等奖(第三完成人)、2020年上海市科技进步奖二等奖(第二完成人)等多个奖项

扫描二维码或
点击“阅读原文”
查看录播视频
![]()
声明:脑医汇旗下神外资讯、神介资讯、脑医咨询、神内资讯所发表内容之知识产权为脑医汇及主办方、原作者等相关权利人所有。未经许可,禁止进行转载、摘编、复制、裁切、录制等。经许可授权使用,亦须注明来源。欢迎转发、分享。



