原创首发于【神内资讯】微信公众号
本文带来中山大学孙逸仙纪念医院梁立阳教授在<第十七届南方神经外科论坛暨2023年广东省医学会神经肿瘤高峰会议•神经内分泌及重症分会场>分享的《下丘脑综合征的诊断和治疗》内容,欢迎大家阅读、分享。
NO.1
下丘脑解剖与生理功能
下丘脑(hypothalamus)
下丘脑(hypothalamus)位于大脑腹面、丘脑的下方,约重4g。
解剖位置:
丘脑前下方、垂体上方、视交叉后方
形成第三脑室的侧壁的底部和下壁
解剖标志:视交叉、灰结节、乳头体
-上界:下丘脑沟
-下界:灰结节-正中隆起,漏斗-垂体,乳头体
-前界:终板,视交叉
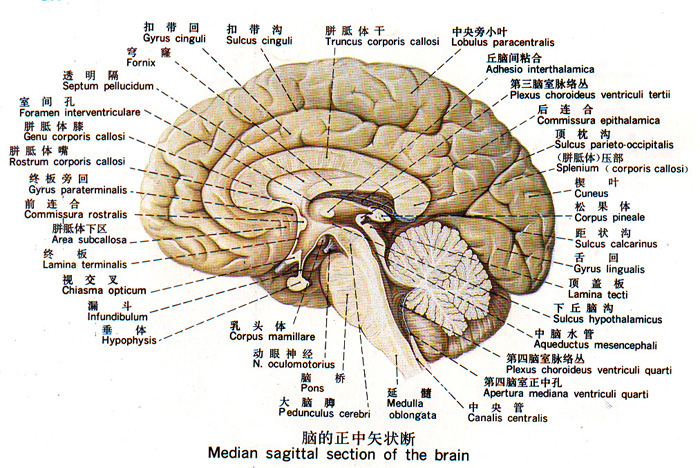
神经核团
内侧区(神经核团)
外侧区(纤维联系系统、外侧核团)
-视前区
-视上部:视上核、视交叉上核、室旁核 (PVN)
-结节部:腹内侧核(VMH)、背内侧核、弓状核(ARC)
-乳头部:后核、乳头状核
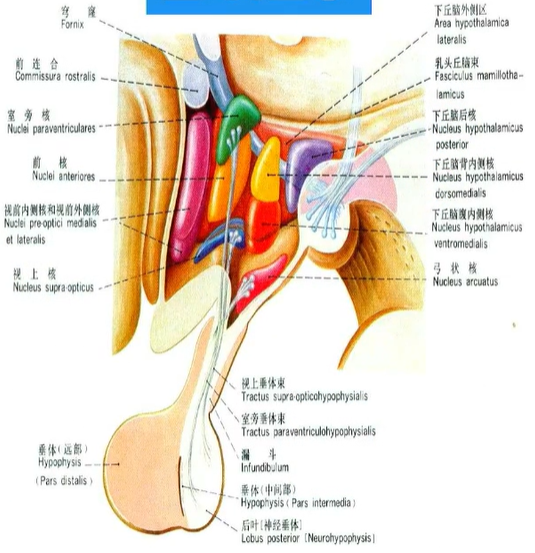
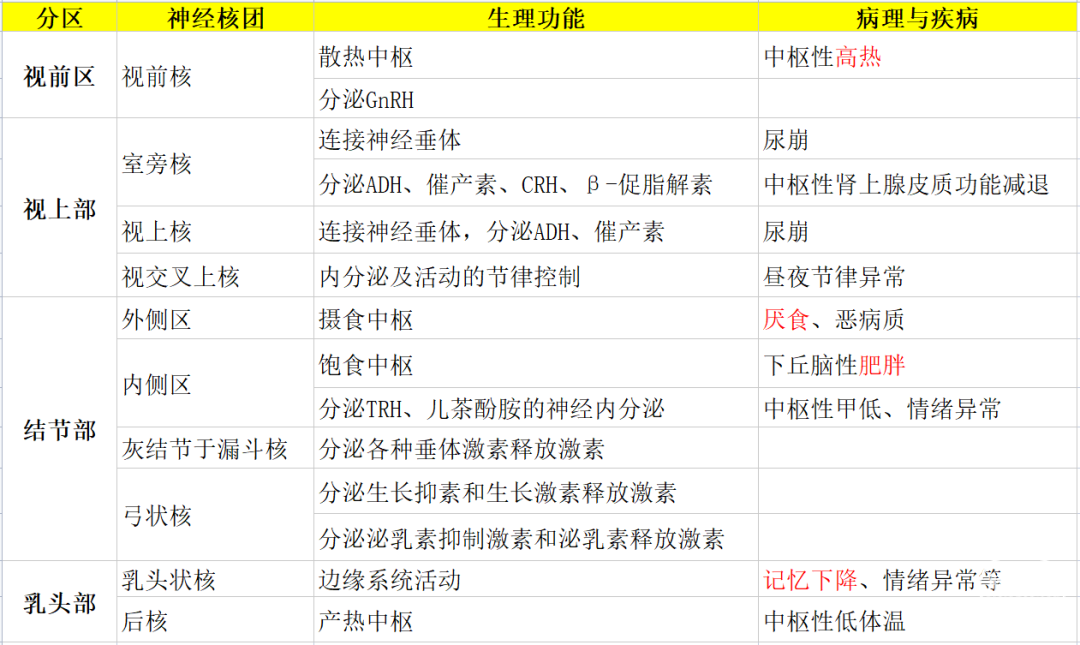
下丘脑的功能
调节体温;调节内分泌活动;调节摄食行为与消化道活动;控制情绪反应;调节水平衡;调节心血管活动;调节免疫反应;与生物节律的关系;与睡眠的关系;与性行为、生殖过程功能的关系
•与人体重要的内分泌、自主神经、基本生命活动三大方面密切相关
与垂体功能的关系
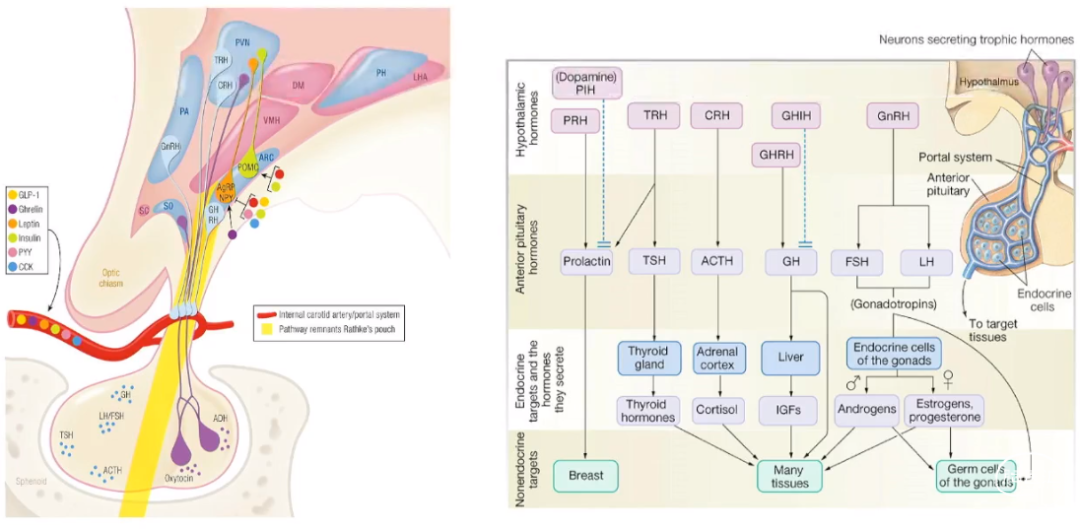
NO.2
下丘脑综合征病因
定义:
复杂的神经内分泌疾病;下丘脑功能紊乱;继发垂体及靶腺功能障碍;内分泌代谢障碍、
体温及睡眠等调节异常;自主神经功能紊乱等
病因:
先天性疾病;后天性疾病
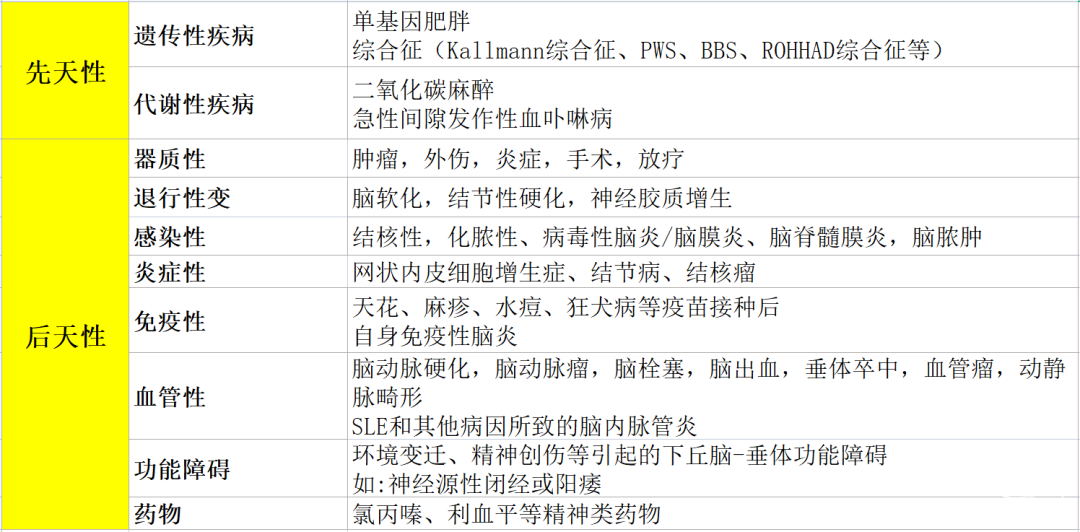
遗传性疾病
单基因肥胖是HO的一个亚组,在下丘脑表达,参与神经核团信号传导通路,通过控制人类摄食行为、能量消耗等方式调节体重。
罕见:瘦素缺乏(LEP)、瘦素受体缺乏(LEPR)
常见:MC4R(儿童早发性肥胖)
临床特征:严重早发肥胖;贪食;高胰岛素血症/胰岛素抵抗/糖耐量受损
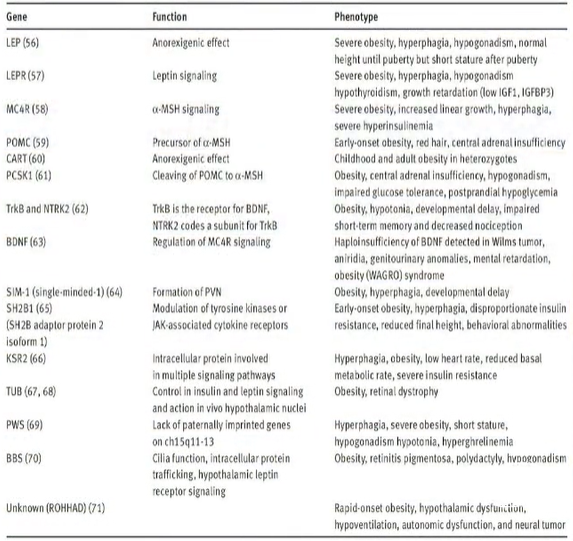
图:下丘脑肥胖的遗传原因及其临床特征
Prader-Willi综合征(PWS)
15q11-13上父源印记基因的缺失
胎儿期:IUGR、胎动少
新生儿期:SGA、肌张力低下、哭声弱、吮吸无力
婴儿期:喂养困难、全面发育迟缓、生长缓慢、体温调节障碍等
幼儿期及以后:食欲过剩、体重增长过速、严重肥胖、智力低下、情绪/行为异常等
高饥饿素血症、胃排空延迟、下丘脑视旁核缩小、分泌催产素细胞减少、瘦素及胰岛素相对于BMI正常
Bardet-Biedl综合征(BBS)
AR,21个BBS基因突变可致病,以纤毛病变为基础的疾病
BBS蛋白在纤毛功能和细胞内蛋白质运输中起作用,病变可累及多系统
BBS蛋白质是必需的瘦素受体成分,瘦素信号通路障碍可致肥胖
主要症状:视网膜变性、肥胖症、多指/趾畸形、性腺发育异常、智力发育迟缓、肾脏异常
次要症状:眼斜视/白内障/散光、短趾/并趾畸形、肝脏纤维化、糖尿病、神经功能损害、颅面部先天畸形、牙齿不规则、运动发育迟缓、高血压、心血管异常、听力损失及嗅觉异常等
诊断:符合4条主要症状或符合3条主要症状及2条次要症状则可临床诊断为BBS
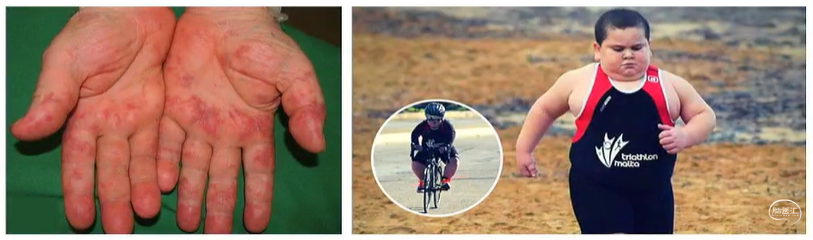
ROHHAD综合征
早发肥胖(RO):6-12个月即出现严重肥胖
下丘脑功能失调(H):水盐平衡失调、甲状腺功能减退症、性早熟、GHD、高泌乳素血症、肾上腺皮质功能低下
通气不足(H):体重增加和下丘脑功能障碍引起
自主神经失调(AD):体温调节障碍、心动过缓、多汗、瞳孔对光的反应改变、斜视、胃肠功能障碍、雷诺病等
精神/行为异常:癫痫、自闭、焦虑等
肿瘤高风险:神经嵴起源肿瘤高发风险,任何年龄段均可发病,遍布胸部、腹部及交感神经系统
目前,ROHHAD综合征的发病机制尚不明确,致病基因不确定,需对症治疗
器质性病变
下丘脑器质性病变最常见的病因:肿瘤、外伤、手术操作等
颅咽管瘤:术前35%;术后65%-80%,多于术后6-12个月发生
颅内肿瘤发生HO的高危因素:
发病年龄(年龄越小,发病率越高);肿瘤大小及范围(对下丘脑的损伤程度,尤其是乳头状核);初诊时是否存在内分泌功能障碍(尤其是尿崩);初诊时体重;肥胖家族史;肿瘤组织学(颅咽管瘤、视神经胶质瘤、生殖细胞瘤);下丘脑区域放疗(>51Gy);脑积水(需要放置侧脑室腹腔引流)
NO.3
下丘脑综合征临床特征
原发病相关表现
占位效应:视力视野受损;头痛、呕吐等颅高压表现
结构破坏:尿崩症
神经系统:脑膜刺激征、运动障碍
全身症状:发热;盗汗.....
内分泌异常
水盐平衡失调:尿崩症、抗利尿激素不适当分泌综合征
GHD或肢端肥大症
中枢性甲低或甲亢
肾上腺皮质功能低下或皮质醇增多症
性发育异常:低促性腺激素型性发育不良或性早熟
泌乳素分泌异常:溢乳或溢乳-闭经综合征、男子乳房发育
•高胰岛素血症:空腹及餐后胰岛素水平增高;副交感神经兴奋性增高;促进胰岛素分泌
aMSH信号通路受损;弓状核对胰岛素反应低下
•高瘦素血症:瘦素信号通路受损;瘦素水平增高;瘦素不敏感;高胰岛素血症促进脂肪细胞对葡萄糖摄取;刺激瘦素分泌
摄食障碍
贪食:腹内侧核或结节部病变
厌食:腹外侧核病变
ghrelin分泌减少导致食欲和饱腹感调节紊乱
瘦素信号通路障碍导致明显饥饿感
体重增长
下丘脑损伤后快速出现
6-12个月左右达顶峰
随后进入稳定阶段
能量摄入增加、消耗减少
能量消耗减少
体力活动量明显下降
基础代谢率降低
副交感神经系统兴奋性增高
昼夜节律紊乱、嗜睡、褪黑素减少等
中枢性甲低/GHD等
睡眠障碍
发作性睡病:不分时间和场地随时睡眠
深睡眠症:可持续数天至数周,可唤醒
睡眠颠倒:日间嗜睡、夜间兴奋
周期性嗜睡强食症
低通气(引起患者死亡的最主要原因)
呼吸中枢对高碳酸血症反应低下
中枢性睡眠呼吸暂停:基础
阻塞性睡眠呼吸暂停
二氧化碳潴留
夜间低通气
心血管系统异常
心律失常:阵发性室上性心动过速;窦性心动过速;心动过缓
血压异常:周期性低血压/阵发性高血压;间歇性发作的直立性低血压(鞍上-第三脑室)
体温调节障碍
中枢性高热;中枢性低热
自主神经功能紊乱
交感神经兴奋性下降-产热、能量消耗、脂肪动员降低
副交感神经兴奋性增高-刺激胰岛素分泌、降低能耗
泌汗障碍:周期性闭汗或多汗
胃肠动力障碍
边缘系统症状
乳头状核受损:记忆力下降(近事遗忘)
前部受损:躁狂症;行为、性格改变;情绪异常;间脑性癫痫发作
褪黑激素信号受损
视交叉上核受损,对光照感知障碍
褪黑素水平降低
垂体分泌激素昼夜节律紊乱
影响NPY、POMC、瘦素等的分泌,睡眠昼夜节律
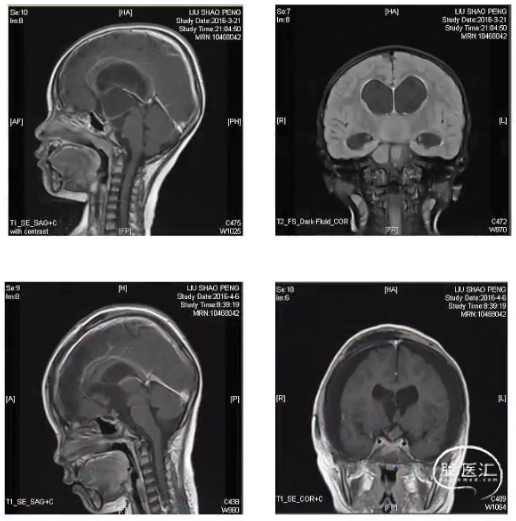
病例示例
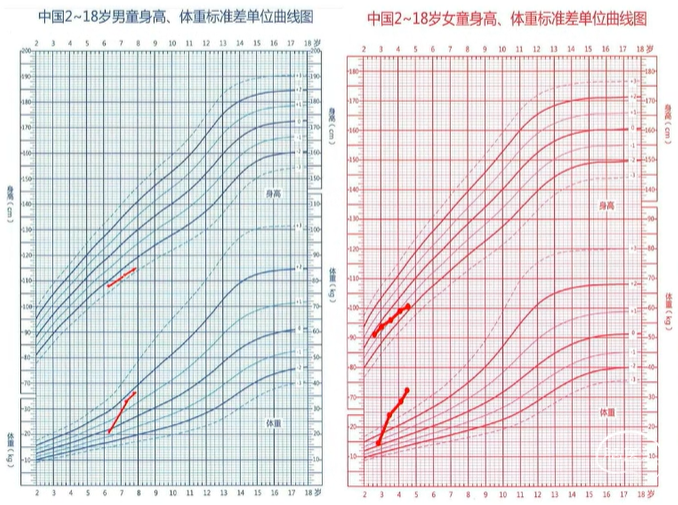
•女,4岁9月,因“体重增长过速、发热18月,气促、发绀10月”就诊
•3岁左右逐渐出现食欲亢进、多食、异常摄食,伴多饮多尿,饮水量/尿量约1600-2000 ml/d
•体重增长过速,约1kg/月,极低热卡饮食仍无改善

其他临床表现:
•反复发热,体温38℃-39.5℃,热型不定;不伴畏寒、寒战等,无感染症状
•抗感染治疗无效,退热药物效果不理想
•感觉异常:痛觉减退,自觉肛周皮肤瘙痒
•泌汗障碍:清醒状态下少汗或无汗,睡眠状态下多汗。与环境温度、发热与否无关
•心动过速:安静状态下心率:110-140次/分
•胃肠动力障碍:反复腹泻与便秘交替出现,予以益生菌等对症治疗不能改善
•昼夜节律紊乱:日间嗜睡(日间总睡眠6-8小时):夜间少睡、易醒(睡眠周期约0.5-1小时)
•情绪改变:易激惹,情绪波动大,低落时不言语,高涨时重复简单言语、无意义大笑
•行为改变:社交行为退缩,与人对视交流减少;有语言或行为攻击
•呼吸改变:呼吸浅、节律紊乱、发绀、活动耐力下降及睡眠呼吸暂停
血氧70%-90%;予以家庭无创呼吸机低-中流量吸氧,血氧饱和度可维持90%以上
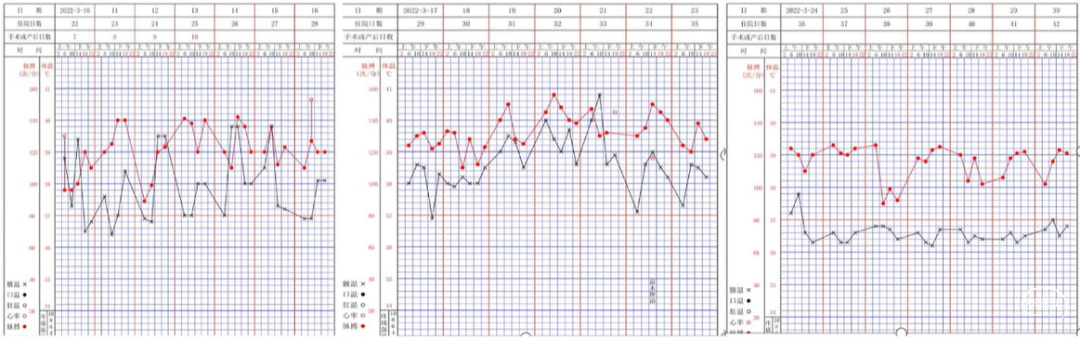
其他病史:
•既往史:“牛奶蛋白”过敏。
•个人史:G2P2,足月顺产出生,出生体重3.0kg,出生身长49cm,
•家族史:父亲肥胖(Ht:170cm,wt:105kg),祖母70岁时因“副神经节瘤”(神经嵴来源)去世
体格检查:
Wt:33.6kg(+6.98SD),Ht:100cm(-2.07SD),BMI 33.6kg/m2,腰围/身高:0.82
实验室检查:
常规:中度正细胞低色素性贫血
生化:高钠血症(147mmol/L-156mmol/L)与低钠血症(126mmol/L-137mmol/L)交替出现
代谢:糖脂代谢无异常
内分泌:IGF-1 34.6ng/ml(35-232ng/ml);FT4 9.42pmol/L(11.5-22.7),TSH 2.77mU/L;血尿皮质醇水平及节律正常;PRL波动于60.4-80.7ng/ml(4.8-23.3)
病例特点:
•异常摄食伴体重增长过速
•体温调节障碍、睡眠障碍、情绪行为异常、低通气等下丘脑功能障碍相关表现
•早发严重肥胖
•垂体多激素缺乏、高泌乳素血症、水盐平衡紊乱
NO.4
诊断、治疗及管理
诊断-思路
•缺乏统一诊断标准。根据病史、症状、体征、实验室检查综合判断
•以下情况需注意下丘脑综合征:
√内分泌紊乱症状及体征不能用单一的靶腺或单纯垂体损害加以解释
√内分泌紊乱症状伴有肥胖、多食、消瘦、厌食、嗜睡、精神失常及体温异常等,不能用其他疾病解释者
√颅内压增高伴视力或视野下降
√合并尿崩症、性功能低下、溢乳者
√少数患者可以表现为嗅觉消失、畸形、性腺发育不全
诊断-功能定位
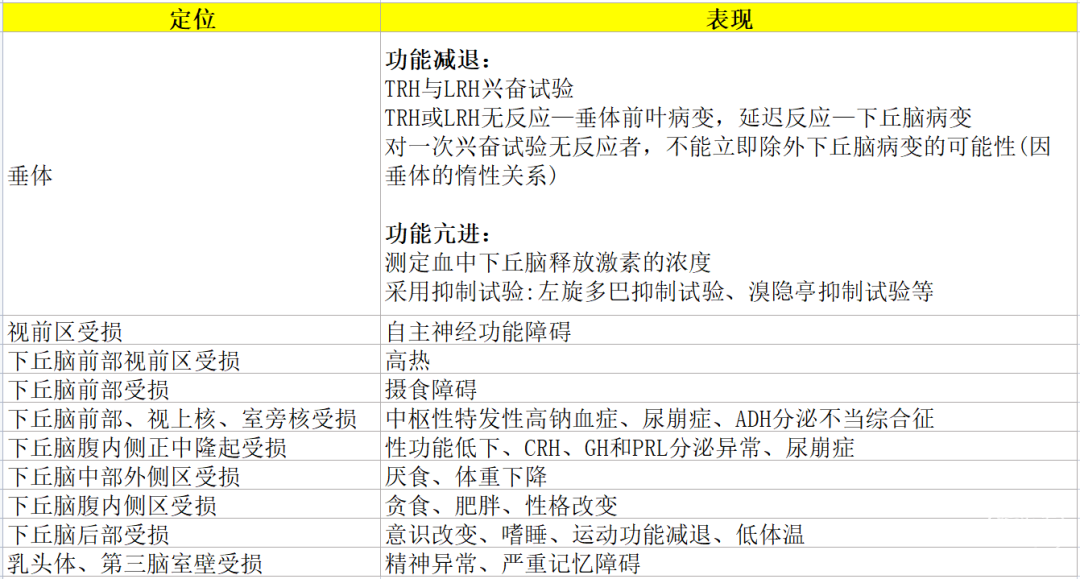
诊断-定性(病因)

诊断
ROHHAD综合征
1. 下丘脑性肥胖
2. 自主神经功能紊乱(体温调节中枢异常、情绪障碍、睡眠障碍、摄食和渴感中枢异常、胃肠功能障碍)
3. 阻塞性睡眠呼吸暂停低通气综合征
4. 认知功能障碍(认知倒退)
5. 中枢性甲状腺功能低下
6. 高泌乳素血症
7. 抗利尿激素不适当分泌综合征
治疗

相关文献研究
改善生活方式(综合干预)
•意大利,对13名平均年龄为12.2岁的下丘脑肥胖患儿,为期6个月的综合干预(饮食控制、体育锻炼、心理辅导),能有效控制HO患者的体重增长
*Tessaris D, Matarazzo P, Tuli G, Tuscano A, Rabbone I, Spinardi A, Lezo A, Fenocchio G, Buganza R, de Sanctis L. Multidisciplinary Approach for Hypothalamic Obesity in Children and Adolescents: A Preliminary Study. Children (Basel). 2021 Jun 22;8(7):531. doi: 10.3390/children8070531. PMID: 34206290; PMCID: PMC8304472.
•CCC(医疗、行为、饮食和运动支持和标准护理)模式能降低体重增长百分数、BM增长,改善HRQoL、身体机能、校园生活能力
综合干预是HO治疗的首先手段
*Haliloglu B, Bereket A. Hypothalamic obesity in children: pathophysiology to clinical management. J Pediatr Endocrinol Metab. 2015 May;28(5-6):503-13. doi: 10.1515/jpem-2014-0512. PMID: 25781673.
降低胰岛素分泌(二甲双胍)
二甲双胍能增加胰岛素敏感性,降低胰岛素抵抗
意大利,年龄>10岁,严重肥胖
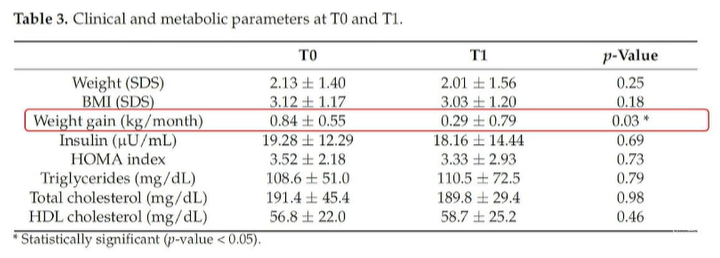
存在高胰岛素血症(Ins>30ml U/L)/胰岛素抵抗(HOMA-IR>4或综合干预6月但体重增长、HOMA-IR>3)的4名患者给予二甲双胍250mg.bid*10天后500mg.bid*6月治疗
对体重、BMI改善无明显作用,可部分改善体重增长和胰岛素抵抗(表4)
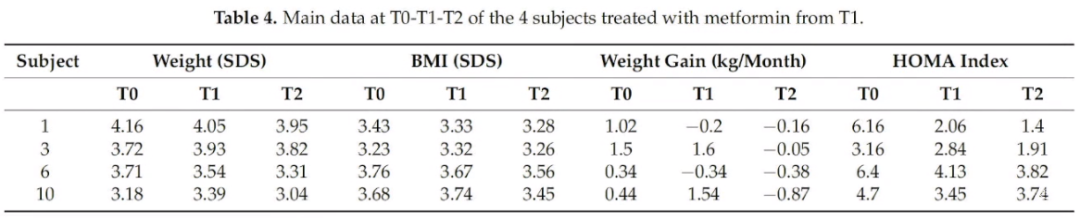
*Haliloglu B, Bereket A. Hypothalamic obesity in children: pathophysiology to clinical management. J Pediatr Endocrinol Metab. 2015 May;28(5-6):503-13. doi: 10.1515/jpem-2014-0512. PMID: 25781673.
降低胰岛素分泌(二甲双胍+二氮嗪)
二氮嗪与胰岛β细胞的KATP通道结合,降低胰岛素分泌;可改善HO患者的高胰岛素血症对颅咽管瘤术后合并HO的患者使用二氮嗪和二甲双胍联合治疗6月
7名患者体重增长减慢、BMI-SDS降低
副作用:水钠潴留、充血性心力衰竭、腹胀等
*Hamilton JK, Conwell LS, Syme C, Ahmet A, Jeffery A, Daneman D. Hypothalamic Obesity following Craniopharyngioma Surgery: Results of a Pilot Trial of Combined Diazoxide and Metformin Therapy. Int J Pediatr Endocrinol. 2011;2011(1):417949. doi: 10.1155/2011/417949. Epub 2011 Mar 22. PMID: 21603206; PMCID: PMC3198743.
生长抑素
与特异G蛋白介导的膜受体结合,抑制胃酸、胰酶、胰高血糖素和胰岛素的分泌;并且减少内脏血流量,降低胃肠道运动
8例HO患者皮下注射奥曲肽后,体重较6个月前的观察阶段显著下降
60例双盲/安慰剂对照试验中,治疗组仅表现为体重稳定及胰岛素、瘦素水平下降
*Lustig RH, Hinds PS, Ringwald-Smith K, Christensen RK, Kaste SC, Schreiber RE, Rai SN, Lensing SY, Wu S, Xiong X. Octreotide therapy of pediatric hypothalamic obesity: a double-blind, placebo-controlled trial. J Clin Endocrinol Metab. 2003 Jun;88(6):2586-92. doi: 10.1210/jc.2002-030003. PMID: 12788859.
拟交感活性药物
HO患者交感神经—肾上腺素活性受损,活力/运动力下降,能量消耗减少
拟交感活性药物可提高患者运动能力、增加能量消耗
对5名颅咽管瘤术后合并HO患者使用2年的安非他明治疗
患者体重持续下降、BMI稳定、活动耐力提高:但患者摄食行为无改善
*Mason PW, Krawiecki N, Meacham LR. The use of dextroamphetamine to treat obesity and hyperphagia in children treated for craniopharyngioma. Arch Pediatr Adolesc Med. 2002 Sep;156(9):887-92. doi: 10.1001/archpedi.156.9.887. PMID: 12197795.
增加能量消耗
HO患者交感神经系统激活减少,且可能合并中枢性甲低;导致基础代谢率降低,能量消耗减少
左旋甲状腺素可能有助于减轻体重
3名HO患者使用左旋甲状腺素治疗后出现体重下降
*Fernandes JK, Klein MJ, Ater JL, Kuttesch JF, Vassilopoulou-Sellin R. Triiodothyronine supplementation for hypothalamic obesity. Metabolism. 2002 Nov;51(11):1381-3. doi: 10.1053/meta.2002.35591. PMID: 12404183.
抑制食欲
•胰高血糖素样多肽-1(GLP—1)
通过迷走传入神经将饱感信号传递至中枢,或直接作用于下丘脑、脑干等的受体,抑制食欲8名HO成年患者使用GLP-1(利拉鲁肽/艾塞那肽),体重减少13.1±5.1kg,改善胰岛素抵抗副作用:恶心、腹泻非常常见,呕吐、腹痛、便秘常见,低血糖常见
*Zoicas F, Droste M, Mayr B, Buchfelder M, Schöfl C. GLP-1 analogues as a new treatment option for hypothalamic obesity in adults: report of nine cases. Eur J Endocrinol. 2013 Apr 15;168(5):699-706. doi: 10.1530/EJE-12-0997. PMID: 23392214.
•5羟色胺或去甲肾上腺素再摄取抑制剂
增加去甲肾上腺素、多巴胺等神经递质水平,从而抑制食欲、减轻体重
HO患者使用西布曲明治疗后体重减轻,但效果低于其他肥胖儿童
副作用:心血管事件高风险
*Danielsson P, Janson A, Norgren S, Marcus C. Impact sibutramine therapy in children with hypothalamic obesity or obesity with aggravating syndromes. J Clin Endocrinol Metab. 2007 Nov;92(11):4101-6. doi: 10.1210/jc.2007-0826. Epub 2007 Aug 28. PMID: 17726084.
减重手术
可调节胃束带(LAGB):能迅速控制食欲,对体重增长及BMI无改善
袖状胃切除术/胃旁路术/胆胰分流术:术后1年体重下降20%;能有效控制体重及BMI增长
出于伦理等方面考虑,减重手术用于治疗HO存在争议
对于年龄<16岁,须经营养科及发育儿科等MDT讨论,综合评估可行性及风险,充分告知及知情同意后谨慎开展,不建议广泛推广
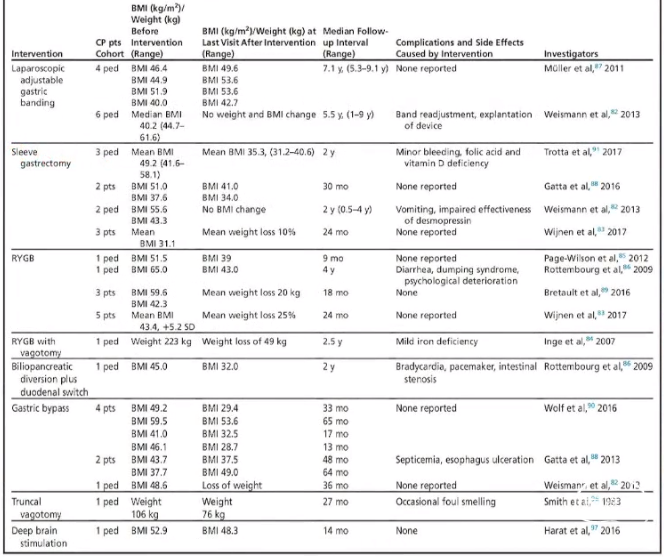
图:下丘脑肥胖的手术干预治疗
*Müller HL. Management of Hypothalamic Obesity. Endocrinol Metab Clin North Am. 2020 Sep;49(3):533-552. doi: 10.1016/j.ecl.2020.05.009. Epub 2020 Jul 15. PMID: 32741487.
下丘脑肥胖症的未来疗法
•催产素:催产素替代物可能会刺激通过下丘脑损伤下调的厌食途径,并可能在上调涉及能量消耗的途径中发挥作用。
•蛋氨酸氨基肽酶抑制剂(MetAP2):用于通过防止肿瘤增殖来治疗癌症。也导致体重减轻,增加脂联素和减少瘦素,脂肪生成减少、脂肪氧化增加和脂肪分解增加
•替索美特(替索芬辛和美托洛尔)
•选择性MC4受体激动剂:刺激PVN和LH中的MC4受体以激活厌食途径,在Bardet-Bield综合征患者中的结果令人鼓舞
下丘脑睡眠障碍的治疗
•昼夜节律是由一个复杂的器官时钟网络产生的,下丘脑的视交叉上核是主要的调节器
•白天过度嗜睡、睡眠呼吸障碍和昼夜节律调节紊乱
•睡眠障碍需要采用多模式方法:褪黑激素;兴奋剂疗法在减少嗜睡和治疗继发性发作性睡病方面具有积极作用;合并OSAS的夜间通气
低通气伴呼吸控制中枢的改变
(管理:人工通气和客观监测)
•睡眠与清醒时呼吸浅
•进行性高碳酸血症和低氧血症但无法刺激呼吸或唤醒
•感受不到气短
•能够有意识地改变呼吸的频率和深度
讲者简介
梁立阳 主任医师
中山大学孙逸仙纪念医院
• 儿科副主任,儿科神经内分泌专科主任;
• 中华医学会儿科学分会内分泌及遗传代谢病学组委员,华南协作组副组长;
• 中国医师协会青春期医学会社会工作组副组长;
• 中国出生缺陷救治基金会儿童内分泌及遗传代谢委员会委员;
• 广东省医学会儿科分会内分泌及遗传代谢病学组副组长;
• 广东省女医师协会女性内分泌专业委员会常委;
• 广东优生优育委员会地中海贫血委员会委员;
• 中山大学孙逸仙纪念医院儿科副主任;
• 中山大学中山医学院组胚教研室临床副主任。
• 长期从事儿童内分泌及遗传代谢性疾病的基础研究和临床工作。擅长儿童及青少年生长迟缓、性早熟、肥胖、性发育异常、糖尿病、甲状腺疾病、垂体功能障碍及罕见遗传代谢病等的临床诊治。在儿童生长发育及内分泌领域国内外核心期刊以第一作者和通讯作者发表专业论文或参编专著、科普书籍数十篇。主持和参与多项基金及临床科研课题。
扫描二维码或
点击“阅读原文”
查看录播视频
![]()
声明:脑医汇旗下神外资讯、神介资讯、脑医咨询、神内资讯所发表内容之知识产权为脑医汇及主办方、原作者等相关权利人所有。未经许可,禁止进行转载、摘编、复制、裁切、录制等。经许可授权使用,亦须注明来源。欢迎转发、分享。








