第一作者:葛红飞,周腾渊,张超
通讯作者:冯华,胡荣
作者单位:重庆西南医院神经外科


1
神经干细胞表达ASIC1a
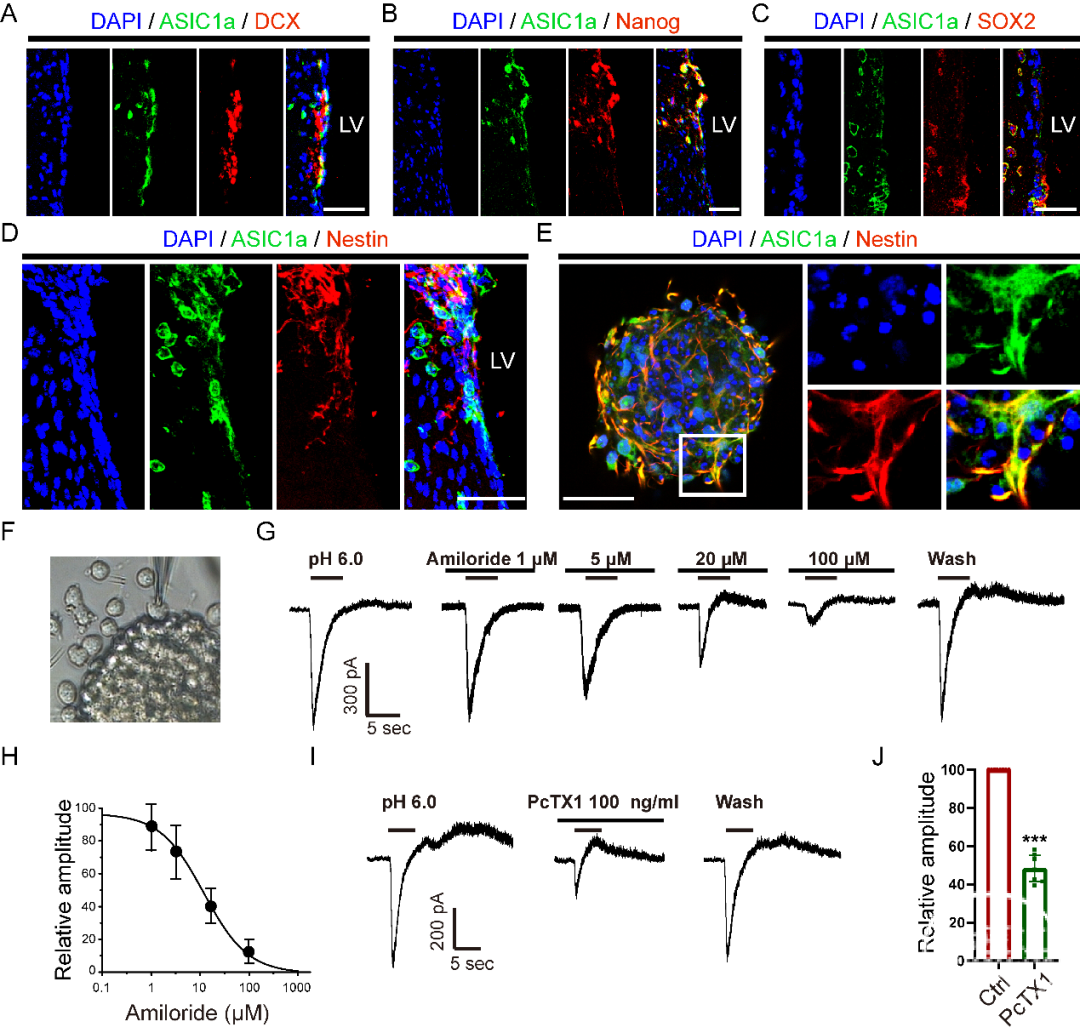
鉴于ASIC可被细胞外酸化微环境激活并能发挥生物学效应,但NPCs是否表达酸敏感通道,既往未见文献报道。为了确定ASIC1a是否在侧脑室周围的NPC中表达,使用不同的NPC标记物和ASIC1a进行了免疫荧光染色。结果显示ASIC1a与Doublecortin(DCX)(图1A)、Nanog(图1B)、SOX2(图1C)和Nestin(图1D)共标,表明ASIC1a在成年小鼠脑中的侧脑室周围NPCs中表达。此外,体外实验显示ASIC1a与从SVZ来源的Nestin+细胞共标记(图1E)。总的来说,这些发现表明ASIC1a在NPCs中表达。进一步,通过体外培养的NPCs,利用膜片钳技术,验证了其电生理特性,酸化诱导的电流能被非特异性ASICs通道阻断剂阿米洛利(amiloride)和同聚体ASIC1a及异聚体ASIC1a/2b的特异性阻断剂PcTx1所阻断(图3F)。上述结果表明ASIC1a在NPCs中表达,并具有离子通道功能。
2
细胞外环境酸化可明显抑制NPCs迁移和神经发生
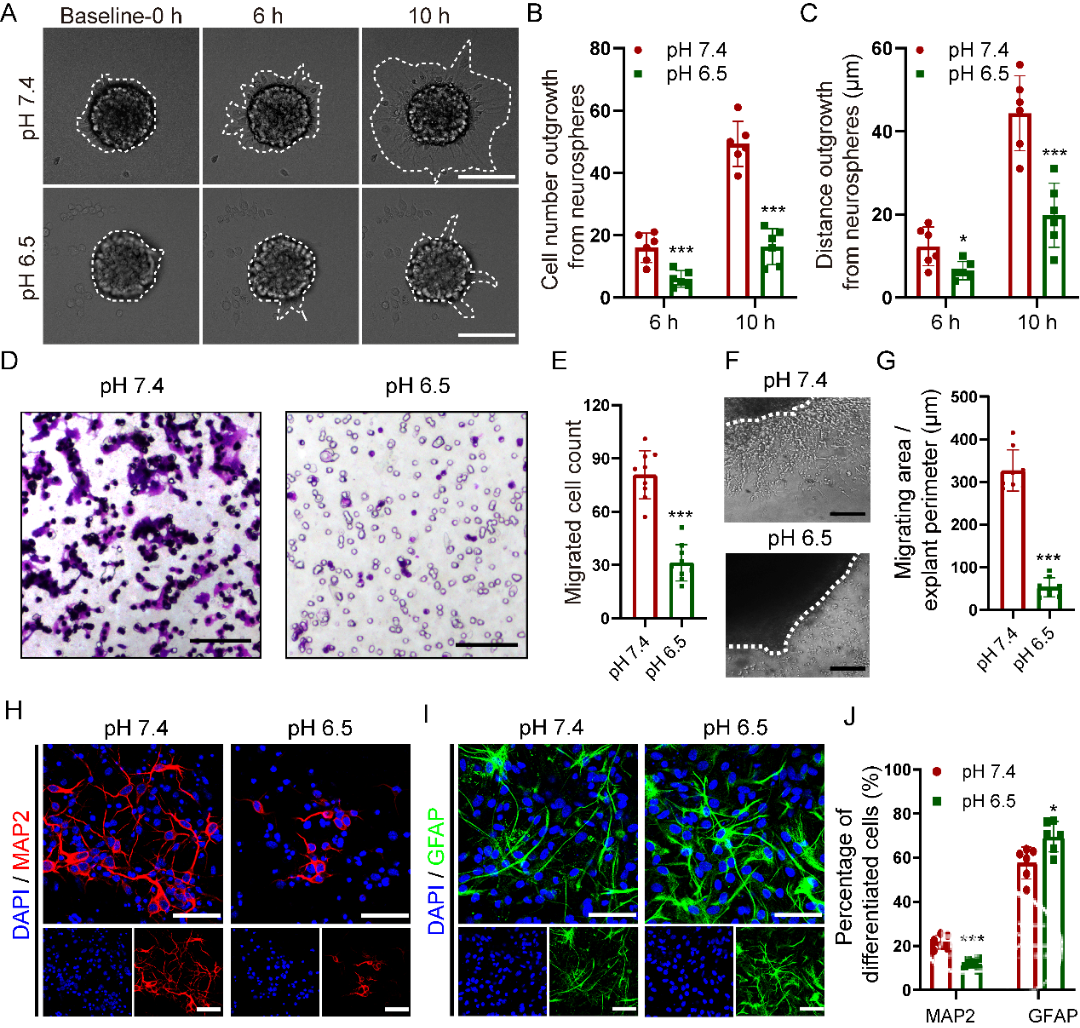
为进一步研究细胞外环境酸化对NPCs迁移的影响。首先,课题组将NPCs球接种于多聚鸟氨酸预先包被过的24孔细胞培养板中,利用活细胞工作站实时观察了细胞在不同pH培养液中,干细胞球向外迁移的细胞数量和迁移距离。实验结果表明:与pH7.4相比,在pH 6.5的情况下,NPCs自干细胞球向外迁移的数量及距离明显减少,且表现出酸度依赖性,酸度越低,抑制作用越强(图 2A-C)。其次,利用Transwell实验设置,观察了细胞自Transwell上层小室向下室迁移的细胞数目。结果表明:NPCs自上室迁移至下室的细胞数目在pH 6.5的情况下明显减少,且呈酸度依赖性(图 2D, E)。此外,作者在体外培养了SVZ组织块,模拟在体条件下观察细胞迁移能力。结果表明:随组织块外环境酸化程度加重,组织块细胞向外迁移的表面积较pH 7.4明显减少(图 2F, G)。以上数据表明:细胞外环境酸化可明显抑制NPCs的迁移能力,并且呈现出酸度依赖性,随酸度下降抑制作用增强。最后,用免疫荧光染色研究酸性条件对NPCs分化的影响。结果表明,与pH 7.4相比,pH 6.5时来自NPCs的MAP2+细胞百分比明显降低,而GFAP+细胞在pH 6.5时的比例明显升高(图2H-J)。综上所述,这些数据表明,细胞外酸中毒激活ASIC1a会损害NPCs迁移和分化为神经元,从而抑制神经发生。
3
微环境酸化通过激活ASIC1a抑制神经干细胞迁移和神经发生

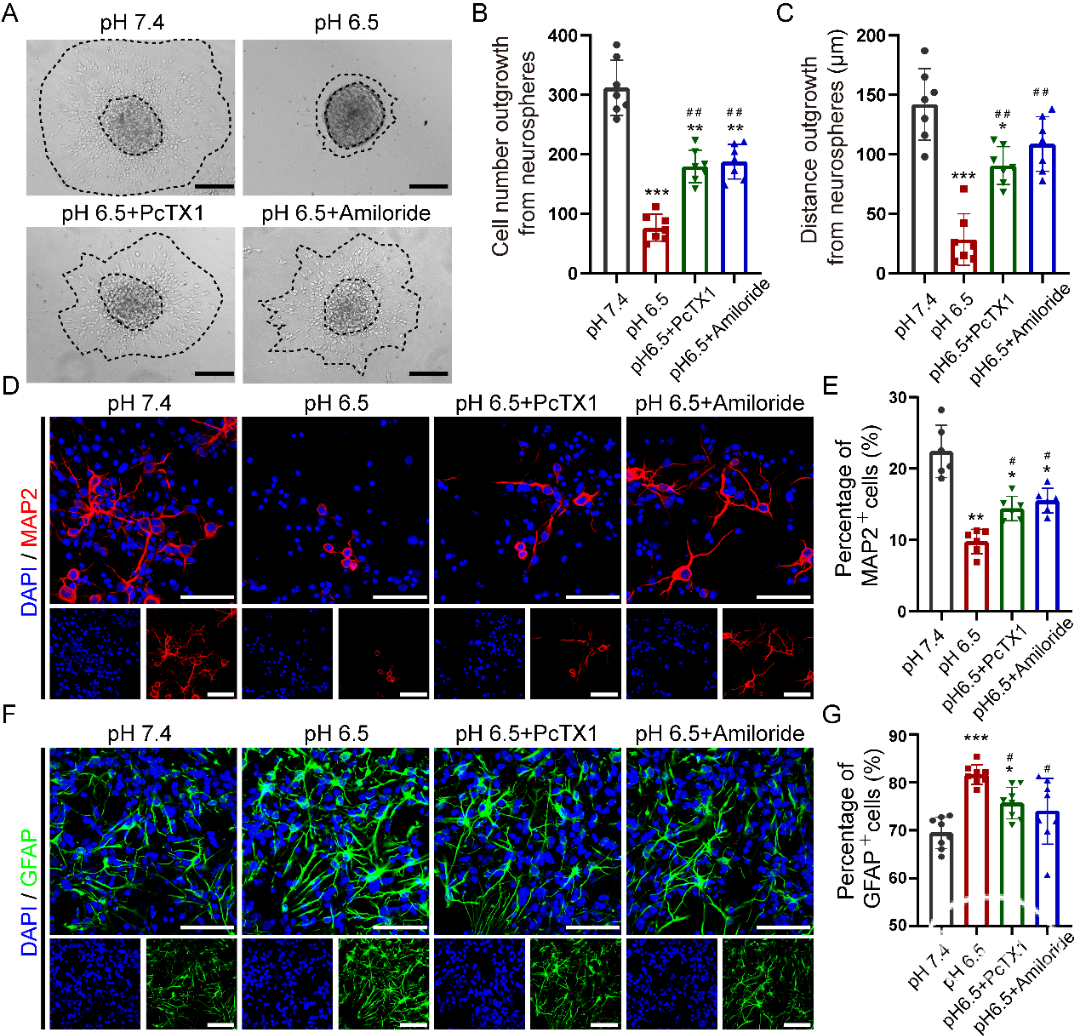
图3. 酸化通过激活 ASIC1a 抑制神经干细胞迁移和向神经元分化
4
ASIC1a阻断剂可以促进NPCs迁移和神经发生
上述结果提示:敲除ASIC1a促进NPCs迁移并向神经元分化。为研究ASICs阻断剂阿米洛利和PcTX1是否可发挥相似作用,用阿米洛利(20μM)或PcTX1(100ng/mL)处理NPCs。结果表明,与pH 7.4相比,pH 6.5时用阿米洛利或PcTX1处理NPCs,酸对NPC的迁移抑制作用显著改善,从细胞球中迁移出的细胞数量和迁移的距离明显增加(图4A-C)。而且,在pH6.5环境下,阿米洛利及PcTX1促进NPCs向神经元(MAP2+)分化,抑制向星形胶质细胞(GFAP+)分化(图4D-G)。总的来说,这些结果表明ASIC1a的阻断剂可以促进NPCs在酸性条件下迁移和神经发生。
5
ASIC1a阻断剂或ASIC1a敲除可以促进脑卒中小鼠的神经功能恢复
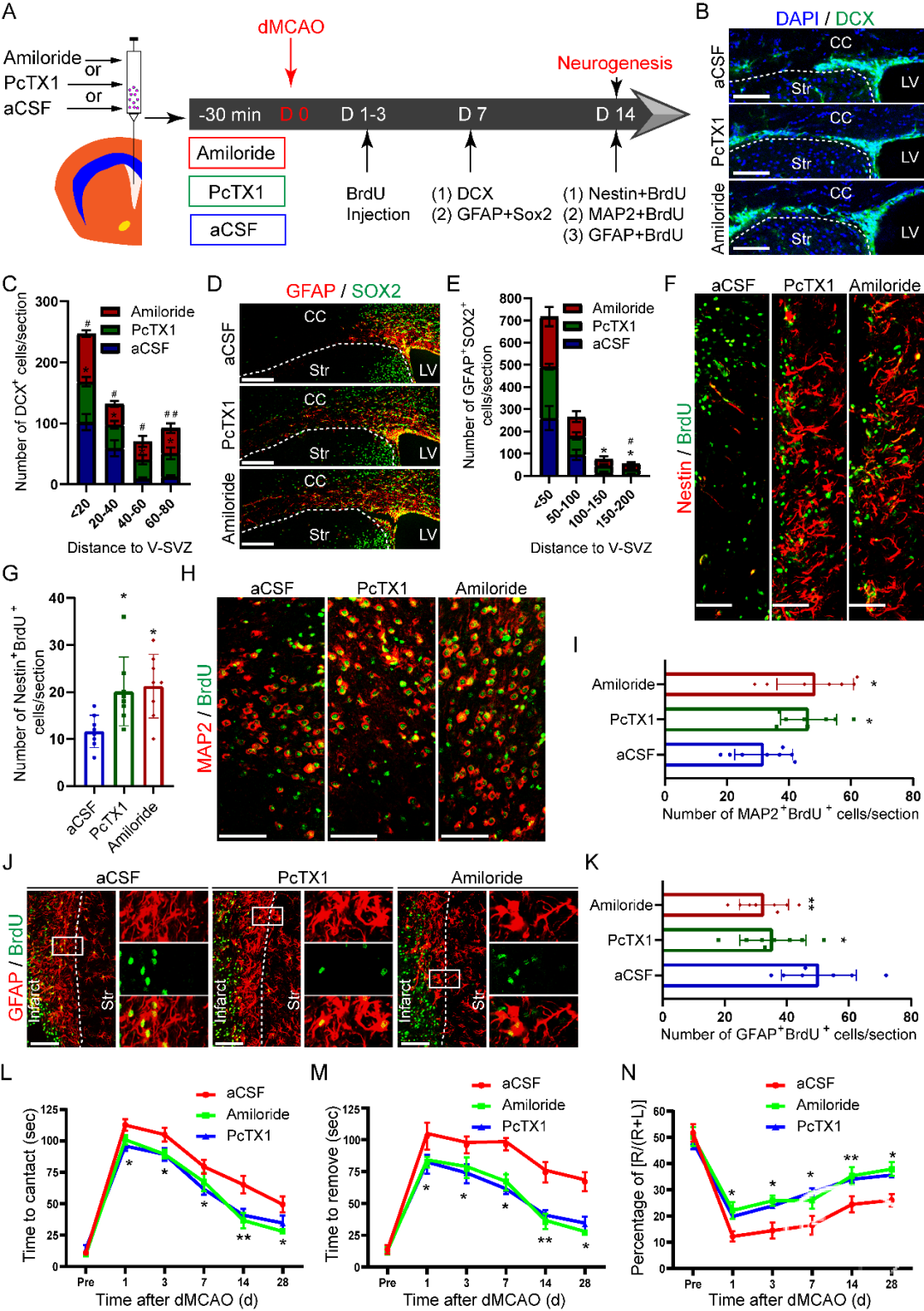
为进一步评估干预ASIC1a对脑梗模型小鼠脑内NPCs迁移和神经发生的影响,一方面采用药理学阻断策略,野生小鼠在dMCAO前30 min脑室内分别注射2 μL人工脑脊液(aCSF)、含aCSF的阿米洛利和PcTX1(图5A-C)。研究发现,在阿米洛利或PcTX1处理的小鼠中,DCX+细胞的数量在缺血半暗带中明显增加。此外,用阿米洛利或PcTX1处理的小鼠GFAP+SOX2+细胞的数量在半暗带中显著增加(图5D和5E)。然后,对侧脑室和沿吻侧迁移流的NPCs进行BrdU免疫染色,检测ASIC1a阻断剂对NPCs迁移的影响。在脑梗造模后第14天,脑室内注射ASIC1a阻断剂可明显增加BrdU+Nestin+细胞的数量(图5F和5G)。这些结果表明ASIC1a阻断剂可以促进了NPCs从脑室下区迁移到缺血半暗带。同时,脑室内注射ASIC1a阻断剂增加了损伤区域周围BrdU+ MAP2+细胞的数量(图5H和5I),而减少了半暗带BrdU+ GFAP+的数量(图5J和5K)。最后进行行为学实验,探索予阿米洛利或PcTX1是否促进小鼠dMCAO后行为恢复(图5L-N)。结果显示,接受ASIC1a阻断剂治疗的小鼠比未接受治疗的小鼠呈现更好的行为恢复。另一方面,采用ASIC1a基因敲除动物建立脑梗死模型,与野生鼠相比,ASIC1a-/-鼠DCX+细胞的数量在缺血半暗带中明显增加,损伤区域周围BrdU+ MAP2+细胞的数量增多,而BrdU+ GFAP+的细胞数量下降,更重要的是行为学实验显示基因敲除鼠的神经功能比野生鼠恢复更明显。以上结果说明靶向ASIC1a干预策略可以促进缺血性脑卒中模型小鼠NPCs的迁移和缺血半暗带神经发生,进而促进其神经功能恢复。
通讯作者简介
冯华 教授
重庆西南医院
教授,主任医师,博导
重庆西南医院神经外科学术带头人,全军神经外科研究所所长,国家973计划项目首席科学家,第十一届中国医师奖获得者,重庆市首批学术学科领军人才,重庆市首席医学专家,重庆英才名家名师
兼任中华医学会神经外科分会常委,中华医学会创伤分会常委,中国医师协会神经外科医师分会常委,中国医师协会神经修复学专业委员会副主任委员兼总干事,重庆市医学会常务理事
主要从事:1.出血性脑卒中防治研究;2.神经系统创伤的救治与神经功能重建;3.脑功能精准定位下脑肿瘤微创切除与光动力诊疗;4.前沿技术在脑科学的转化
先后主持国家973计划项目、国家自然科学基金国际合作项目、国家自然科学基金重点项目、重庆市攻关工程项目等各级科研项目50余项,科研经费10660余万元
获批发明专利26件,其中国际PCT专利8件;主编(译)专著11部,其中英文专著4部
发表SCI论文226篇(IF>10.0的16篇,IF>5.0的87篇),他引5181次
获国家科技进步二等奖1项,省部级一等奖7项
点击二维码,前往冯华 教授学术主页
查看更多精彩内容
胡荣 教授
重庆西南医院
教授、主任医师、博士生导师
重庆西南医院神经外科(国家重点学科、国家临床重点专科、重庆市神经外科临床研究中心)主任
国家重点研发计划项目首席专家、重庆市杰出青年、重庆英才•创新领军人才、高校创新研究群体负责人
兼任重庆市医学会卒中分会主任委员、中国医师协会神经修复学专业委员会委员、中华医学会神经外科学分会颅脑创伤专家委员会委员等
临床主要从事:1.神经内镜经鼻和经颅微创切除颅底肿瘤;2.脑出血精准诊疗与修复;3.多模态导航与术中唤醒下脑深部肿瘤精准切除
主要研究方向:1.脑卒中后神经损伤与修复;2.微环境与干细胞命运决定;3.脑出血诊治的多中心临床研究
主持国家重点研发计划项目、国家973计划项目子课题、国家自然科学基金项目等各级科研项目28项,牵头国内多中心临床研究1项,参与国际多中心临床研究1项
获批专利12项(其中PCT专利2项,发明专利7项);获“中国医师协会神经外科分会全国手术大赛一等奖”、“王忠诚中国神经外科优秀青年医师奖”、“踏血无痕脑肿瘤显微手术大赛第二名” 和“全军神外手术大赛银奖”
点击二维码,前往胡荣 教授学术主页
查看更多精彩内容
(一)科研PI岗位
(二)科研助理岗位
福利待遇:
1.年薪30万元-100万元(年薪面议);
2.在享受同级别聘用人员薪酬待遇基础上,具博士学位人员在引进的前三年,每月享受5000元博士津贴,三年后根据考核情况纳入医院优秀人才培养计划;
3.租房补贴:被医院认定为PI(含青年PI)的人员,按照当地房租水平享受2000元-4000元/月的租房补贴;
4.岗位配套:科研PI配套不少于4人的科研助理编制,青年PI配套1-3人的科研助理编制;
5.培养机制:按照医院人才培养机制开展个性化培养,畅通职业发展路径;优先纳入医院“百名学术英才”培养计划(另有人才津贴及本人、配偶、子女医疗福利),在出国深造、课题申请、职称晋升、人才项目推荐等方面重点扶持;
6.子女保障:子女就读排名重庆第一、全国前列的幼儿园;
7.其他保障:按有关规定享受健康查体、探亲休假、因私出国、交通补助等福利。
声明:脑医汇旗下神外资讯、神介资讯、神内资讯、脑医咨询、AiBrain 所发表内容之知识产权为脑医汇及主办方、原作者等相关权利人所有。












