

在科学描述之前,法国雕塑家Daumier (1808–1879) 在他的雕塑作品中描绘了颈面部肌张力障碍。
1887年,美国神经学家Horatio Wood首次描述颅颈肌张力障碍。1910年,法国神经学家Henri Meige描述的一组锥体外系疾患,第一次提出Meige综合征,迄今已有百余年的历史。梅杰综合征也叫颅颈肌张力障碍,因为按照国际惯例,梅杰综合征仅仅指代为病因不清的眼睑痉挛合并口下颌肌张力障碍,可伴有面部、咽部、舌部等受累,并以“颅段肌张力障碍”的名称取代“梅杰综合征”。
梅杰综合征根据发病和累及部位不同可以分为眼睑痉挛型、眼睑痉挛合并口下颌肌张力障碍型、口下颌肌张力障碍型和其他发病类型。主要表现为双眼睑痉挛、口下颌肌张力障碍面部肌张力失调样不自主运动。
1、眼睑痉挛型:表现为眼睑阵发性不自主痉挛或强直性收缩或不自主眨眼。约25%患者以单侧眼睑痉挛起病,逐渐发展为双侧3
2、眼睑痉挛合并口下颌肌张力障碍型:在表现眼睑痉挛的同时,口唇及颌面部肌肉亦呈痉挛性收缩,表现噘嘴、缩唇、张口、伸舌、嘴角及面肌不自主抽动,患者呈怪异表情
3、口下颌肌张力障碍型:仅有口唇及颌部肌肉痉挛性抽动
4、其他发病类型:在上述3个类型的基础上合并颈、躯干、肢体肌张力障碍
近年来,梅杰综合征患病人数呈明显上升趋势。遗憾的是梅杰综合征起因和发病机制目前尚不清楚。可能的因素认为心理因素、药物因素、创伤及口腔操作或手术等因素导致的脑内神经介质,尤其体内乙酰胆碱及多巴胺的平衡失调,可能与本病的发生有关。


梅杰综合征的治疗方法有药物治疗、肉毒毒素注射治疗和手术治疗。全身型肌张力障碍首选口服药物治疗,但是对于大多数局灶型和节段型肌张力障碍,口服药物疗效欠佳,可首选肉毒毒素注射。口服药和肉毒毒素治疗效果欠佳的遗传性或特发性单纯型累及节段和颈部的肌张力障碍适合脑深部电刺激DBS手术,其他局灶型肌张力障碍也可试用DBS。
2003年,美国FDA批准(人道主义器械豁免)美敦力DBS用于肌张力障碍的治疗,2016年获中国NMPA批准。这也是目前唯一获批用于肌张力障碍治疗的微创外科疗法,目前美敦力DBS可用于治疗7岁及以上的原发性肌张力障碍患者,是肌张力障碍的有效治疗方式。欧洲神经病学EFNS指南、运动障碍协会MDS指南、中国肌张力障碍诊断与治疗指南、肌张力障碍治疗专家共识均对DBS治疗梅杰综合征进行了推荐。


PubMed, Web of Science and Embase 三个电子数据库的23篇符合条件的文章,115位患者,94位Gpi-DBS,21位STN-DBS。结果显示,
• Gpi-DBS 治疗梅杰患者,其运动症状得到明显改善;
• BFDRS-M的改善只与术前的基础评分有关;
• Gpi-DBS可通过症状减轻,提升患者的生活质量;
• 相比于STN, Gpi是治疗Meige患者效果更好;
• 平均BFMDRS-M:21.5 ± 11.0 vs 8.6 ± 6.9, P < 0.001
• 平均BFMDRS-D:6.4 ± 5.1 vs 2.9 ± 2.4, P < 0.001)
• 平均随访时间:31.9 ± 30.7 个月
• Gpi组BFMDRS-M:23.1 ± 11.2 vs 8.6 ± 6.8, P < 0.001
• STN 组BFMDRS-M:14.5 ± 6.7 vs 8.3 ± 7.7, P < 0.001


DBS治疗梅杰综合征,术后无死亡或严重不良事件发生,极少数患者出现出血、定位、硬件并发症、移位、感染等并发症,由手术或慢性刺激引发的严重副反应未出现,一些轻症如运动功能迟钝、平衡恶化、口周紧密、僵硬、构音障碍,大部分都可通过调整参数逆转或减轻。


Gpi-DBS在改善梅杰综合征患者运动症状的同时,可以显著提高患者的生活质量,针对药物难治性梅杰患者推荐使用。
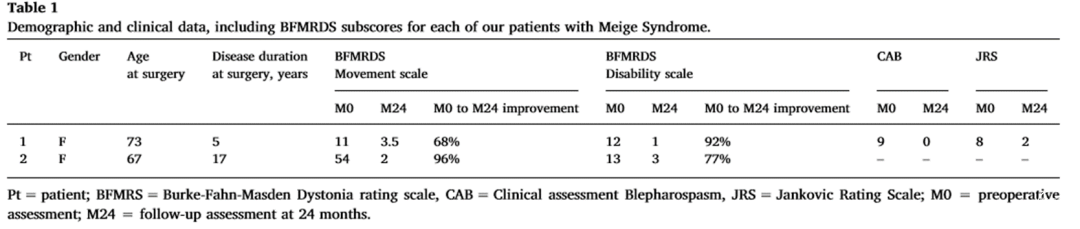
有文献报道,2例患者DBS术后残疾(BFMRS 、BDS)改善:患者1-77%;患者2-92%;术后24个月随访,肌张力症状(BFMRS、JRS)改善: 患者1-68%; 患者2-96%;残疾(BFMRS 、BDS)改善:患者1-77%;患者2-92%。


与帕金森病不同,梅杰综合征Gpi的腹侧通常是最佳的靶点位置,功能区对应面部相关神经元。Gpi通常单极刺激,双极刺激可以减少光幻视,但对症状无益。文献显示,交叉电脉冲可提供定制化的神经元组织激活。
• 传统程控的最优参数:BFMDRS:43-19,但颈部和右侧面部症状未改善
• 左侧电极使用双极刺激:10- 11+,但仍未改善治疗效果
• 使用交叉电脉冲,对刺激区域重新塑型,BFMDRS:19-2,随访2年稳定有效



DBS主要改善患者的运动症状,但患者非运动症状管理重要性逐渐受到临床医生重视。




硕士研究生导师
临床医学博士
江苏省神经调控专业委员会委员
江苏省医学会神经外科分会功能学组委员
江苏省中西医结合学会神经外科专业委员会青年委员
南京市疼痛学会微创学组委员
江苏省委组织部苏北发展特聘专家
江苏省第十五批“六大人才高峰”培养资助对象
专长于帕金森病、肌张力障碍、特发性震颤、三叉神经痛、面肌痉挛等疾病的诊断治疗。

点击或扫描上方二维码,查看更多“功能”内容












