原创首发于【神内资讯】微信公众号
今天分享的是陆军军医大学第二附属医院杨清武教授的《急性缺血性卒中影像学评估新策略》。本篇内容中,杨清武教授对急性缺血性卒中影像学评估策略进行了回顾,并对其影像学评估运用基础及影像学评估临床研究进展进行了详细介绍,欢迎大家阅读。
缺血性卒中概述
急性缺血性卒中(acute ischemic stroke, AIS):各种原因导致的脑组织血液供应障碍,并由此产生缺血缺氧性坏死,进而出现神经功能障碍的一组临床综合征,约占我国卒中的70%,具有高发病率、高死亡率、高致残率及高复发率等特点。
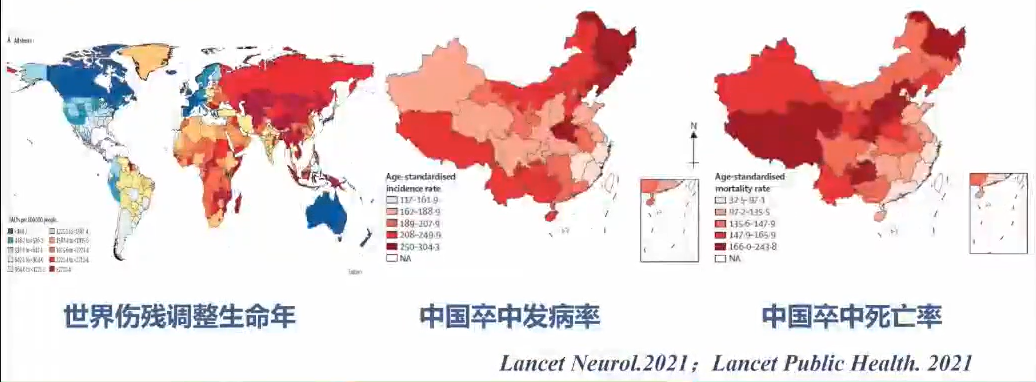
低收入国家是脑卒中的重灾区,其年龄标准化死亡率是高收入国家的3.6倍。
我国为世界脑卒中高发地区,脑卒中是国人首位致死致残性疾病。
缺血性卒中防治
再灌注治疗是急性缺血性卒中的有效治疗手段。
静脉溶栓联合血管再通治疗成为急性缺血性卒中的标准治疗方式,血管再通率从41%提升至94%,良好预后比例从26.5%提高至51%;
经高级影像筛选可超时间窗血管再通治疗,良好预后比例可达49%。
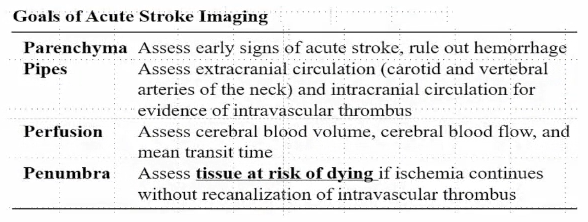
急性缺血性卒中影像学评估——目的
急性缺血性卒中影像学评估关注点——4P
Parenchyma:排除脑出血,发现早期缺血征象
Pipes:发现颅内外大血管阻塞与狭窄
Perfusion:评价脑血流动力学状况
Penumbra:鉴别可逆性损伤与不可逆坏死
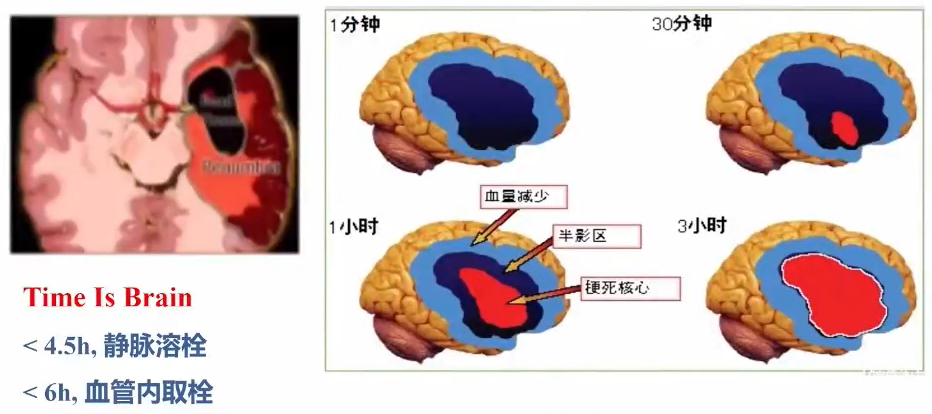
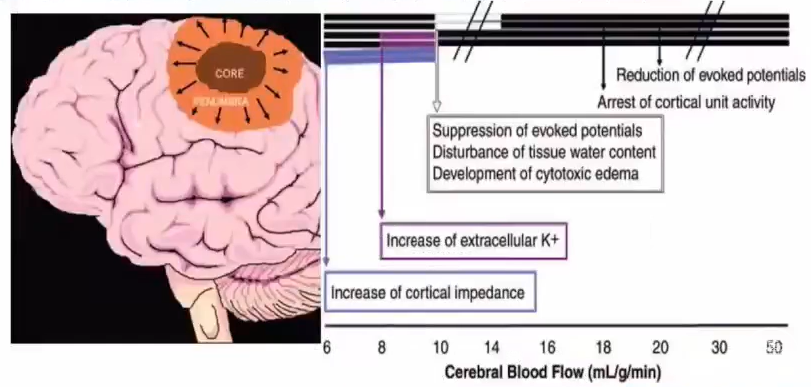
半暗带(Penumbra):可挽救的脑组织
急性脑缺血形成由不可逆的梗死中心以及周围环绕的顿抑细胞。
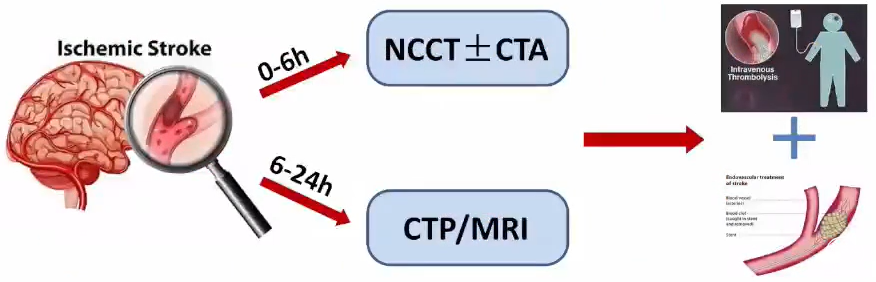
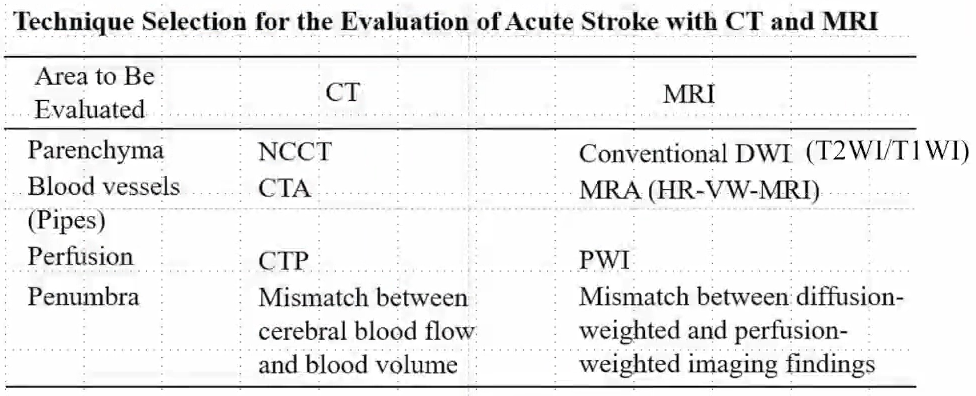
急性缺血性卒中影像学评估——方法
基于4p的影像学检查方法
急性缺血性卒中CT模式
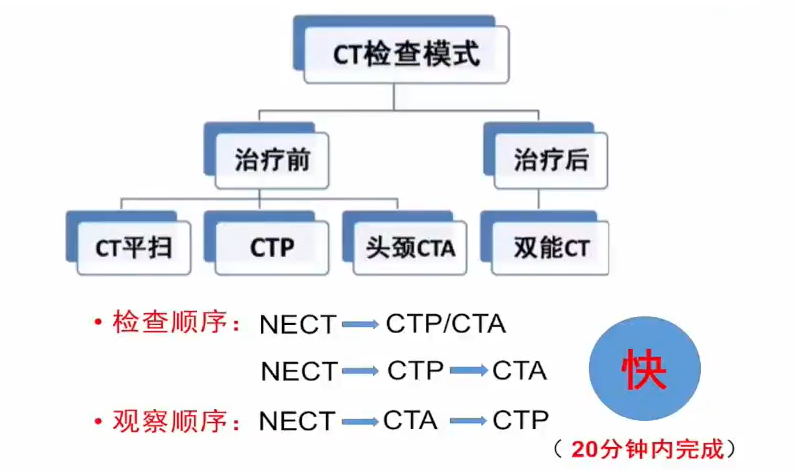
急性缺血性卒中一站式CT检查

梗死灶评估——CT平扫(NECT)
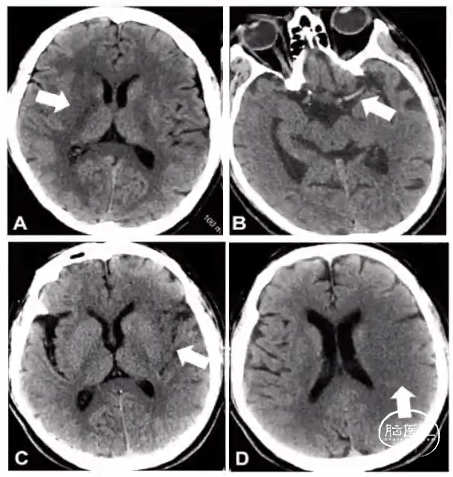
急性缺血性卒中CT早期征象
豆状核模糊征
大脑中动脉高密度征
岛带征
脑实质低密度、灰白质界限消失、脑回肿胀、脑沟变浅
注:CT早期征象常提示不可逆梗死核心
前循环ASPECTS评分:缺血进展的量化评估
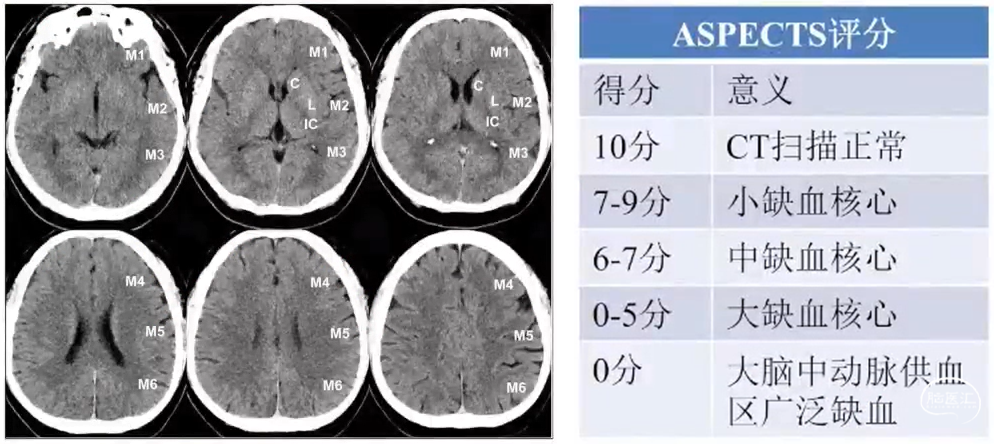
注:超早期梗死灶在NCCT上显示率较低,且存在其他低密度病灶,影响评分敏感性。
后循环的ASPECTS评分(pe-ASPECTS):缺血进展的量化评估
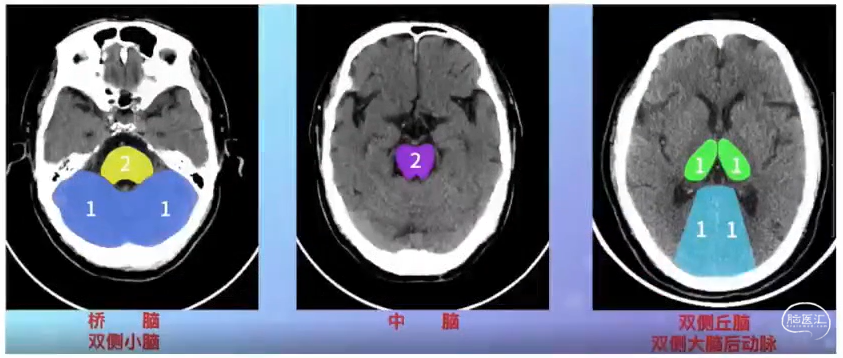
提高ASPECTS评分准确性
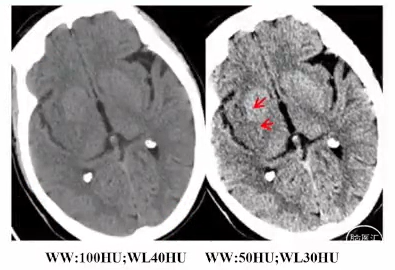
CT窄窗技术:推荐采用:窗宽50HU/窗位30HU
窗宽调窄
窗位降低
增加对比度
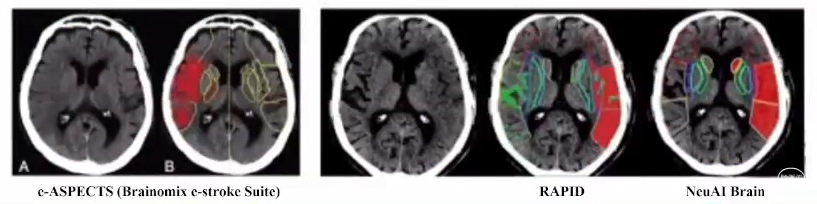
AI辅助评价: 评估准确性与影像专家接近
组织窗评估——CTP
CT灌注成像——CTP
灌注(Perfusion)是血流通过毛细血管网,将携带氧和营养物质输送给组织细胞的重要功能;动力来源于脑灌注压(CPP);
主要用于与脑的微小血管的血流动力学研究;发病30min可显示缺血灶;
评价缺血半暗带,敏感度90%,特异度100%。
关键:对比剂团注,高时间分辨率灌注
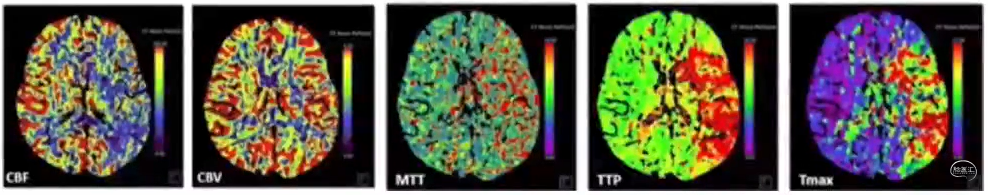
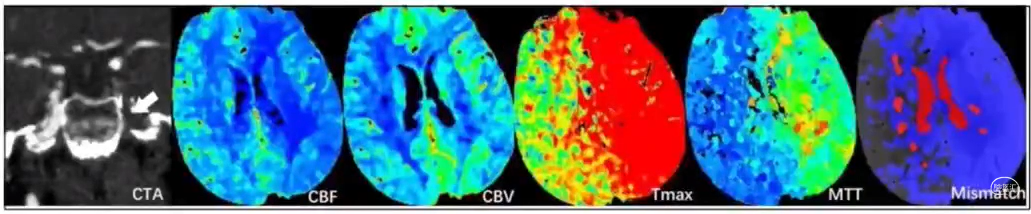
CTP参数
CBV,脑血容量,反映梗死核心的大小;
CBF,脑血流量,反映梗死组织的活性;
MTT,平均通过时间,MTT延长,CBV增加,提示存在侧枝循环或者血管再通;
TTP,达峰时间,间接反映脑灌注;
Tmax,残余功能的达峰时间,反映半暗带的指标。
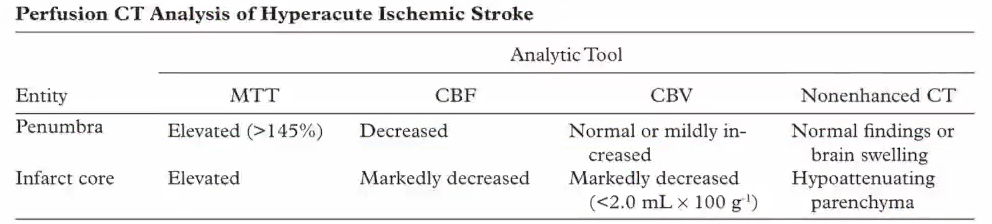
CTP评估——梗死核心
能量衰减,细胞毒性水肿
CBF<10ml/100g/min或<正常组织30%
CBV下降
Tmax延迟大于10s
CT低密度
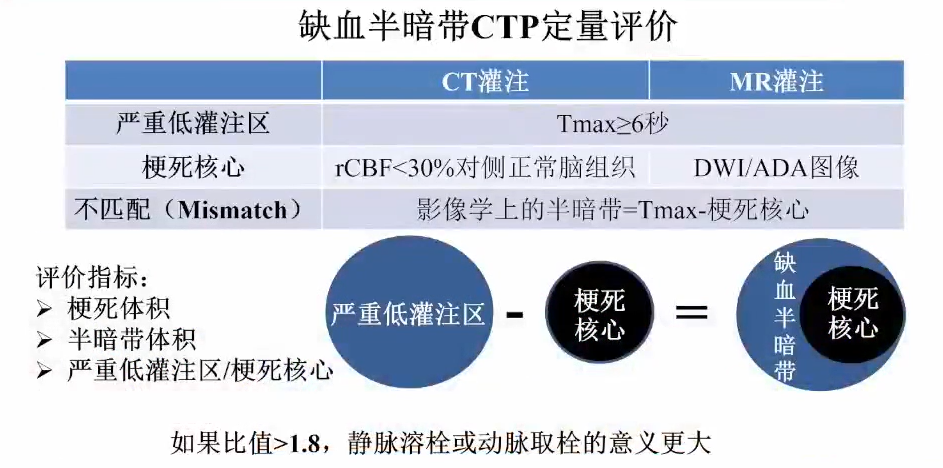
CTP评估——缺血半暗带
电衰竭,未到能量衰减
CBF 10-20ml/100g/min或<正常组织30%-50%
CBV正常或轻度增加
Tmax延迟大于6s,小于10s
CT无低密度
与梗死核心相同血管供血区内梗死灶周围的血流低灌注区,该区域神经细胞因缺血发生生理生化异常并导致功能障碍,但尚未死亡,及时改善低灌注可恢复正常。
CT灌注成像——CTP
通过低灌注区体积/梗死核心体积,计算不匹配概率(mismatch ratio),判断患者是否具有适合动脉内治疗的目标不匹配区域(target mismatch)
核心梗死区小(<70ml),低灌注区与核心梗死区不匹配比例大(>1.2或1.8)且严重低灌注区(Tmax>10s)<100ml,提示患者适合接受动脉内治疗。

组织窗评估——CTA
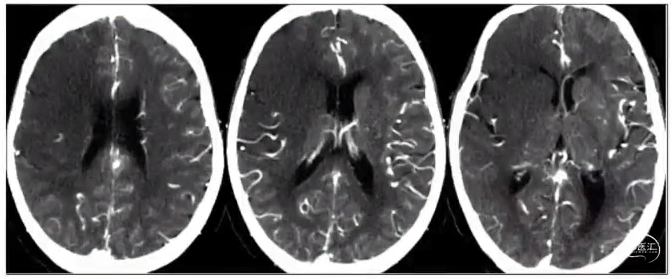
CTA源图像
在不具备CTP检查能力的防治卒中中心,可考虑采用CTA源图像进行缺血性半暗带初步评估。
CTA源图像低密度可能提示CBV减低,与DWI高信号及最终梗死体积密切相关,基于CTA源图像的ASPECT评分>5分,与良好预后相关。
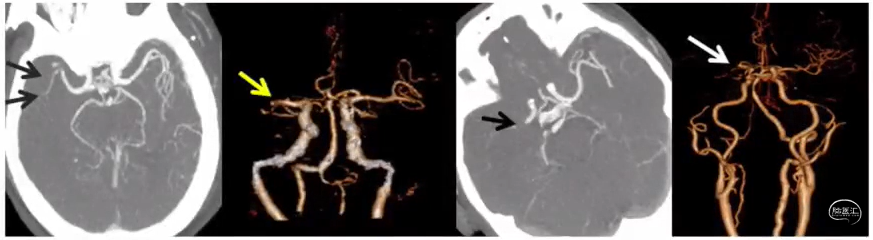
责任血管评估——CT血管成像(CTA)
临床无创诊断脑血管病的首选检查
CTA运用广泛,用以评估颅内外血管循环状况,快速明确血管闭塞位置
CTA主要对急性脑卒中颅内血管的血栓识别与颈动脉、椎动脉评估
CTA还可快速确定血管是否合并狭窄、钙化斑块以及弓上血管的入路路径是否迂曲,为血管内治疗选择适合的材料和技术方案提供参考依据
侧枝循环评估
侧枝循环的影像学评估
直接评估:DSA(金标准,有创、费用较高),CTA(单时相,多时相)MRA,TCD
间接评估:CTP,PWI,ASL
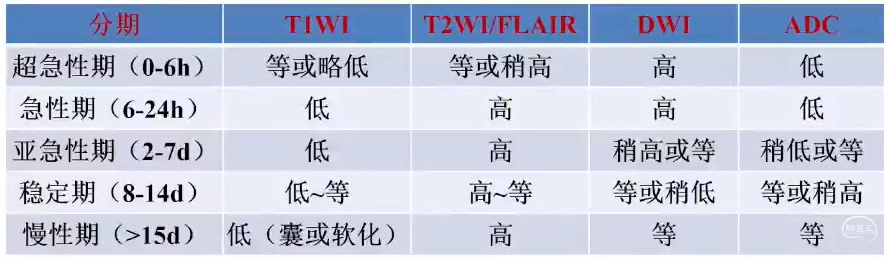
侧枝循环评估——单时相CTA
2分量表:1分,侧支血管差(闭塞区域血管充盈与对侧相比≤50%);2分,侧支血管好(闭塞区域血管充盈与对侧相比>50%)
3分量表:1分,仅脑表面侧支血管可见对比剂充盈;2分,外侧裂池区侧支血管可见充盈;3分,闭塞血管以远可见大量侧支血管充盈。
4分量表:0分,无侧支血管(闭塞区域无对比剂充盈);1分,侧支血管差(闭塞区域血管充盈与对侧相比>0但≤50%);2分,侧支血管中等(闭塞区域血管充盈与对侧相比>50%<100%);3分,侧支循环好(闭塞区域100%血管充盈)。
5分量表,缺失(absent)、少于(less)、等于(equalto)、多于(more)、明显多于(exuberant)对侧半球5个等级。
侧枝循环评估——多时相CTA
多时相CTA将侧支血管对比剂充盈状态与充盈时间延迟相结合,与单时相CTA相比,可更好地评估侧支循环状态,预测临床结局。
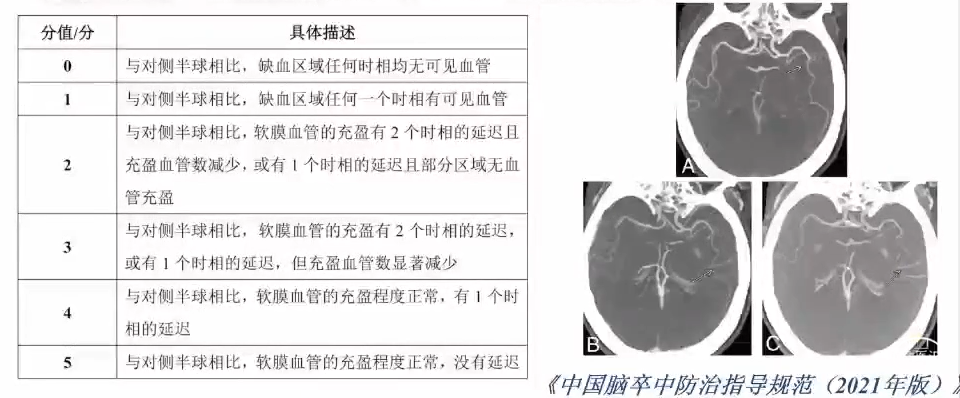

取栓术后复查——双能CT(DE-CT)
双能CT鉴别出血和对比剂外渗
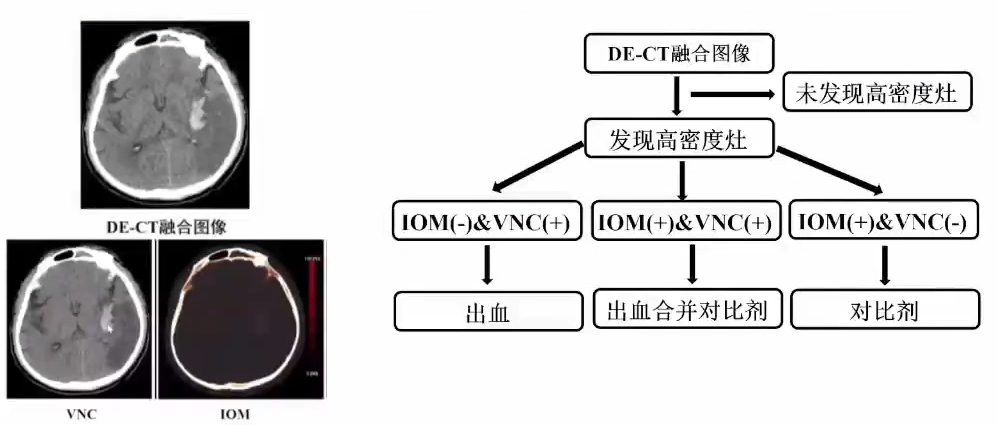
急性缺血性卒中MR模式
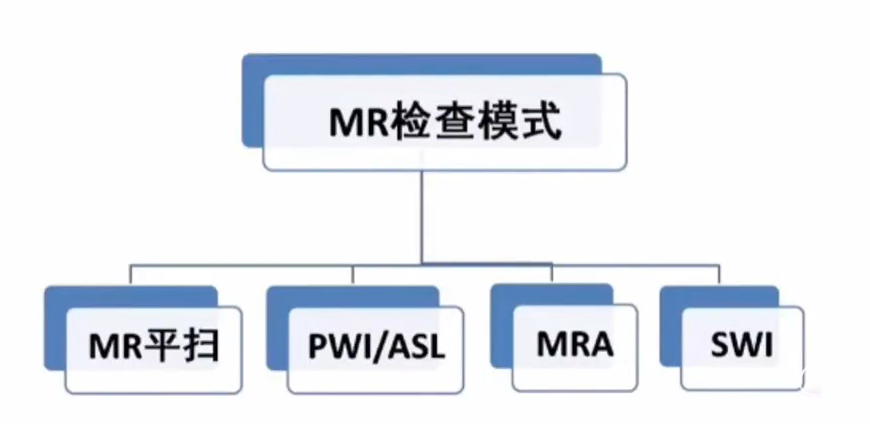
急性缺血性卒中多模态MR
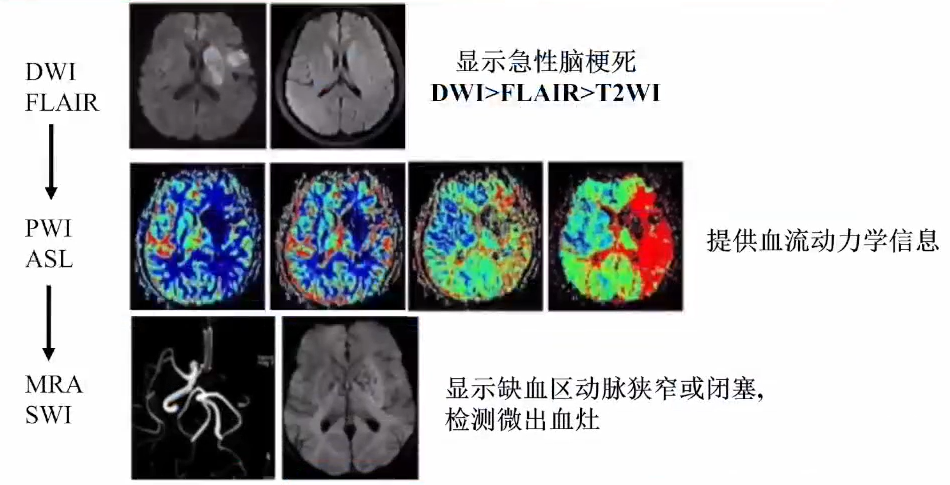
责任血管评估——MR模式
磁共振血管成像(MRA)
急性期脑梗死表现为:DWI高信号,表观扩散系数(ADC)图呈低信号,提示水分子扩散受限。(早诊断)
TOF-MRA无创、简便且更为安全,避免了肾毒性对比剂和电离辐射,能够显示大脑动脉环及其邻近颈动脉和各主要分支,可显示AIS的责任血管,评估血管有无狭窄、闭塞以及病变的程度
TOF-MRA容易将次全闭塞诊断为完全闭塞,容易对血管狭窄程度过度评估。
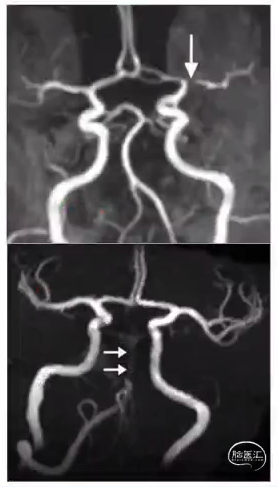
责任血管评估——磁共振血管成像(MRA)
HR-VW-MRI
清晰显示血管管腔、管壁及血管周围结构;
用于直接评估血管壁病变及对颅内动脉疾病诊断和鉴别诊断。

组织窗评估——MR模式
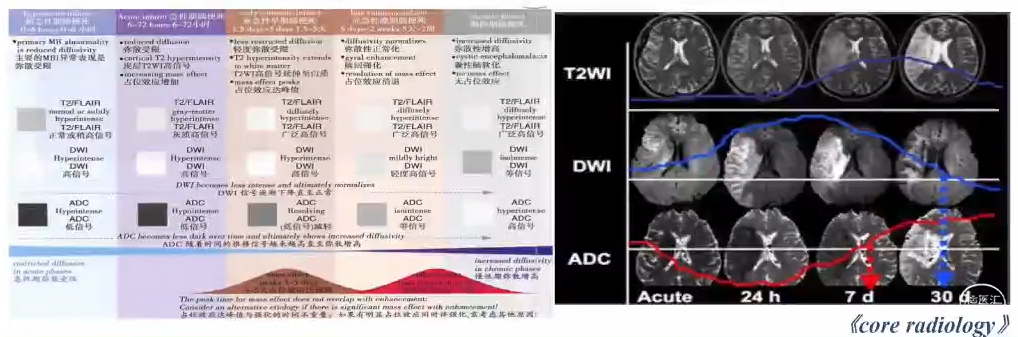
MR成像-DWI
在7-15天,DWI显示轻度升高/等信号影,而ADC表现“假正常化”;
DWI信号强度增加是由于早期弥散受限,之后是由于梗死组织T2穿透效应;
DWI信号不能被单独用于梗死阶段的评估,需与ADC图像对比评估。
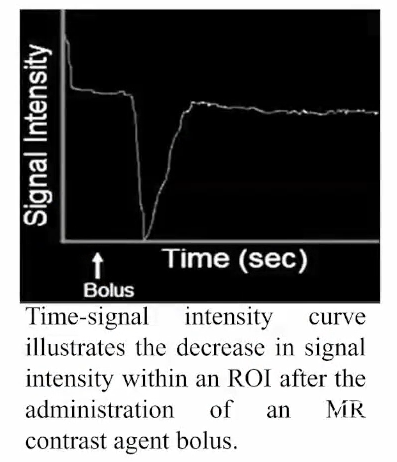
MR成像-PWI
PWI通过注射造影剂计算脑组织血液平均通过时间、脑血流量和脑血容量等参数,评估组织灌注,识别灌注不足的缺血半暗带,有助于在卒中早期筛选可能从再灌注中获益的病人并及时予以相应的治疗。
延迟峰值时间4~5.9s提示该低灌注区域为可逆性损伤区域。
DWI-PWI不匹配
DWI异常高信号代表梗死核心,PWI异常代表整个血流动力学的紊乱。
(1)核心梗死区:ADC值<600s/mm2的DWI高信号区域。
(2)低灌注区:Tmax>6s,或相对MTT值>145%对侧正常脑组织。核心梗死区小(<70ml),低灌注区与核心梗死区不匹配比例大(>1.8)且严重低灌注区(Tmax>10秒)<100ml,提示患者适合接受动脉内治疗。
缺血半暗带,可逆性脑缺血带。
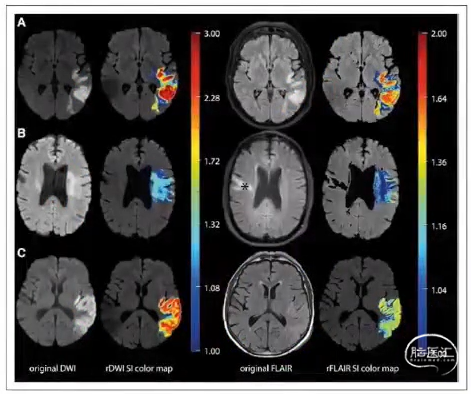
DWI-FLAIR不匹配
DWI高信号,FLAIR上相应区域信号改变不明显时,即DWI-FLAIR不匹配,表明患者发病时间在4.5h之内,作为静脉溶栓治疗筛选指标,适用于醒后脑卒中。
FLAIR像缺血区看到匍匐走行于脑表面的迂曲线血肿体积样高信号影,称为FLAIR血管高信号征(FVH),代表了缓慢血流的存在,可以提示侧支循环建立。
FLAIR血管高信号所在范围大于DWI高信号范围时,提示存在缺血性半暗带,可以快速识别可能从血管内治疗获益的近端大血管闭塞的AIS患者。
缺血性卒中影像学评估临床应用
缺血性卒中影像学评估——共识

缺血性卒中影像学评估——专家共识
2021年中国急性脑梗死缺血半暗带临床评估核治疗专家共识
对于发病<4.5h,拟行静脉溶栓的患者,应尽快行CT平扫排除出血,不推荐行多模影像学检查评估缺血半暗带而延误静脉溶栓时间(Ⅰ级推荐,A级证据)。
对于发病时间不明或距最后正常时间>4.5h,可考虑使用MRI检查,以FLAIR/DWI“不匹配”来评估缺血半暗带,筛选静脉溶栓可能获益的患者(Ⅱ级推荐,B级证据)。
对于发病<6h,拟行血管内取栓治疗的患者,应进行CTA或MRA检查明确血管情况(I级推荐,A级证据);根据临床症状、 CT平扫和CTA(MRI和MRA)结果,当NIHSS≥6分而ASPECTS≥6分时,或NIHSS≥8分而DWI高信号体积≤25mL者,可考虑血管内取栓,不必进一步进行灌注成像等其他影像学评估缺血半暗带(Ⅰ级推荐,B级证据)。
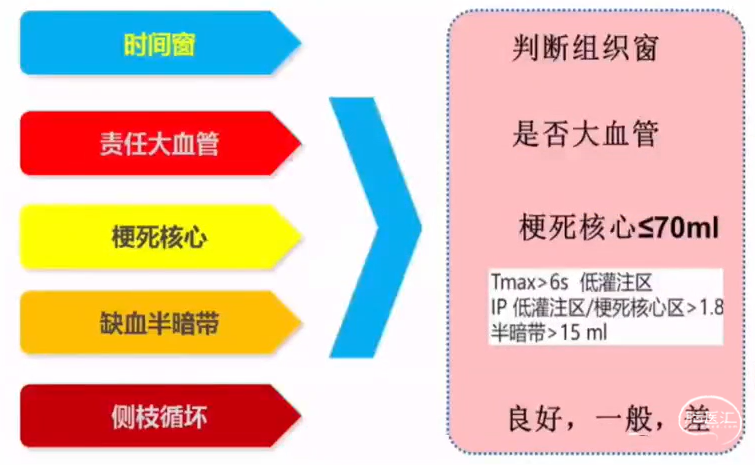
对于发病时间在6~16h的患者,应采用CT模式中CBF/CBV“不匹配”定性评价缺血半暗带;或参照DAWN或DEFUSE-3研究标准:以Tmax >6 s和rCBF <30%定量评价缺血半暗带,以低灌注体积/梗死核心>1.8,且梗死核心≤70mL、缺血半暗带体积≥15mL筛选适合取栓的患者(Ⅰ级推荐,A级证据)。
对于发病时间在16~24h或发病时间不明的患者,应采用CT模式中CBF/CBV“不匹配”定性评价缺血半暗带,可参照DAWN研究标准筛选适合取栓的患者(Ⅰ级推荐,B级证据)
人工智能辅助分析软件有助于快速、全自动定量评估梗死核心和缺血半暗带体积(Ⅰ级推荐,B级证据)。
侧支循环的评估有助于判定缺血半暗带的转归(Ⅰ级推荐, B级证据)
DAWN临床影像不匹配标准:
①年龄≥80岁,NIHSS评分≥10分,梗死面积<21ml
②年龄18-79岁,NIHSS≥10分,梗死面积<31ml
③年龄18-79岁,NIHSS≥20分,梗死面积31-51ml
患者存在严重神经功能缺失,但影像学显示梗死核心较小,提示存在较大范围缺血半暗带。
DEFUSE-3灌注/梗死核心不匹配标准:
核心缺血区<70ml,低灌注区与梗死核心体积比值>1.8且不匹配区域>15ml
临床研究新进展
与No CTP相比,经CTP筛选的患者功能预后更好,无效再通率降低;
与No CTP相比,经CTP筛选的超时间窗患者症状性脑出血和住院死亡无差异。
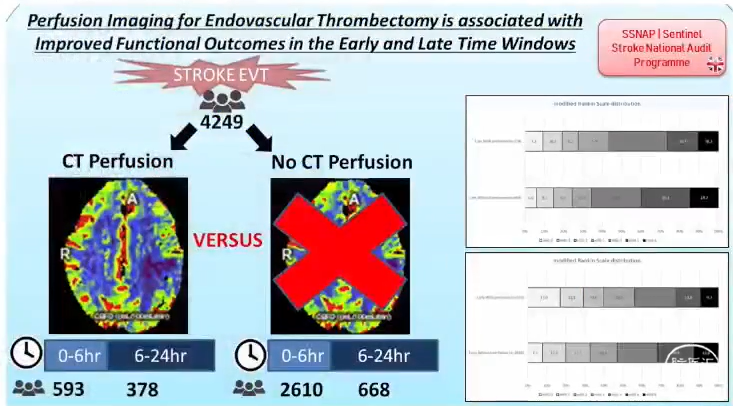
Stroke, 2022 Sep;53(9):2770-2778
CTP组和NCCT±CTA组在90天功能障碍(ordinal shift:aOR, 0.983[95% CI, 0.81-1.662],P=0.949)或功能独立(aOR, 0.640[95% CI, 0.318-1.289],P=0.212)方面无显著差异。
治疗时间窗(0-6小时vs 6-24小时)和CT选择方式(CTP vs NCCT±CTA)在90天的功能障碍方面无交互作用(P=0.45)。
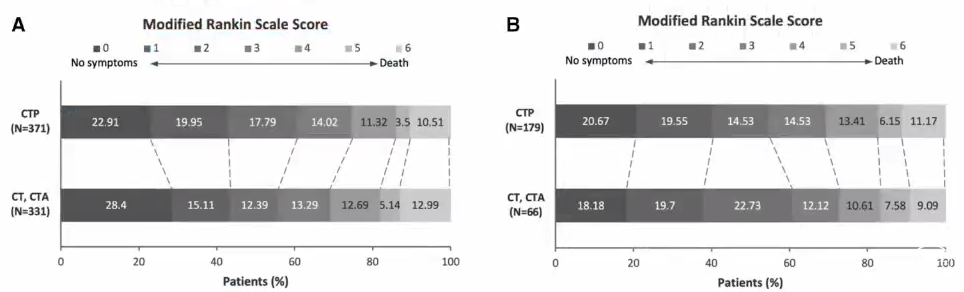
Stroke, 2021;52:491-497
观察性研究表明,超时间窗患者基于CT和CTP/MRI两种筛选模式对超时间窗急性大血管闭塞性卒中患者行血管内治疗,功能预后比例无差异。
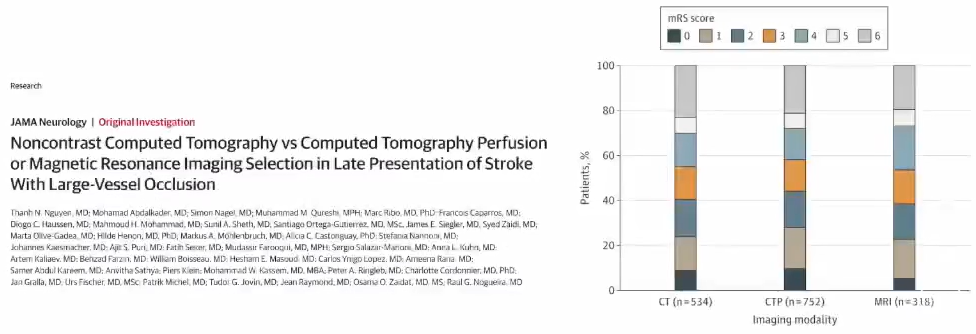
JAMA Neurology 2021
无论是时间窗内还是超时间窗,影像学评估模式并不影响EVT患者临床结局。

Stroke, 2022 Sep;53(9):2770-2778
讲者简介
杨清武主任医师
陆军军医大学第二附属医院
神经内科主任、教授/主任医师、博士生导师,博士后合作导师。
国家自然科学基金杰出青年基金获得者;教育部“长江学者”特聘教授;国家科技部科技创新领军人才;“重庆英才”优秀科学家;重庆市科技创新领军人才。
担任国家高等教育教学指导临床医学委员会委员;中华医学会神经病学分会委员;重庆市卒中学会会长。
Translation Stroke Research、Frontier in Neuroscience、Stroke Vascular Neurology、Brain Hemorrhages、生理学报及中华神经科杂志中华脑血管病杂志(电子版)等国内外学术杂志的副主编、常务编委、编委。
以通讯作者在国际著名期刊JAMA、JAMA Neurology、JAMA Net Open、Circulation、Ann Neurol、Prog Neurobiol、Neurology、Stroke、J Immunol及JCBFM等高影响杂志发表SCI论文70篇。
获省部级科技进步一等奖四项,主编专著1部,副主编专著4部,招收培养博士后、博士研究生、硕士研究生60余名。

扫描上方二维码
进入 杨清武 主任医师 学术主页
查看更多精彩内容
扫描二维码或
点击文末“阅读原文”
查看录播视频
![]()
声明:脑医汇旗下神外资讯、神介资讯、脑医咨询、神内资讯所发表内容之知识产权为脑医汇及主办方、原作者等相关权利人所有。未经许可,禁止进行转载、摘编、复制、裁切、录制等。经许可授权使用,亦须注明来源。欢迎转发、分享。






