新加坡国立大学化学与生物分子工程系的Min Wu等在来源于神经胶质瘤患者细胞颅内移植的小鼠模型,构建用于检测GBM的光声成像的纳米粒子TCFNP@iRGD,该材料在体外和体内均显示优异的GBM检测性能;结果发表于2022年9月的《Advanced Healthcare Materials》在线。
——摘自文章章节
【Ref: Wu M, et al. Adv Healthc Mater. 2022 Nov;11(21):e2201640. doi: 10.1002/adhm.202201640. Epub 2022 Sep 1.】
研究背景
研究方法
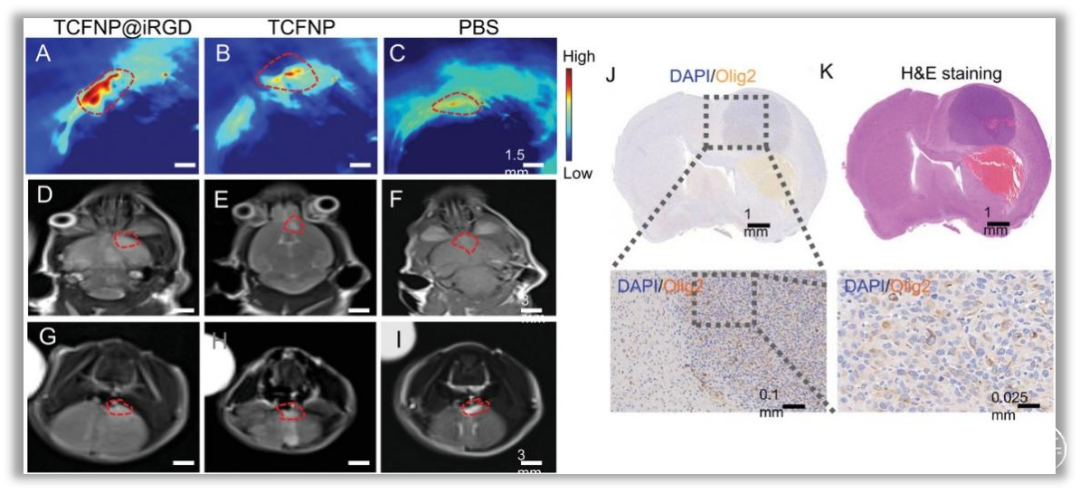
作者利用纳米沉淀法结合有机小分子PA造影剂[2-(3-氰基-4,5,5-三甲基呋喃-2(5H)-亚基)丙二腈(TCF)-OH]构建PA成像纳米材料(NPs)(TCFNP@iRGD)。同时在胶质母细胞瘤原位荷瘤小鼠模型中,利用MRI和PA成像对模型颅内肿瘤进行成像研究和对比。
研究结果
研究结果表明,通过纳米沉淀法合成的TCFNP与TCFNP@iRGD具有相似的物理性质,包括粒径大小和吸收峰。TCFNP@iRGD的PA信号生成性能呈浓度依赖性和具有优异的光稳定性。
作者发现,TCFNP@iRGD与GBM细胞孵育后可呈现来自透明质酸的红色荧光和TMRMA-iRGD的绿色荧光,两种荧光可良好相融,肿瘤细胞能成功摄取TCFNP@iRGD。作者利用肿瘤多细胞球模型(MCS)进一步研究该材料的穿透力,结果表明iRGD修饰可以帮助NPs渗透到MCS核心。
作者将3D MCS细胞嵌入凝胶中,并通过实时光声成像系统评估PA信号;发现TCFNP@iRGD处理后的MCS细胞比TCFNP有更强的PA映射信号。
研究结论
综上所述,研究采用有机小分子造影剂设计并构建GBM肿瘤靶向材料TCFNP@iRGD,实现在体内外检测GBM的优异性能。该研究成果作为基于GPDC颅内异种移植小鼠模型GBM光声成像的首篇报道,实现检测GBM肿瘤特异性的PA成像性能,证明该材料在GBM临床诊断中具有广阔的应用潜力。

声明:脑医汇旗下神外资讯、神介资讯、神内资讯、脑医咨询、Ai Brain 所发表内容之知识产权为脑医汇及主办方、原作者等相关权利人所有。





