
撰稿 | 随艺
排版 | AiBrain 编辑团队
亨廷顿病(Huntington’s disease ,HD)是一种常染色体显性遗传神经退行性疾病,由亨廷顿蛋白(HTT)基因外显子1的CAG短串联重复(STR)扩增引起。这种三核苷酸序列编码氨基酸谷氨酰胺(Q),将HD置于更广泛的神经系统疾病类别中,称为聚谷氨酰胺(polyQ)疾病。在突变型HTT中,运动症状可以从儿童期到老年期表现出来,其发病与CAG重复长度呈负相关,CAG重复时间越长,症状越早出现。
目前可用于HD患者的疗法只能提供适度的症状缓解,受影响的个体通常在诊断后15-20年因并发症而死亡。因此,HD治疗开发的一个主要重点已经转向通过消耗突变HTT来靶向疾病的根源。除了突变HTT蛋白的毒性外,越来越多的证据表明突变HTT mRNA也有助于疾病发病机制。因此,抑制HTT转录物和蛋白质水平的策略作为治疗方法将是最有益的。
2022年12月12日,美国加州大学圣地亚哥分校的Gene W Yeo课题组在Nature Neuroscience上发表了题为“An RNA-targeting CRISPR–Cas13d system alleviates disease-related phenotypes in Huntington’s disease models”的研究文章,该研究证明了RNA靶向的CRISPR-Cas13d系统作为HD治疗方法的原理证明,这种策略对治疗其他显性遗传疾病具有重要意义。


首先,作者开发了一种CAGEX RNA靶向Cas13d(Cas13d–CAGEX)系统,将其包装在慢病毒和AAV递送载体中的单个载体中,以评估其在多个已建立的HD临床前模型中的治疗潜力。这些包括来自HD患者的成纤维细胞、来自HD患者诱导的多能干细胞(iPSC)系的具有纹状体特征的分化神经元以及表达人突变外显子-1的全长突变HTT敲除小鼠模型,其在天然小鼠亨廷顿蛋白基因zQ175/+中具有扩增的CAG重复(约220个重复)(图1a)。
接下来,作者通过蛋白质印迹分析(图1c)、RNA点印迹分析(图1d,f)证实,本研究开发的Cas13d系统(包括CAGEX-2 gRNA,现在被称为“Cas13d - CAGEX”)可以有效地消除人类细胞中的CAGEX RNA和随后的polyQ蛋白,而可能不会靶向其他三核苷酸重复元件(如CUGEX)。
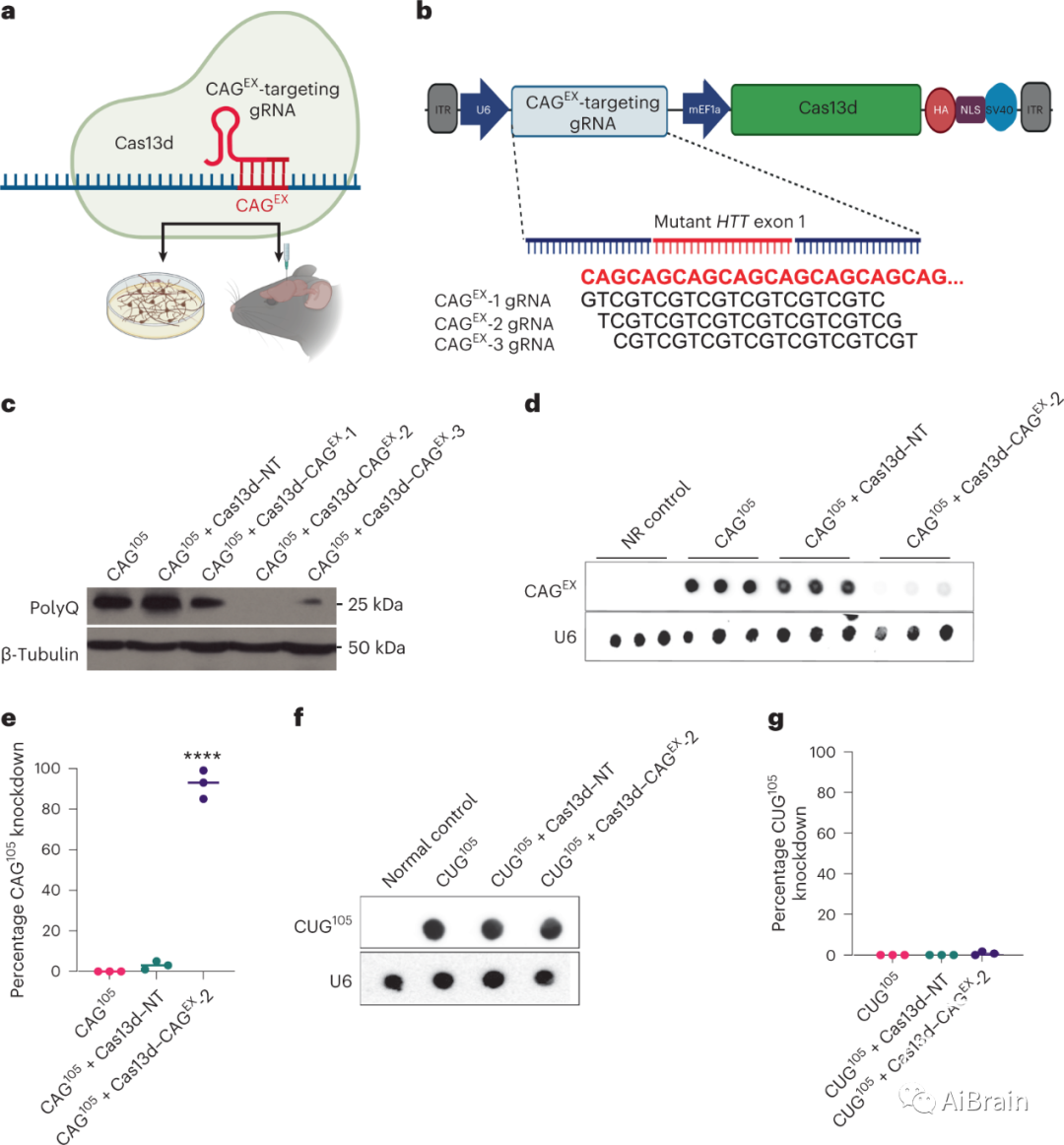
图1:以RNA为靶点,cas13d为基础的HD基因治疗方法的开发。

为了在人类临床前模型中评估Cas13d-CAGEX,作者从三个先前验证过的来自个体HD患者的iPSC系中产生了一组富含纹状体特征的神经元培养物。在分化后16日(此时每种培养物大部分由神经前体细胞组成),使用提供Cas13d-CAGEX或非靶向Cas13d-NT的组成型慢病毒系统转染每种HD和对照神经元培养物(图2a)。在分化后第32天,HD和对照培养物均由纹状体标志物阳性的神经元,多巴胺和cAMP调节的神经元磷酸蛋白(DARPP-32)和COUP-TF1相互作用蛋白2(CTIP2)组成(图2b)。
RNA槽点印迹杂交检测到,Cas13d-CAGEX显著降低了CAGEX RNA,在HD 66中降低了84.1%,在HD 77中降低了79.8%,在HD 109中降低了56.2%(图2c-d)。由于蛋白聚集是HD的病理特征,作者确定了Cas13d-CAGEX对EM48抗体免疫标记的突变型HTT聚集的影响。Cas13d-CAGEX处理的HD系与Cas13d-NT处理的HD系相比,突变型HTT聚集物显著减少,表明Cas13d-CAGEX可以选择性地抑制突变型HTT聚集物(图2e-g)。
为了评估Cas13d-CAGEX对(67/15)CAG重复序列(GM04723)和(46/18)CAG重复序列(GM02151)HD患者的成纤维细胞的等位基因选择性,作者使用了两种来自HD患者的成纤维细胞。使用基于患者特异性单核苷酸多态性(SNP)的引物进行的逆转录等位基因特异性定量PCR(RT-qPCR)表明,与转染Cas13d-NT的患者相比,在经表达Cas13d-CAGEX的慢病毒载体处理的每个患者成纤维细胞系中,突变型HTT RNA有显著和特异性敲低(图2h,i)。这些数据支持将Cas13d-CAGEX广泛用于突变型HTT中具有成人或青少年发病HD相关CAG重复长度的患者。

图2:Cas13d-CAGEX降低HD患者细胞mHTT mRNA和蛋白表达。

接着,作者利用DESeq2包进行的全转录组RNA测序(RNA-seq)分析确定了988个差异表达基因(DEGs),这些差异表达基因将HD神经元细胞系与对照区分开(图3a-c)。重要的是,上述每种HD相关病理通路的反向DEGs都富集,这表明本研究的基因疗法可以减轻先前报道的mHTT的下游影响。
作者观察到,48%(HD 109)、56%(HD 77)和45%(HD 66)的最稳健的HD DEGs被部分逆转(图3d-f)。除了常见的988 DEGs,令人兴奋的是,本研究还确定通过Cas13d-CAGEX治疗,HD109中患者特异性DEG也部分逆转了76.7%,HD77中的81.3%,以及HD66中较小程度逆转。这些结果表明,本研究的基因治疗方法减少了群体和个体患者中最常见的最突出的疾病标志物。
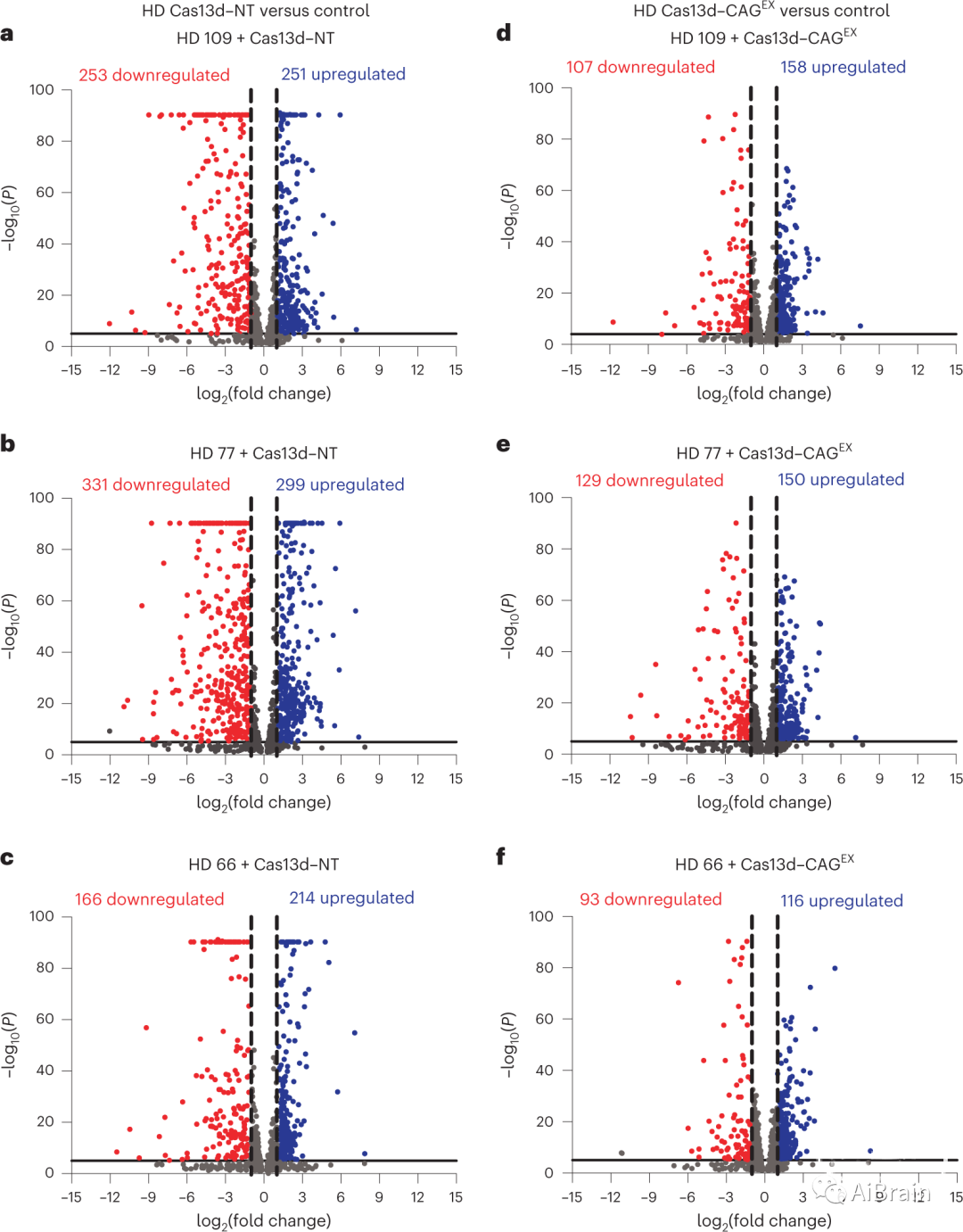
图3:Cas13d-CAGEX可部分逆转患者iPSC源性神经元的HD分子表型。

为了确定本研究的方法是否可以预防或停止zQ175/+小鼠体内神经退行性表型的进展,作者将Cas13d-CAGEX或Cas13d-NT包装到单链AAV血清型9(AAV9)病毒载体中,并对等量的两个月龄zQ175/+ HD小鼠和年龄匹配的野生型同窝小鼠对照进行双侧脑内注射Cas13d-CAGEX或Cas13d-NT。结果显示,运动功能和体重在注射后的8个月内进行纵向监测(图4a),并在研究结束时测定mHTT聚集物、HTT mRNA和蛋白水平。
作者通过平衡木实验评估了治疗对运动功能的影响。而zQ175/+ HD小鼠在8月龄及以后表现出明显的运动功能障碍;与接受Cas13d-NT治疗或未接受治疗的zQ175/+小鼠相比,接受Cas13d-CAGEX治疗的小鼠运动能力显著改善,表现为通过时间缩短(图4b)。重要的是,Cas13d-CAGEX对WT小鼠的运动功能没有影响(图4c),也没有改变zQ175/+(图4d)或WT小鼠(图4e)的体重,这意味着Cas13d-CAGEX不会对小鼠产生明显的不良影响。
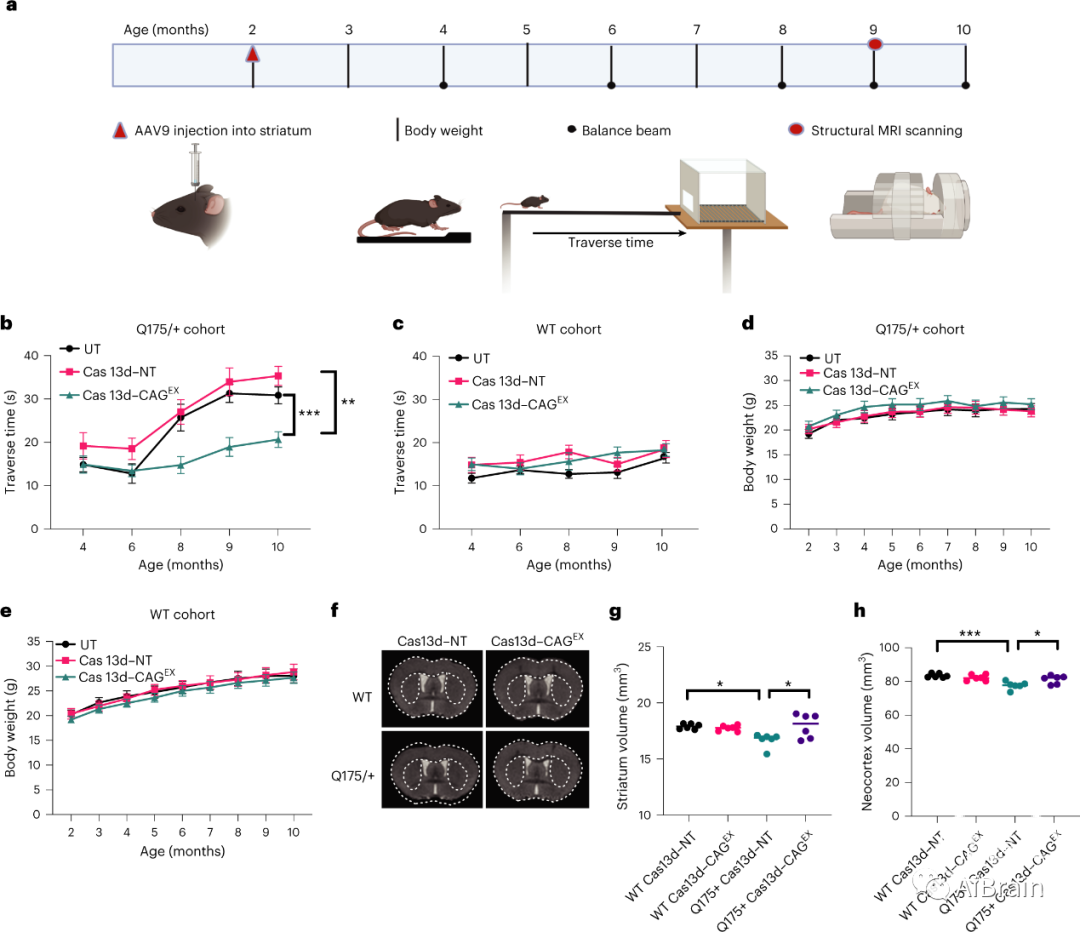
图4:Cas13d-CAGEX在HD全长敲入小鼠模型中的治疗效果。

接下来,作者确定了Cas13d-CAGEX对zQ175/+小鼠纹状体mHTT聚集的影响。与注射Cas13d-NT的zQ175/+小鼠相比,注射Cas13d-CAGEX的zQ175/+小鼠纹状体中EM48突变体聚集物显著减少(图5a-c),表明Cas13d-CAG+EX在体内可以有效抑制突变体HTT聚集物。
重要的是,在Cas13d-CAG+EX注射的zQ175/+小鼠纹状体中mHTT、HTT和蛋白水平显著降低。在接受Cas13d-CAGEX处理的zQ175/+和WT小鼠中,WT小鼠的HTT mRNA和蛋白水平均保持不变(图5d-f在图5g-k中定量)。这再次证明了使用Cas13d-CAGEX对致病性HTT mRNA进行等位基因选择性靶向的潜力。
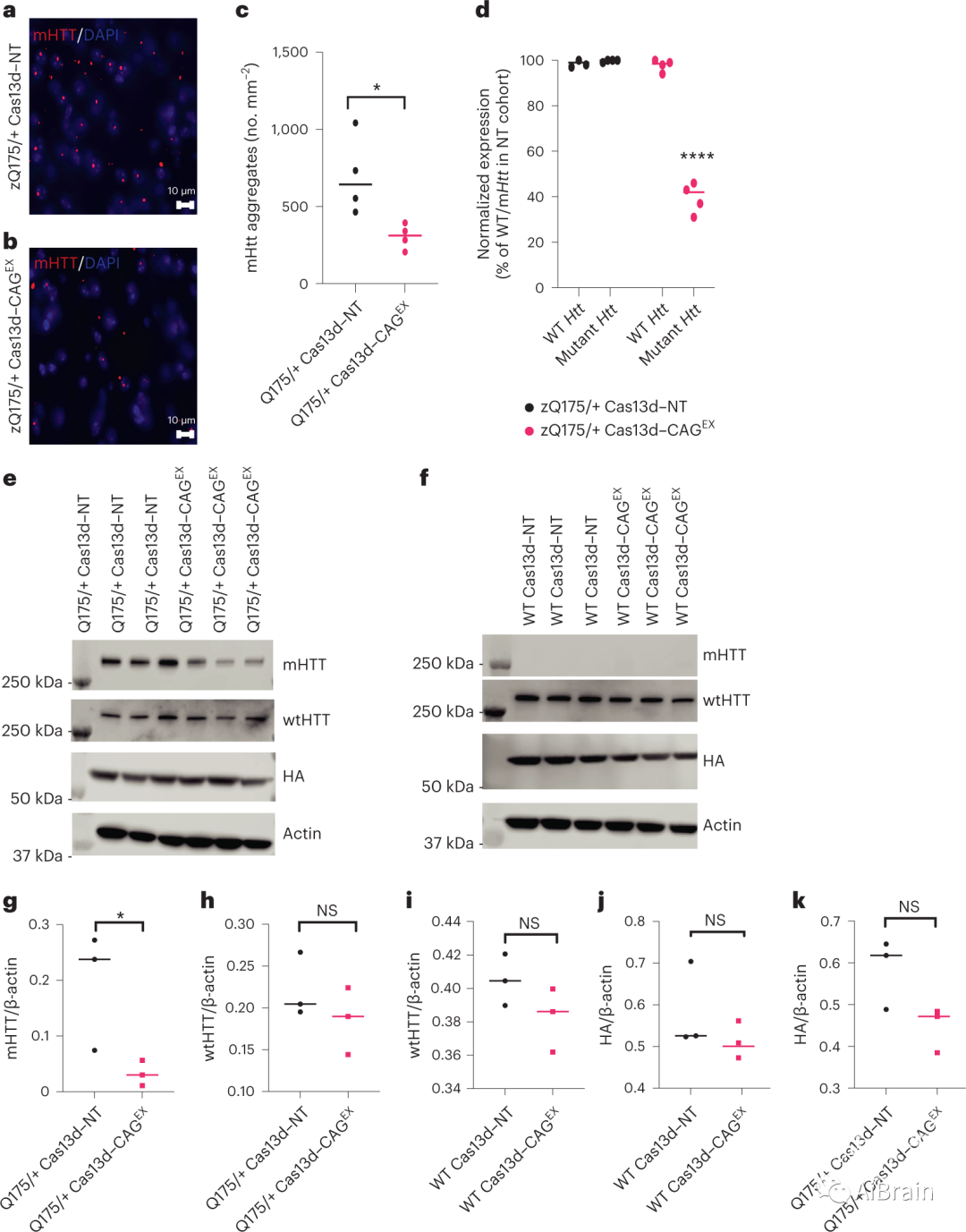
图5:在HD的全长敲入小鼠模型中Cas13d-CAGEX对突变型HTT蛋白和mRNA的等位基因特异性敲低。
综上所述,本研究在一个病毒递送载体中包装了Cas13d和CAGEX RNA靶向gRNA。确定Cas13d-CAGEX选择性地降低了来自3例HD患者iPSC系的纹状体神经元的CAGEX HTT RNA,提示对成人和青少年HD患者人群有潜在的治疗益处。病毒转染Cas13d-CAGEX在zQ175/+ HD小鼠中导致突变型HTT mRNA和蛋白的等位基因选择性抑制,脱靶最小。
最后,作者发现在Cas13d-CAGEX处理的zQ175/+ HD小鼠中,运动功能显著改善,mHTT聚集减少,纹状体萎缩减轻。这一策略对治疗其他神经退行性疾病具有广泛意义。
参考文献(上下滑动查看):
AiBrain内容团队为大家整理了文章的pdf,如有需要,请公众号后台留言“pdf”或扫码添加AiBrain助手微信获取。


✦往期精彩回顾✦


声明:脑医汇旗下神外资讯、神介资讯、脑医咨询、AiBrain所发表内容之知识产权为脑医汇及主办方、原作者等相关权利人所有。未经许可,禁止进行转载、摘编、复制、裁切、录制等。经许可授权使用,亦须注明来源。欢迎转发、分享。