
撰稿 | Kelin
排版 | AiBrain 编辑团队
髓鞘包裹神经元轴突是确保神经元的健康和电脉冲的快速传播以支持中枢神经系统(CNS)功能的重要基础,例如认知、学习和记忆涉及髓鞘的形成,需要髓鞘具有良好的结构完整性,而支持髓鞘健康的机制尚不清楚。中枢神经系统小胶质细胞是脑实质中唯一的一类固有免疫细胞,早期的一系列研究发现小胶质细胞在发育早期在胼胝体区域大量富集,其分泌的IGF1等生长因子可以影响髓鞘的发育;有研究通过药物清除发育早期脑中的小胶质细胞也发现髓鞘的发育受到显著影响。同时临床研究报道发现CSF1R突变的病人小胶质细胞缺失时存在脑白质的发育不良,均提示小胶质细胞对髓鞘健康具有重要作用。
近日,英国爱丁堡大学Veronique E.Miron课题组在《Nature》上发表“Microglia regulate central nervous system myelin growth and integrity”的研究论文。该研究通过转基因手段清除脑中的小胶质细胞,发现在发育早期(Postnatal 24-30)缺少小胶质细胞并不会影响髓鞘形成,但是对于髓鞘的生长及后期的认知功能具有重要影响,同时能够有助于防止髓鞘变性来保持髓鞘的完整性。小胶质细胞缺失主要通过TGFβ1-TGFβ1R信号的破坏促进少突胶质前体细胞中的脂质代谢,从而影响髓鞘的正常结构,最终导致认知能力下降。


集落刺激因子1受体(CSF1R)是维持小胶质细胞生存和再生的重要受体,哺乳动物Csf1r基因含有一个高度保守的超级增强子,即fms-intronic regulatory element(FIRE),因此作者使用CSF1R的超级增强子Fire缺失的转基因小鼠FireΔ/Δ,能够实现发育早期到成年后脑中小胶质细胞的缺失,而不影响血管周巨噬细胞(LYVE1+/Iba1+)(图1)。

图1. CSF1R增强子FIRE缺失可以清除脑中小胶质细胞
随后作者在P24-30,通过免疫荧光发现,相较于对照组(Fire+/+)小鼠,小胶质细胞缺失的FireΔ/Δ小鼠中成熟少突胶质细胞的数量无显著变化。同时通过免疫荧光分析胼胝体区域髓鞘相关蛋白MAG、MBP、CNPase、MOG和PLP等指标,均无显著变化;此外通过髓鞘电镜技术,进一步验证FireΔ/Δ小鼠胼胝体区域有髓鞘轴突的数量及成熟度均无显著差异(图2),说明在发育早期小胶质细胞的缺失不影响髓鞘的生成。
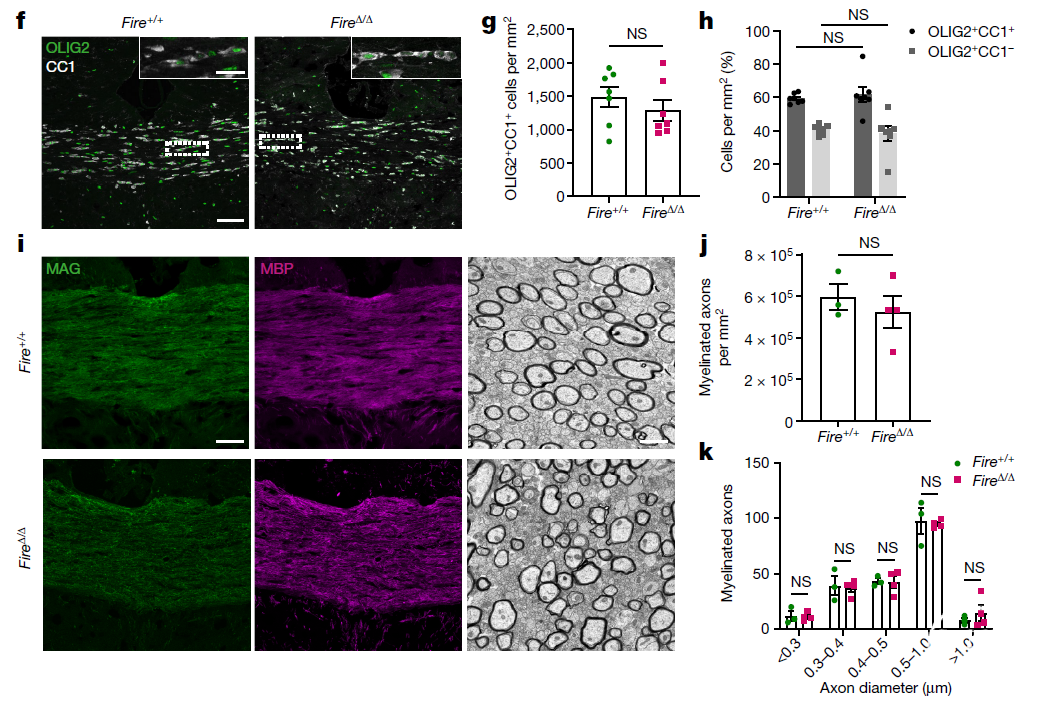
图2. 小胶质细胞对于少突胶质细胞的成熟和髓鞘生成是非必须的

虽然在FireΔ/Δ小鼠中并未发现髓鞘生成受到影响,但是作者通过高倍的电镜却发现髓鞘的结构存在异常(髓鞘外翻或松散),体现出髓鞘过度形成。在P25–P30,在FireΔ/Δ小鼠中44%有髓髓鞘表现出外翻或松散,而在Fire+/+对照组中只有14%的比例。FireΔ/Δ小鼠在较小直径的轴突上表现出扩大的未压实髓鞘(内舌区域),而在大直径的轴突中差异不显著,说明观察到轴突直径依赖性可能反映较大直径轴突的髓鞘形成发生在较小轴突之前,首先是内舌的生长,然后是压实,使髓鞘变厚。
随后作者分析了髓鞘变化对轴突健康的影响,通过分析发现虽然磷酸化神经纤维的表达在1个月时未受影响,但表明轴突运输受损的轴突体会在<0.1%的有髓鞘轴突中观察到。由于髓鞘结构的这些变化足以导致认知障碍,因此作者使用Barnes迷宫空间学习和记忆任务评估了FireΔ/Δ小鼠的认知情况,发现FireΔ/Δ小鼠认知灵活性也是受损的。
这一结果说明在缺乏小胶质细胞的情况下会发生髓鞘过度形成,这表明调节髓鞘生长需要小胶质细胞。

图3. 小胶质细胞调节髓鞘生长

为了进一步评估小胶质细胞对脱髓鞘的影响,作者通过髓鞘电镜技术对6个月大的FireΔ/Δ小鼠中的髓鞘的评估,发现FireΔ/Δ小鼠中存在大量脱髓鞘的区域,与Fire+/+小鼠相比,表现出有髓轴突的数量和比例的显著下降。
进一步分析发现与Fire+/+小鼠相比,6个月大的FireΔ/Δ小鼠的轴突保留髓鞘的内舌尺寸减小,髓鞘变薄。这些结果表明,随着年龄的增长,小胶质细胞的缺失会诱导中枢神经系统脱髓鞘。
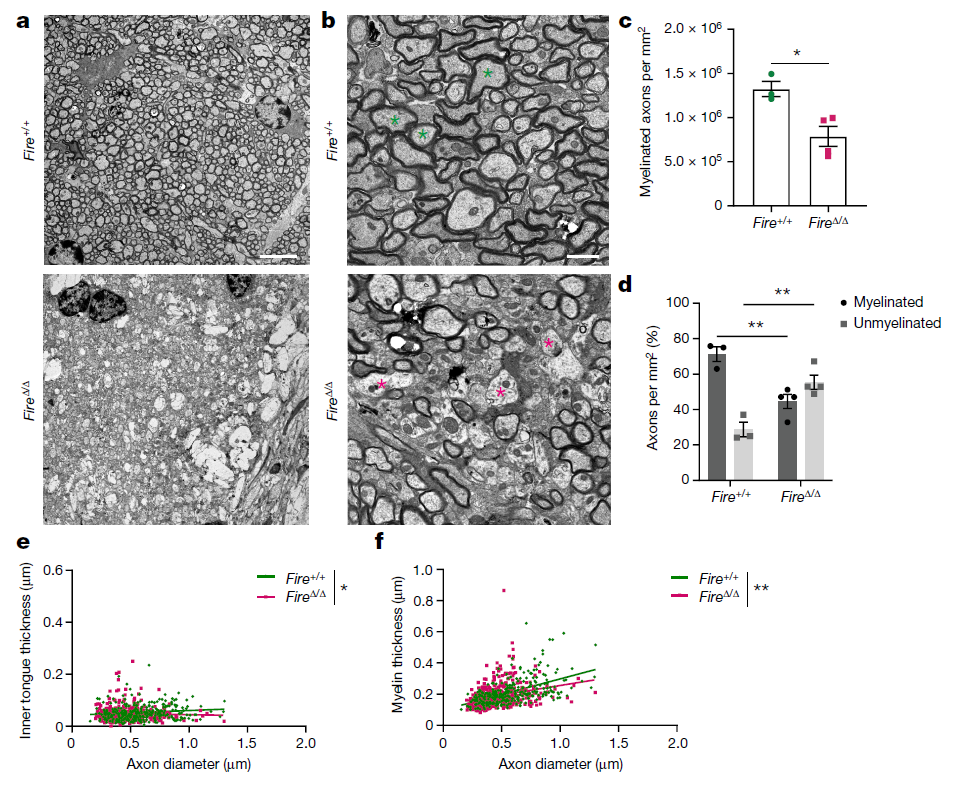
图4. 小胶质细胞的缺失导致脱髓鞘

作者为了进一步分析在人类中小胶质细胞是否也影响髓鞘的健康,因此进一步分析了CSF1R杂合突变的具有轴突球体和色素胶质的成人型白质脑病病人的(ALSP)样本,发现ALSP患者额叶白质中的小胶质细胞相对较少;此外,通过髓鞘电镜技术发现ALSP病人白质显示髓鞘外翻和散开、髓鞘变厚和扩大的内舌,观察到脱髓鞘并发现随着年龄的增长而逐渐恶化。这些结果也说明人脑白质小胶质细胞的减少与髓鞘形成过度和最终脱髓鞘有关。
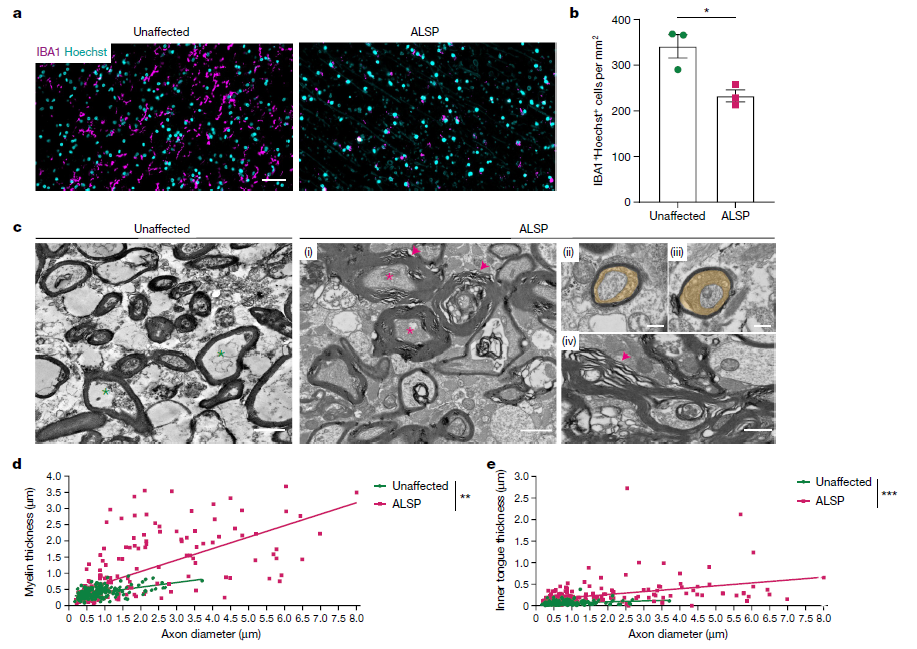
图5. 人类脑白质中小胶质细胞的减少与髓鞘形成和脱髓鞘有关

随后,作者进一步通过单细胞测序技术分析P24-30时期胼胝体区域,来探究在小胶质细胞缺失状态导致髓鞘健康丧失的细胞类型和分子机制。
作者对1个月大的FireΔ/Δ和Fire+/+小鼠的脑组织进行了单细胞RNA测序,根据细胞的标志基因将细胞分类,鉴定出四类少突胶质细胞(Olig 1-4),其中Olig1这群少突胶质细胞只在FireΔ/Δ小鼠中出现,且高表达Serpina3n和C4b,通过免疫荧光作者证实SERPINA3N + OLIG2 +这群少突胶质细胞缺失在FireΔ/Δ小鼠中存在。
通过对这群少突胶质细胞的基因进行富集分析,发现这群少突胶质细胞主要与脂质合成和代谢有关,进一步通过Ingenuity Pathway Analysis(IPA)分析发现主要是胆固醇生物合成和胆固醇生物合成途径I-III上调。而胆固醇富含髓鞘,是髓鞘生长所必需的成分。FireΔ/Δ小鼠脑白质的脂质组学分析也显示胆固醇酯增加和甘油三酯减少,这表明胆固醇过多和脂质输出受损。此外,已在ALSP病人中也有报道胆固醇转运相关基因的失调。
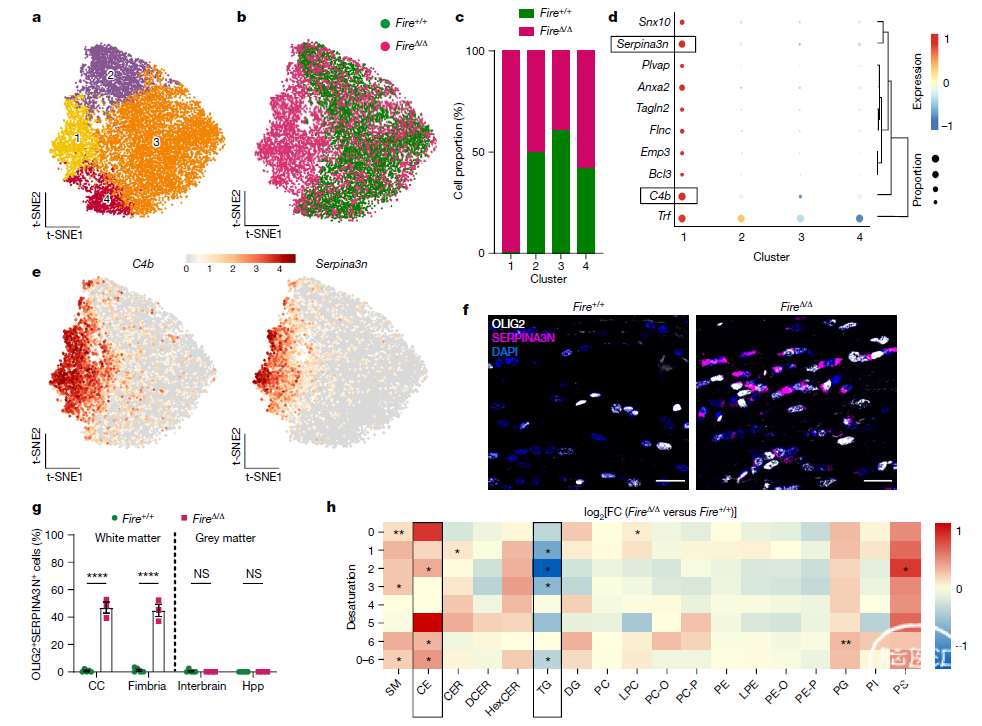
图6. FireΔ/Δ小鼠脑中特异性表达一群脂代谢旺盛的少突胶质细胞

随后作者为确定小胶质细胞的缺失影响高脂质代谢这群少突胶质细胞,作者对Oligo1这群少突胶质细胞显著改变基因的调节因子进行预测并鉴定出主要候选调节分子TGFβ1(主要由脑中小胶质细胞表达),同时大量研究报道其会影响脂质代谢。随后作者通过ELISA检测进一步分析发现TGFβ1水平在FireΔ/Δ小鼠白质中显着下调。
作者接下来分析TGFβ1是否会影响少突胶质细胞的功能。由于已有研究发现中枢神经系统中Tgfb1的敲除会导致小胶质细胞数量减少、稳态丧失和单核细胞浸润导致变量增多,因此作者在成熟少突胶质细胞中进行Tgfbr1的条件性敲除(PlpcreERT-Tgfbr1fl/fl)。从P14到P18进行他莫昔芬处理,到P28,在条件性敲除小鼠发现较小直径的轴突上具有增大的内舌,在较大直径的轴突上具有较厚的髓鞘,这一结果模拟了1个月大的FireΔ/Δ小鼠的现象。
那么在FireΔ/Δ小鼠中刺激TGFβR1信号是否可以逆转髓鞘的状态呢?为回答这一问题,作者在FireΔ/Δ小鼠的少突胶质细胞缺乏足够TGFβR1表达的情况下,使用TGFβ信号下游的小分子激动剂SRI-011381盐酸盐,这种方法可以直接刺激TGFβR1下游的SMAD2–SMAD3 通路。作者对2个月大的FireΔ/Δ小鼠使用SRI-011381盐酸盐,在三个月时发现与未经处理的FireΔ/Δ小鼠相比,髓鞘内舌厚度和髓鞘厚度均显着降低。这一结果表明,破坏的TGFβR1信号是FireΔ/Δ小鼠中髓鞘形成失调的主要机制。
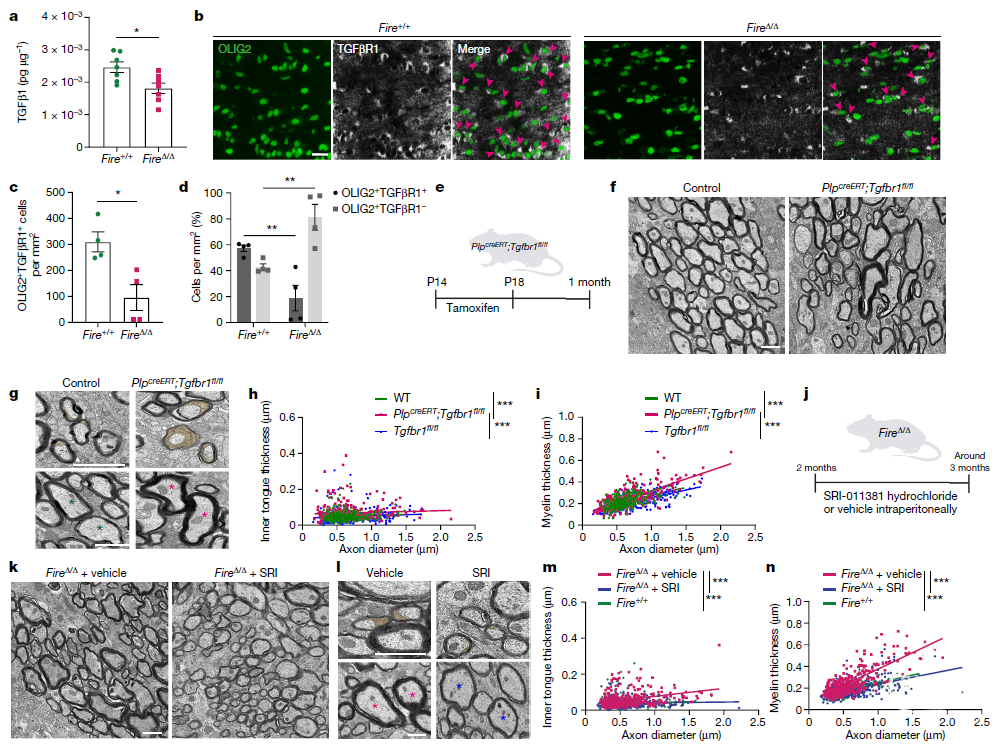
图7. TGFβR1信号能够调节髓鞘的完整性
综上所述,这一研究主要揭示了TGFβ1–TGFβR1轴在小胶质细胞-少突胶质细胞通讯中的重要作用,TGFβ1-TGFβ1R信号的缺失会导致少突胶质细胞的脂代谢的上调而影响髓鞘的健康。同时这一研究也揭示了小胶质细胞在维持成年期髓鞘健康和完整性方面的作用,并强调小胶质细胞是衰老和疾病中髓鞘破坏的关键治疗靶点。
参考文献:
Niamh B. McNamara,…..Veronique E. Miron et al. Nature. 2022. https://doi.org/10.1038/s41586-022-05534-y.
AiBrain内容团队为大家整理了文章的pdf,如有需要,请公众号后台留言“pdf”或扫码添加AiBrain助手微信获取。


✦往期精彩回顾✦


声明:脑医汇旗下神外资讯、神介资讯、脑医咨询、AiBrain所发表内容之知识产权为脑医汇及主办方、原作者等相关权利人所有。未经许可,禁止进行转载、摘编、复制、裁切、录制等。经许可授权使用,亦须注明来源。欢迎转发、分享。