
排版 | AiBrain 编辑团队
惊跳反射(startle reflex)是所有哺乳动物共有的一种响应外界刺激的非自主性快速防御行为,主要表现为闭眼、面部和头颈部收缩及全身弹跳等前期紧急戒备范式,为后续进一步的防御反应做好准备。负性情绪,尤其是恐惧情绪,可以调节动物的惊跳反射水平,这一现象被称为恐惧增强惊跳反射(Fear-potentiated startle, FPS)。
大量的临床观察表明,患有创伤后应激障碍症(Post-traumatic stress disorder, PTSD)、恐慌症(Panic disorder, PD)等恐惧情绪障碍症的患者往往伴随有惊跳反射异常增强的现象。然而,目前对这一现象的生理机制尚不清楚。
2022年9月18日,中国科学技术大学生命科学与医学部熊伟教授课题组在Molecular Psychiatry期刊在线发表了题为A midbrain-reticulotegmental circuit underlies exaggerated startle under fear emotions的研究论文。
在这项工作中,研究人员通过光遗传、化学遗传操纵、在体电生理记录及环路示踪等手段,发现了中缝背核(Dorsal raphe nucleus, DRN)-RtTg这条神经环路在FPS效应中的重要作用。

中国科学技术大学熊伟教授课题组前期对惊跳反射这种本能行为的神经环路及相关疾病进行了大量的研究。阐明了遗传性家族惊厥病(hyperekplexia)中过度惊跳反射的神经分子机制(Nat Neurosci, 2014; iScience, 2019; JBC, 2020);发现了网状背盖核RtTg谷氨酸神经元介导惊跳反射的发生,并鉴定了一条控制惊跳反射发生的神经环路,为后续研究不同情绪效价状态,如恐惧、抑郁、焦虑或是正性情绪对惊跳反射的调控奠定了基础(Nat Commun, 2021)。
这篇最新的Molecular Psychiatry论文中,研究人员首先构建了FPS模型小鼠,通过全脑c-fos染色及在体光纤记录,发现介导惊跳反射的RtTg谷氨酸能神经元,其活动在FPS效应时进一步增强(图1)。
随后,研究人员对RtTg神经元的上游一级投射脑区进行了病毒示踪,发现中缝背核DRN到RtTg存在直接投射。当使用光遗传手段激活该投射后,小鼠的惊跳反射行为出现明显增强。进一步的染色及追踪实验发现,RtTg脑区存在两种细胞类型,一是分布于RtTg外圈的GABA能(RtTgP-GABA)神经元,二是成簇分布于RtTg内核的谷氨酸能(RtTgC-Glu)神经元,而只有RtTgP-GABA 神经元特异性接受来自DRN内五羟色胺(5-HT)能神经元的投射(图2)。
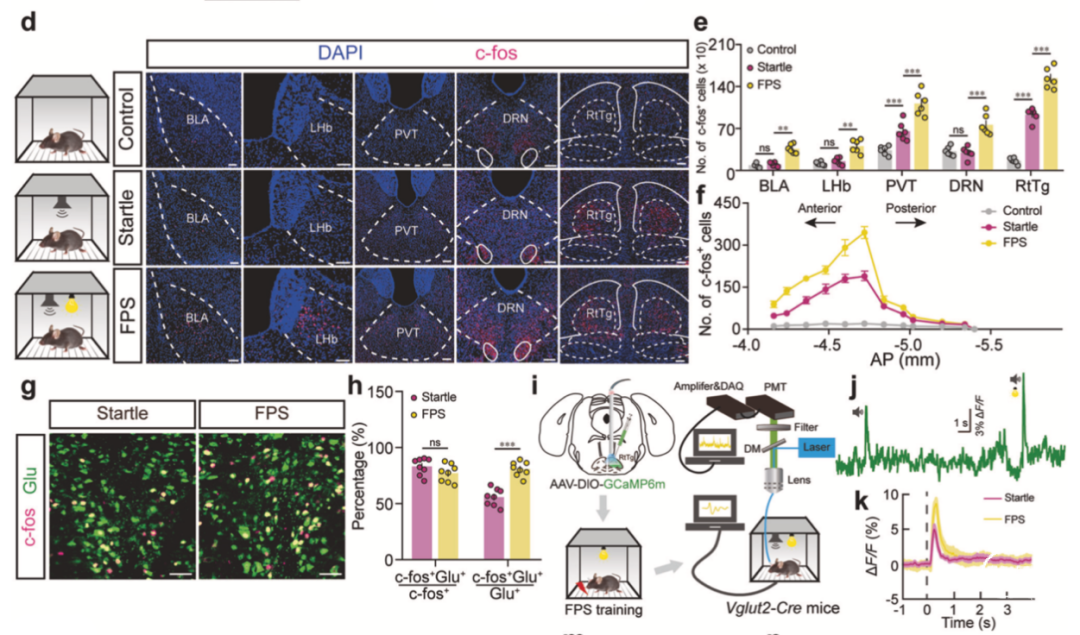
图1 FPS时小鼠RtTg内谷氨酸能神经元被激活
接下来,研究人员对DRN-RtTg投射环路进行功能解析,发现RtTgP-GABA与RtTgC-Glu神经元之间形成抑制性局部微环路。当条件性恐惧激活DRN-RtTgP投射环路后,RtTg内抑制性微环路得以解除,从而表现为恐惧增强惊跳反射。
化学遗传学激活DRN-RtTgP时,小鼠出现惊跳反射增强,而抑制DRN-RtTgP投射则可恢复小鼠在恐惧情绪下出现的惊跳反射增强。
最后,研究人员通过药理学筛选、荧光染色及shRNA敲降等手段,进一步在受体层面解析出5-HT1B在FPS效应中的关键作用。当用5-HT1B特异性拮抗剂阻断或shRNA敲降RtTgP内GABA能神经元上5-HT1B表达水平后,小鼠的FPS水平得以明显恢复。
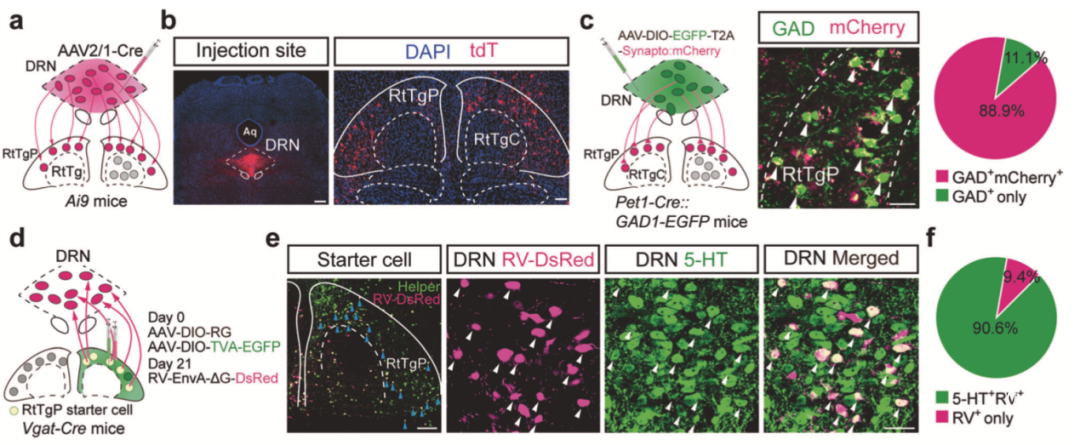
图2 DRN内5-HT神经元特异性投射到RtTg内GABA能神经元
综上,这项研究从环路鉴定、神经元类型分析、递质种类判断及下游受体亚型等维度,解析了恐惧增强惊跳反射的神经环路及分子机制(图3),研究结果加深了我们对高级情绪调控本能防御行为神经机制的认识,也为临床上开发能够更有效治疗惊跳反射异常的药物作用靶点及治疗方法提供了新的方向。
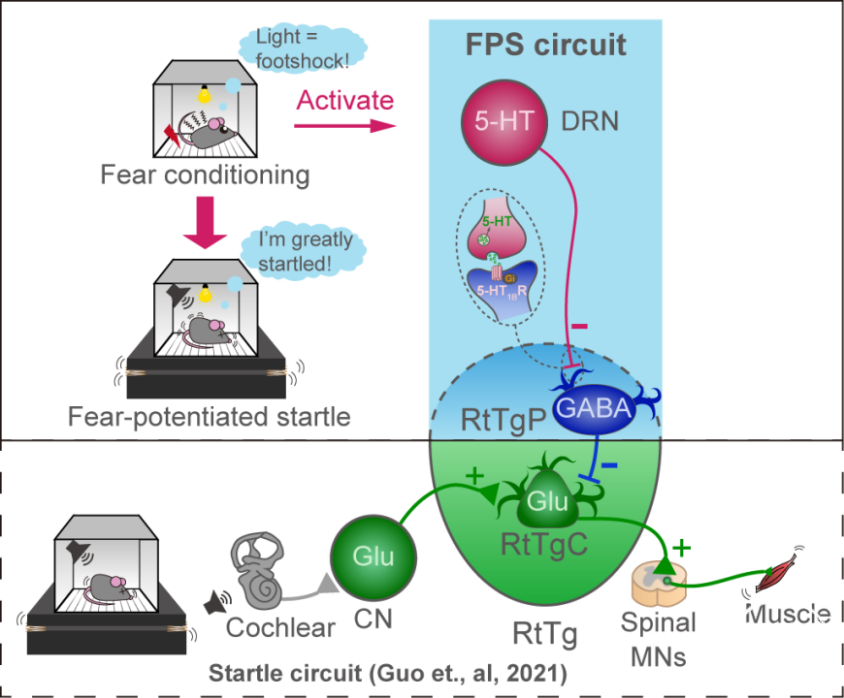
图3 惊跳反射及恐惧增强惊跳反射环路示意图
中国科学技术大学博士后郭薇薇、范思佳为论文的共同第一作者,熊伟教授为论文的唯一通讯作者。
原文链接:
https://www.nature.com/articles/s41380-022-01782-6
转载自 | BioArt



声明:脑医汇旗下神外资讯、神介资讯、脑医咨询、AiBrain所发表内容之知识产权为脑医汇及主办方、原作者等相关权利人所有。未经许可,禁止进行转载、摘编、复制、裁切、录制等。经许可授权使用,亦须注明来源。欢迎转发、分享。