美国约翰斯霍普金斯大学医学院神经外科的Alan R. Cohen等对儿童脑肿瘤分类和治疗的最新进展进行综述,文章发表在2022年5月的《The New England Journal of Medicine》杂志。
——摘自文章章节
【Ref: Cohen AR. N Engl J Med. 2022 May 19;386:1922-31. doi: 10.1056/NEJMra2116344.】
脑肿瘤是儿童常见的实体肿瘤,也是儿童癌症死亡的主要原因。中枢神经系统(CNS)肿瘤占儿童癌症的20%,发病率仅次于白血病。近来,随着中枢神经系统肿瘤诊断和治疗的发展,许多患儿的生存期和生活质量已有所改善。但是,儿童脑肿瘤的预后仍然较差。美国约翰斯霍普金斯大学医学院神经外科的Alan R. Cohen等对儿童脑肿瘤分类和治疗的最新进展进行综述,文章发表在2022年5月的《The New England Journal of Medicine》杂志。
低级别胶质瘤是儿童最常见的脑肿瘤。这组肿瘤有明显的异质性。与成人不同,儿童低级别胶质瘤很少转化为更高级别的肿瘤;成人低级别胶质瘤中常见IDH1或IDH2突变型可转化为高级别肿瘤;在儿童中较少见。
手术是大多数儿童低级别胶质瘤的初始治疗方法,以明确诊断,实现最大限度安全切除。在一项大型国际研究中,低级别胶质瘤儿童的5年无进展生存期为69%,5年总生存率为95%。肿瘤进展的危险因素为幼龄、切除不完全、纤维型组织特征和位于下丘脑或视交叉。儿童低级别胶质瘤常难以全切,特别是位于中线深处。这些肿瘤,部分生长缓慢,可进行影像学定期监测(图1)。放疗对复发或残留的低级别胶质瘤有效,5年无进展生存期为71%,总生存期为93%。由于放疗对发育中的大脑神经有杀伤性,故须根据年龄、解剖部位和遗传学特征对有进展风险的儿童采用辅助化疗。化疗药物包括长春新碱、卡铂、长春碱、6-硫鸟嘌呤、丙卡巴嗪、洛莫司汀、顺铂、依托泊苷和伊立替康等,无论是单药还是联合使用都有一定疗效。
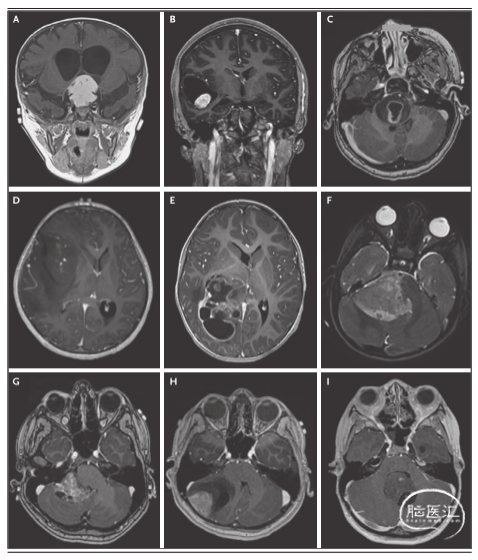
图1. 儿童脑肿瘤MRI-T1加权增强扫描,显示儿童脑肿瘤在位置、大小、强化和内部结构的异质性。
丝裂原活化蛋白激酶(MAPK)信号通路通过细胞表面信息传递调节基因表达完成多种细胞功能,包括细胞生长。大多数低级别胶质瘤有一个或更多MAPK通路改变,包括BRAF致癌基因的突变或融合、NF1突变、成纤维细胞生长因子受体1突变和神经营养酪氨酸受体激酶(NTRK)家族融合等。研究发现BRAF体细胞改变或NF1种系改变可能在肿瘤发生中起作用。一些低级别胶质瘤已发现有BRAF改变,它编码MAPK通路的下游调节因子——丝氨酸苏氨酸激酶蛋白(BRAF)。BRAF的两个常见改变是BRAF V600E癌基因的一个点突变和BRAF与另一个功能未知的大基因KIAA1549融合。
BRAF抑制剂(dabrafenib)和下游MEK抑制剂(trametinib和selumetinib) 正在深入研究。BRAF突变的儿童低级别胶质瘤,特别是与肿瘤抑制基因CDKN2A纯合缺失相关的儿童,对传统放化疗的反应较差。BRAF抑制剂对此初见成效。
(2)毛细胞型星形细胞瘤
儿童星形细胞瘤最常见的是毛细胞型星形细胞瘤,约占儿童、青少年和青年(<20岁)脑肿瘤的20%。肿瘤生长缓慢,10年存活率超过90%。肿瘤大多位于小脑和鞍上区,但也可出现在其它部位。毛细胞型星形细胞瘤很少发生恶性转化,一般预后良好。但20%的患者预后较差,出现局部复发或播散。在80%-90%的毛细胞型星形细胞瘤中发生KIAA1549-BRAF融合,特别是后颅窝的星形细胞瘤,可能与较长的总生存期有关。
(3)儿童弥漫性高级别胶质瘤
儿童高级别胶质瘤占儿童脑肿瘤的10%,预后差。经手术和辅助治疗后,有70% -90%患儿在确诊后的2年内死亡。“多形性胶质母细胞瘤”是成人最常见的原发性恶性脑肿瘤,WHO CNS5对其进行重新分类,强调分子标记物。新的分类将胶质母细胞瘤狭义地定义为发生于成人的弥漫性、IDH野生型星形胶质细胞瘤,它具有特定的组织学或分子改变。因此,“胶质母细胞瘤”一词已从儿童肿瘤中删除。
一项对儿童高级别胶质瘤认识的进展是发现染色质重排基因家族组蛋白H3的驱动突变。在弥漫性中线或半球胶质瘤患者中,体细胞H3尾部突变抑制甲基化并阻断其向胶质方向分化,促进胶质瘤形成。
第一种亚型是弥漫性中线胶质瘤,最致命,影响幼儿,不能切除。因为发现额外的分子变化,已用新的术语“H3K27改变(altered)”取代之前的“H3K27M突变(mutant)”。H3K27改变的肿瘤,包括先前命名的桥脑弥漫性内生性胶质瘤以及累及丘脑和其它中线结构的侵袭性胶质瘤。对弥漫性中线胶质瘤的甲基化的研究已确定组蛋白H3的致癌组蛋白错义点突变。与野生型相比,这些肿瘤的生存率较低。H3K27改变比组织学分级更能预测预后,是儿童弥漫性中线高级别胶质瘤的特征性改变。
第二种亚型是弥漫性半球胶质瘤,H3G34突变型,发生在年龄较大的儿童和年轻成人。该肿瘤与α-地中海贫血x连锁(ATRX)、TP53肿瘤蛋白53(TP53)突变和O6-甲基鸟嘌呤-DNA甲基转移酶(MGMT)启动子甲基化等基因改变有关。在超过80%的中线高级别胶质瘤和超过40%的大脑半球(主要是儿童)胶质瘤中已发现组蛋白改变。第三种亚型是儿童弥漫性高级别胶质瘤,H3野生型和IDH野生型,是一种侵袭性肿瘤,常见于大脑半球,预后较差。
第四种亚型是发生于新生儿和婴儿的一种临床上独特的肿瘤,是婴儿型半球胶质瘤,它通常含有酪氨酸激酶受体基因融合,包括ALK、NTRK1/2/3、ROS1和MET4。这些改变都是治疗靶点,初步研究发现激酶融合阳性的肿瘤疗效更优。
儿童弥漫性高级别胶质瘤的标准辅助治疗是局灶姑息性放疗,但长期生存率低,在过去50年里没有明显改善,其3年无事件生存率和总生存率分别为10%和20%。桥脑弥漫性中线胶质瘤的预后极差,未放疗患者中位生存期为4个月,而放疗者中位生存期也仅为8-11个月。
儿童高级别胶质瘤的靶向治疗已进入临床应用,但未显示明显疗效。化疗的总体疗效有限。替莫唑胺在成人高级别胶质瘤中,与单纯放疗相比,提高了无事件率和总生存率,但对于儿童并非如此。一项2期研究将洛莫司汀加入替莫唑胺,与单独使用替莫唑胺相比,无事件率和总生存率更好。
使用组蛋白去乙酰化酶(HDAC)抑制剂可靶向H3K27突变。Fimepinostat是一种泛HDAC和PI3K抑制剂,正用于涉及高级别胶质瘤和复发髓母细胞瘤的1期试验。其它在研究的治疗方法有免疫检查点抑制剂、嵌合抗原受体T细胞治疗、癌症疫苗和溶瘤病毒治疗等。
2. 室管膜肿瘤
室管膜瘤是儿童第三大常见脑肿瘤,仅次于胶质瘤和髓母细胞瘤,占儿童中枢神经系统肿瘤的5%-10%;90%在颅内,大部分起源于后颅窝,其余位于脊髓。室管膜瘤具有异质性;根据组织学、分子特征和位置进行分类,至少有9种分子亚型。以前的WHO组织学分类与预后相关性不佳,现已修改。
室管膜瘤根据间变程度分为1级、2级或3级,罕见的室管膜下瘤为1级,粘液乳头状室管膜瘤曾定为1级,现在归类为2级,因其复发的可能性与传统的脊髓室管膜瘤相似。
2级和3级室管膜瘤可位于幕上或幕下。幕上室管膜瘤根据两种致癌性分子融合进行分类。70%发生C11orf95-RELA融合,导致核因子κB信号通路的组成性激活。C11orf95基因的新命名为ZFTA;ZFTA可能与更多的配体融合,而不仅仅是RELA。另一种融合涉及YAP1。与YAP1融合相比,有报道称新命名的ZFTA融合在预测临床病程方面优于组织学分类,预示着预后较差。
基于甲基化组学分析,后颅窝室管膜瘤细分为两种常见的亚型:PFA和PFB室管膜瘤。前者主要发生在婴儿,位于侧方,预后比PFB室管膜瘤差。与PFB肿瘤相比,PFA肿瘤的H3K27三甲基化表观遗传标记相对缺失。PFB亚型多发于年龄较大的儿童,一般预后较好。
儿童非转移性室管膜瘤的初始治疗是最大限度安全切除,其次是局灶适形放疗。婴儿不适合放疗。化疗作用尚不明确。儿童室管膜瘤的长期预后仍然很差,10年的总生存率和无进展生存率分别为50%和30%。
胚胎性肿瘤也是一组异质性恶性中枢神经系统肿瘤,主要影响幼儿,约占儿童脑肿瘤的20%。肿瘤由小、圆、密集的蓝染细胞构成,胞浆稀少,分化程度不同,最初归类为原始神经上皮性肿瘤(PNETs)。发生在后颅窝称为髓母细胞瘤,发生在松果体区称为松果体母细胞瘤,发生在幕上为幕上PNETs。根据WHO CNS5,胚胎性肿瘤分为髓母细胞瘤和其它CNS胚胎性肿瘤两类。
儿童最常见的脑肿瘤是低级别胶质瘤;而髓母细胞瘤是儿童最常见的恶性脑肿瘤。它们通常起源于小脑,患者表现为颅内压增高或小脑功能障碍。髓母细胞瘤占儿童胚胎性肿瘤的60%以上,其中70%发生在10岁以下的儿童,男孩的发病率高于女孩。但根据肿瘤亚型的不同,其年龄和性别差异有所不同。三分之一的病例发生在三岁以下儿童。
与髓母细胞瘤患儿预后不良相关的因素,包括肿瘤体积大、发病时已播散、年龄小(<3岁)以及术后影像学上肿瘤残留大于1.5cm²。以前的形态学分类确定四种亚型:典型髓母细胞瘤、大细胞间变髓母细胞瘤、结缔组织增生结节性髓母细胞瘤和广泛结节性髓母细胞瘤。后两种类型相对预后较好。
CNS5系统识别的两种类型的髓母细胞瘤是分子定义的髓母细胞瘤和组织学定义的髓母细胞瘤。分子定义的髓母细胞瘤包括四种亚型,每种亚型都有独特的甲基化组和转录组特征以及独特的临床行为。遗传分析已经确定亚型的子类,并提出新的治疗策略。
WNT激活型占所有髓母细胞瘤的10%,男女发病率相同,发生在年龄较大的儿童或青少年。肿瘤位于小脑中线,有时累及脑干。WNT型髓母细胞瘤具有典型的组织学特征,通常与CTNNB1编码的β-catenin积累有关。90%的病例存在CTNNB1突变,导致核β-catenin积累,促进肿瘤发生。这类肿瘤预后较好,10年无事件生存率超过95%。
SHH激活型占髓母细胞瘤的30%,影响幼儿和青壮年。它们通常位于小脑半球,被认为起源于小脑外颗粒细胞层的前体。与WNT髓母细胞瘤相比,SHH髓母细胞瘤在生物学和临床上具有更多异质性。它们通常来自SHH-PTCH-SMOO-GLI信号通路的种系或体细胞改变,包括肿瘤抑制基因PTCH1的缺失或功能缺失突变(43%的病例),原癌基因SMO的激活突变(9%),以及癌基因GLI1和GLI2的扩增(9%)。SHH髓母细胞瘤根据TP53肿瘤抑制基因的存在或缺失进行分层。TP53突变(发生在9%的病例中)是肿瘤发生的驱动因素,预后不良,而WNT肿瘤中的TP53突变不影响结局。TERT启动子突变影响端粒结构的维持,发生在40%的SHH髓母细胞瘤中,几乎存在于所有成人病例中。SHH髓母细胞瘤分子分型促使靶向治疗的临床尝试,新的SMO抑制剂vismodegib和sonidegib治疗难治性或复发性SHH髓母细胞瘤的研究正在开展。在目前的命名中,非WNT、非SHH亚型包括第3组和第4组髓母细胞瘤。与WNT和SHH髓母细胞瘤不同,这些肿瘤发生在男孩中比女孩多见,常在初诊时已出现转移。肿瘤位于小脑中线,通常具有典型的或大细胞间变性组织学特征。潜在的驱动基因突变尚未确定。第3组肿瘤占髓母细胞瘤的25%,发生在婴儿和儿童,预后最差,5年总生存率为50%。第4组肿瘤最常见,占所有髓母细胞瘤的35%。发生在年龄较大的儿童和青少年;预后中等,5年总生存率为70%。基因改变包括MYCN癌基因(6%病例)和CDK6(5%-10%的病例)的扩增。与第3组髓母细胞瘤一样,该类肿瘤具有多种染色体畸变。可分为17q染色体富集的高危组,10年总生存率为36%,而11号染色体缺失和MYCN扩增的低危组,10年总生存率为72%,是高危组的两倍。包括最大限度安全切除后颅脊髓放疗和化疗。目前研究的重点包括对WNT髓母细胞瘤的降级治疗以减少脑脊髓放疗和化疗的毒性;SHH髓母细胞瘤的SMO及其下游通路的靶向治疗以及非WNT、非SHH髓母细胞瘤风险分层治疗。其它中枢神经系统胚胎性肿瘤,包括非典型畸胎样横纹肌瘤、伴有多层菊形团胚胎性肿瘤、中枢神经系统神经母细胞瘤(FOXR2激活型)以及伴有BCOR基因内部重复串联的中枢神经系统肿瘤。
综上所述,基因测序和DNA甲基化组学分析极大地改变儿童脑肿瘤分类。手术和辅助治疗的进展改善部分肿瘤的预后,但迄今为止,分子诊断对治疗进展的作用还有限。靶向治疗有望改善肿瘤预后,减轻治疗的不良反应。

声明:脑医汇旗下神外资讯、神介资讯、神内资讯、脑医咨询、Ai Brain 所发表内容之知识产权为脑医汇及主办方、原作者等相关权利人所有。
投稿邮箱:NAOYIHUI@163.com
未经许可,禁止进行转载、摘编、复制、裁切、录制等。经许可授权使用,亦须注明来源。欢迎转发、分享。









