
本次病例分享展示了一名51岁男性患者,病理检测及分子基因检测显示为胶质母细胞瘤,IDH野生型,TERT突变,MGMT启动子非甲基化,预期生存时间为11.3~13.4个月。患者于术后4周即进行同步放化疗+肿瘤电场治疗,并尝试联合PD-1免疫治疗及靶向治疗等综合治疗。治疗期间,虽然患者出现肿瘤反复变化、治疗相关性皮疹以及癫痫,经调整TTFields以及药物方案后,获得改善并生存至今。
01
患者基本情况
51岁,男性 因“右侧肢体乏力1周”入住外院,发现左侧顶叶占位,考虑胶质母细胞瘤,发展非常迅速
02
诊疗经过
2020-07-21:于外院行手术治疗
2020-08-06:开始TMZ125mg Qd(新辅助化疗)
2020-08-18:开始同步放化疗
2020-09-04:开始接受肿瘤电场治疗(TTFields)
2020-10-14:开始TMZ辅助化疗,西妥昔单抗450mg Qw,瑞戈非尼160mg 2w/1w(根据基因检测及个案报道)
2020-10-29:患者头部出现皮疹,考虑瑞戈非尼引起多见,停用西妥昔单抗和瑞戈非尼
2020-11-01至11-09:暂停TTFields(第一次暂停),待皮疹消退后,恢复使用TMZ+TTFields治疗
2020-12-19:患者意识变差,复查发现新的额叶病灶(第一次肿瘤进展)
2020-12-21:尝试降低靶向药剂量后,联合PD-1治疗(TMZ辅助化疗+TTFields+PD-1-200mg Q3w+西妥昔单抗200mg Q3w)
2021-01至02:经调整西妥昔单抗剂量和间隔时间后,虽间中出现皮疹,但对TTFields使用影响较小,病情稳定,能简单交流
2021-02-10至02-19:因春节期间,病人自行暂停TTFields(第二次暂停)
2021-02-19:癫痫发作,继续调整西妥昔单抗用量,以增加TTFields使用时间
2021-03-10:癫痫控制,神志转清,没有皮疹
2021-03-15:出现PD-1相关性皮疹爆发,立即采用(丙球0.4g/kg+甲强龙2mg/kg)*3d,每3d减量,同时保护创面,预防感染,营养支持;处理后皮疹消退,精神好转,右下肢肌力改善到3级
2020-03-15至04-04:皮疹治疗期间,暂停TTFields20天(第三次暂停)
2021-04-10:恢复使用TTFields,语言功能进一步改善
2021-04-21:PD-1和靶向药停用后,复查MR:原发灶肿瘤和左侧额叶新生肿瘤增大
2021-05-10至05-14:SRS治疗左额叶病灶
2021-05-27:复查MR见原肿瘤及额叶转移灶内出现坏死,但脑水肿明显,对侧出现新发肿瘤(第二次肿瘤进展),降低西妥昔单抗剂量(100mg Q2w),加用贝伐珠单抗(300mg Q2w),结合TTFields,后仍因无法耐受头部皮疹,故停用TTFields(第四次暂停)
2021-06-18:患者皮疹消退后,对侧额叶病变进一步增大,CBF明显增加,后接受SRS以及西妥昔单抗100mg Q2w+贝伐珠单抗300mg Q2w治疗对侧额叶病变
2021-10-12:原病灶缩小,中线复位,左侧额叶新生肿瘤(第三次肿瘤进展),接受SRS治疗左侧额叶病变
2021-12:患者不能耐受西妥昔单抗的皮疹副作用,对贝伐珠单抗的皮疹反应为轻度,减量至200mg Q2w后可以耐受。MR(2022-02-22)显示原额叶病灶缩小,右侧脑室旁新生肿瘤(第四次肿瘤进展),原发灶周边有增长趋势,后接受SRS治疗右侧脑室旁病灶
2022-04-11:复查可见右侧脑室旁新生肿瘤坏死,但原发灶在增长
患者病情变化图(至2022-04):图示

03
病理检测及分子基因检测结果


患者属IDH野生,TERT突变型GBM,预后约11.3个月
患者属MGMT无甲基化组(即甲基化均值<10%),其mPFS为7.2个月,mOS为13.4个月
MGMT启动子非甲基化,对替莫唑胺敏感度较低
TMB=1.35muts/Mb;微卫星稳定型(MSS)


04
影像学资料

















05
佩戴TTFields情况

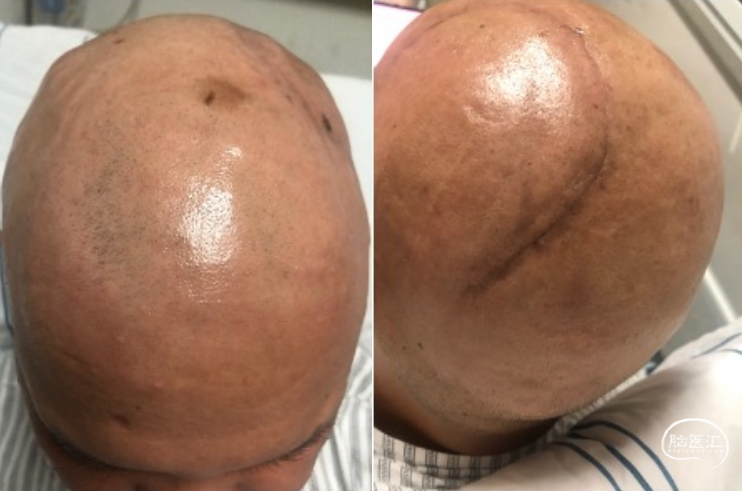









2021-09-16随访生活质量,如视频所示。

06
结论
男性患者,51岁,肿瘤切除后接受放化疗以及TTFields 术后病理检测及分子基因检测显示为胶质母细胞瘤(IDH野生,TERT突变),预后约11.3个月;MGMT无甲基化组( 即甲基化均值<10% ),mPFS为7.2个月,mOS为13.4个月 患者术后约1月开始进行同步放化疗,同步放化疗期间接受TTFields;期间出现额叶转移、对侧新发肿瘤、额叶新生肿瘤以及右侧脑室旁新生肿瘤等4次肿瘤进展,1次癫痫;根据患者具体情况动态调整放靶向药物以及免疫疗法药物,调整TTFields佩戴时间 远端进展的出现可能有:1.TTFields根据肿瘤位置进行个体化定位,TTFields强度集中于肿瘤发生位置,以达到最佳治疗效果;2.在出现远处肿瘤复发脑区,放射野未覆盖或覆盖剂量不足;3.使用TTFields的患者生存时间延长,所以更有机会观察到远端转移的发生 提高患者的依从性是TTFields改善胶质母细胞瘤生存的独立预后因素;TTFields期间,因皮疹/癫痫暂停TTFields4次,后经药物处理后病情好转并逐渐稳定
这例患者在外院手术后转来我院,从早期治疗期间的MR结果来看,肿瘤的恶性程度极高。这与患者的肿瘤基因检测的不良预后分子特征相符:IDH野生型,TERT突变,MGMT启动子无甲基化。因此,在早期即给与了积极的综合治疗。按照NCCN指南,早期放疗期间即用上TTFields,放疗结束即按照基因检测到的突变靶点以及其相关案例报道,探索性应用靶向治疗,给予早期干预。但是,靶向药物的副作用间接减少了TTFields的使用时间,影响疗效。因此,在使用TTFields联用其他治疗时,特别需警惕选用容易引起皮疹的药物,以免影响TTFields的疗效。
在整个治疗过程中,该患者陆续出现颅内多处肿瘤,在TTFields问世前相对少见,可能与TTFields主要集中于原发肿瘤的位置,而且患者生存时间延长,以致临床上可以观察到更多的胶质瘤生长模式,有助于我们对胶质瘤的发生、发展和衍化等问题的进一步认识。
患者使用免疫治疗后出现了严重的免疫相关反应,经及时的积极处理后,度过了生命危险。此时,虽然停用了TTFields和免疫治疗,通过降低靶向药物和贝伐珠单抗剂量,以及姑息性的立体放射治疗,经历了一段较长时间的稳定。这与免疫相关反应发生前同样的治疗,效果差异较大;即使停用了TTFields后,肿瘤也没有出现术后早期的快速复发,不排除机体已产生对肿瘤的免疫记忆,帮助杀伤肿瘤,减少肿瘤的免疫逃逸。这个问题值得我们思考。
回顾整个病例,从影像学和基因检测结果均提示预后极差,但临床医生根据最新的循证医学证据,极有代表性地阐释了如何个体化使用放疗、化疗、TTFields、靶向治疗和免疫治疗相结合的综合治疗手段,为患者“与瘤共存”带来曙光。
这是一例左顶叶原发性胶质母细胞瘤的患者,各项分子指标提示预后很差:1.IDH野生型;2.TERT启动子突变;3.MGMT非甲基化。从患者后续的治疗也可以看到治疗过程曲折,疗效反复,多次复发并出现颅内多灶播散。在整个治疗过程中,临床医生根据最新的循证医学证据,积极尝试了靶向、免疫等联合治疗方案,最终达到21个月的OS,优于历史数据的中位值。
但回顾这个病例,有几个问题值得我们思考:1.患者虽然使用了TTFields,是否因佩戴有效时间不足影响了疗效的进一步发挥;2.根据基因检测结果使用了西妥昔单抗,带了明显的皮疹副作用,影响了TTFields的佩戴使用,因此,出现这种情况,该如何权衡治疗方案的选择;3.免疫治疗引起的皮疹发生率不低,在前期出现靶向治疗相关性皮疹后,采用免疫及靶向联用,会否增加皮疹发生率及严重程度?
由于EF14的优秀结果,TTFields已经成为了胶质瘤辅助治疗的一线方案,我们期待能有更多的真实世界数据告诉我们在联合使用TTFields的时候,如何能够更好的提高患者的依从性,减轻相关毒副作用,如何更好的与现有的靶向治疗、免疫治疗相结合,为患者带来进一步生存的提高。
专家简介

医学博士,教授,主任医师,博士生导师
中山大学附属第三医院神经外科学科带头人,垂体瘤诊治中心主任
中国医师协会神经内镜医师培训基地主任
广东省医学会神经外科学分会侯任主任委员
中国医药教育协会-神经内镜与微创医学专委会副主任委员
中国研究型医院学会神经微侵袭治疗专业委员会常务委员
广东省医学会神经外科分会神经内镜学组组长
国家自然科学基金评审专家
长期从事显微外科和神经内镜治疗各种神经外科疾病,致力于颅内病变精准定位、术中神经功能监测、个体化术前手术设计等现代微创理念和技术的推广。
主持国家、省部级医学科研基金10余项,总经费600余万元。发表论著60余篇,其中SCI收录40余篇,主编及参编著作3部。培养亚专科骨干10余人,培养博士及硕士40余人。
研究方向:精准神经外科技术(包括临床医学、生物医学大数据、人工智能、机器人)研发和应用;神经损伤修复和再生。

广东省人民医院放疗科主任医师,行政主任,博士及博士后合作导师
广东省医学会神经肿瘤分会常委
广东省医师协会放射肿瘤分会委员
中国医药教育学会放射肿瘤分会委员
广州市医师协会放射肿瘤分会常委
从事放射肿瘤学临床、教学和科研工作10余年,在中枢神经系统肿瘤的临床诊断、放射治疗尤其是精准放疗以及综合治疗方面有着丰富的临床经验。主要研究方向为:放射性神经损伤发生机制及临床防治,影响肿瘤辐射敏感性的分子机制。2014年至今主持国家自然基金4项、省级课题3项。为国家自然科学基金及广东省自然科学基金函审专家。研究成果发表于CNS Neuroscience & Therapeutics、 Mol Neurobiol、Cell DeathDisease 、Nuroscience等SCI期刊

神经外科学博士,硕士生导师,中山大学附属第三医院神经外科副主任医师,现任广东省医学会神经肿瘤学分会副主任委员,广东省抗癌协会神经肿瘤专委会青委常务委员,广东省中医药学会神经损伤与修复专业委员会常务委员,广东省医学会神经外科学会神经肿瘤学组委员,广东省医师协会神经外科分会委员,欧美同学会医师协会神经肿瘤分会委员,广东省生物医学工程学会医疗机器人与人工智能分会委员。
主要从事颅内肿瘤的基础和临床研究,综合手术、放疗、化疗、肿瘤电场治疗、靶向治疗和免疫治疗等前沿治疗手段,尤其对胶质瘤积累了较丰富的临床经验,2015年赴美国访问学习,从事胶质瘤的基础实验研究。目前围绕胶质瘤的相关研究,在国际知名SCI期刊发表论文12篇,国内核心期刊发表论文10余篇,主持3项省部级科研项目和中山大学5010临床研究,获批专利3项。




