提示
前言
浙大二院神经外科成立功能神经外科亚专科还比较年轻,但发展很快。在难治性癫痫的诊治、帕金森氏病的精准治疗方面和神经内科、神经影像、核医学等学科合作,起点高,研究深,成效好。癫痫中心主任是学校从事癫痫基础研究的国内大咖,使得癫痫基础和临床研究能更好地有机结合,取得了很好成果,和学校工科团队合作的脑机接口癫痫诊治临床转化前沿研究上处于国内领先水平。目前功能神经外科由朱君明主任牵头负责。自301期开始系列报道科室功能神经外科亚专业组的相关病例,与同道共享。
病史简介
诊治经过
术后检查
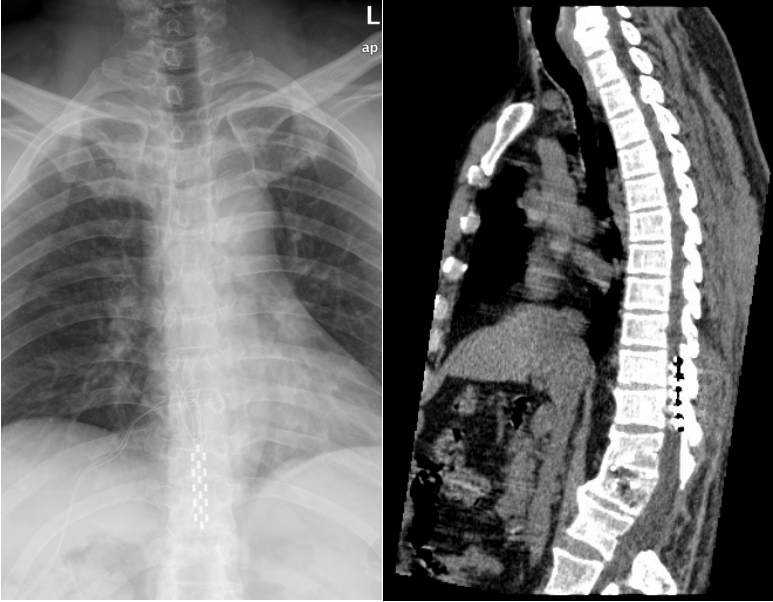
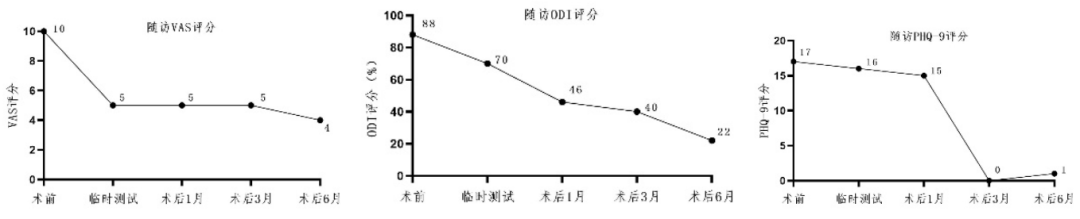
讨论
参考文献
(本文由浙二神外周刊原创,浙江大学医学院附属第二医院神经外科朱周乐博士生整理,朱君明主任医师校审,张建民主任终审)





