2020年12月接诊一例来自吉林的4岁女性患儿(身高:95cm,体重:15kg),主诉:手术后颅骨缺失1年余,要求行颅骨修补。查体:患儿生长发育良好,神清语利,自主体位,右侧颞顶枕部可见手术瘢痕,颅骨缺失面积约10X8cm,骨窗张力中等,头皮略膨隆,余神经系统查体未见明显阳性体征。头颅三维CT显示:右侧颞顶枕去骨瓣术后,右侧颞顶枕脑软化灶形成,局部脑膜脑膨出。
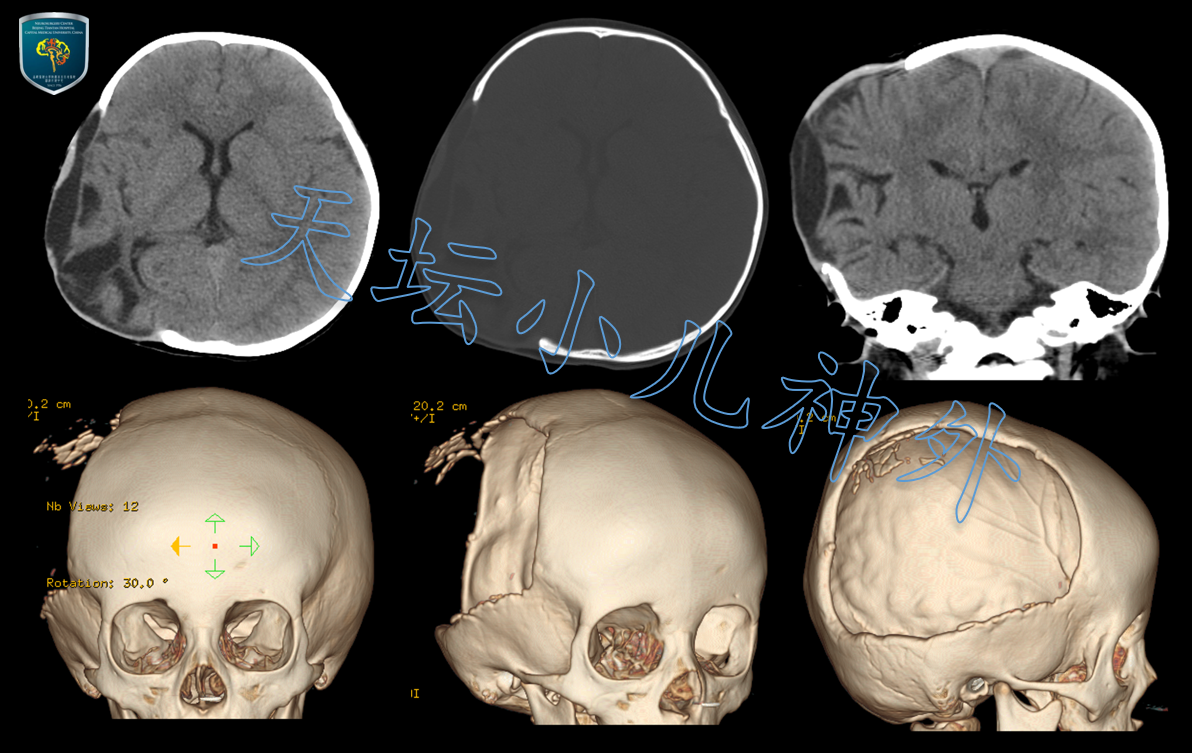
图1:右侧颞顶枕部可见手术后颅骨缺损,局部脑软化灶形成,脑膜脑膨出。
该患儿手术指征明确,于2020年12月24日在全麻下行右侧颞顶枕原切口入路颅骨修补成形术。患儿左侧卧位,右侧颞顶枕原切口开颅,可见颅骨缺损范围约10X8cm,假膜不完整、局部破损,清除部分软化灶,脑组织塌陷满意后,人工硬脑膜修补,将已塑形的PEEK假体嵌入骨窗内,根据事先设计好的固定点,4枚钛片和3枚可吸收颅骨锁将假体固定,手术顺利,塑性后外观满意,术中出血约100ml,未输异体血,术后安返病房监护。

图2:术中显示PEEK假体塑性满意。

图3:术后三维CT显示右侧颞顶枕颅骨缺损区修补成形满意。
患儿术后恢复好,术后十天顺利出院,外貌复原满意,无新增神经系统阳性体征。
治疗体会
儿童颅骨术后缺损、二期异体材料修补术,一个潜在风险是颅骨生长受限,因此,6岁后待颅骨生长基本完成后再行修补时机最佳。6岁前儿童开颅手术时,慎重采用去骨瓣减压术。一旦去除骨瓣,也应较成人减少缺损范围、人工硬膜减张缝合从而保持假膜的完整性、毗邻肌肉尽量还纳贴敷,为二次修补创造便利。颅骨缺损会对儿童造成诸多不利影响,除了头形不美观,由于大脑直接暴露于大气压下,可产生体位性头痛、感觉异常、颅神经麻痹等症状。同时,脑脊液、血流等动力学改变,可出现硬膜下积液、脑代谢降低等问题,严重者影响脑发育1。有报道,进行颅骨修补手术的最小患儿只有4月龄2,据此,我们认为,儿童脑外伤后去骨瓣减压一定要慎重,能不去处尽量不去除;去除后,能修补尽早修补,以减少不必要的继发性损害。
目前临床广泛应用的颅骨修补材料是钛网和PEEK材料。钛网是一种金属合金,具有较高的强度和延展性,不易被腐蚀、不易诱发炎症,感染风险低,且具有良好的美容效果3,缺点是术后可能出现头皮磨损,材料外露,对冷热环境敏感,妨碍磁共振检查等。PEEK(Polyether ether ketone)材料,中文译作聚醚醚酮,是聚芳醚酮(PAEK)家族中的无色有机热塑性聚合物。过去的几十年中,PEEK材料在医学领域广为应用,如牙体植入、体间融合、关节置换、软组织修复等4。2007年,斯坦福大学医学院整形外科学部的Scolozzi首次使用了PEEK材料进行颅骨修补5,一例42岁男性患者先后使用钛网和骨水泥进行颅骨修补,均告失败;采用PEEK假体植入,经一年随访显示重建稳定、无感染,仅遗留颞肌萎缩导致的颞部凹陷持续存在。PEEK材料具有良好模拟骨骼机械特性、不传导热量、坚固耐用、磁共振成像无伪迹等一系列优质特性;术后感染是颅骨修补常见并发症,4.8%的患者需要去除修补材料6,PEEK材料的又一显著优势是,即使发生术后感染,依旧能够取出假体灭菌后择机再次使用7-9。
儿童较成人头皮、肌肉明显薄弱,PEEK假体植入后易形成皮下积液,若感染严重可导致手术失败。美国犹他州立大学第一儿童医学中心的Bowers等对28例患儿颅骨修补PEEK植入进行了研究,因感染失败率为21%10;梅奥诊所Abu-Ghname等人的一项系统回顾中描述,儿童颅骨修补PEEK植入的失败率为19.3%11。因此,采用PEEK材料进行颅骨修补,对手术医生临床经验要求极高,术中要尽量保证皮下游离时头皮厚度、假膜的完整、假体植入的牢靠固定、减少假体毗邻空间的死腔,围手术期引流的应用及有效抗炎,从而确保手术成功。
近年来,清华大学崔福斋团队尝试制备与天然矿化胶原成分结构相似的仿生材料,具有良好的组织相容性和成骨活性,引导骨再生、修复骨缺损12。目前,该材料已应用于长肢骨缺损重建、牙槽骨吸收重建,因其优秀的仿生学特性,有可能成为未来儿童颅骨修补的理想材料。
参考文献
1. Honeybul, S. Neurological susceptibility to a skull defect. Surgical neurology international 5, 83, doi:10.4103/2152-7806.133886 (2014).
2. Grant, G. A. et al. Failure of autologous bone-assisted cranioplasty following decompressive craniectomy in children and adolescents. Journal of neurosurgery 100, 163-168, doi:10.3171/ped.2004.100.2.0163 (2004).
3. Shah, A. M., Jung, H. & Skirboll, S. Materials used in cranioplasty: a history and analysis. Neurosurgical focus 36, E19, doi:10.3171/2014.2.FOCUS13561 (2014).
4. Lu, B., Wang, J., Guo, Y. & Chen, S. Medical applications of polyether ether ketone. Translational Surgery 3, doi:10.4103/ts.ts_3_18 (2018).
5. Scolozzi, P., Martinez, A. & Jaques, B. Complex orbito-fronto-temporal reconstruction using computer-designed PEEK implant. J Craniofac Surg 18, 224-228, doi:10.1097/01.scs.0000249359.56417.7e (2007).
6. Zhang, J. et al. The application of polyetheretherketone (PEEK) implants in cranioplasty. Brain Res Bull 153, 143-149, doi:10.1016/j.brainresbull.2019.08.010 (2019).
7. Morrison, C. et al. In vitro biocompatibility testing of polymers for orthopaedic implants using cultured fibroblasts and osteoblasts. Biomaterials 16, 987-992, doi:10.1016/0142-9612(95)94906-2 (1995).
8. Wenz, L. M., Merritt, K., Brown, S. A., Moet, A. & Steffee, A. D. In vitro biocompatibility of polyetheretherketone and polysulfone composites. Journal of biomedical materials research 24, 207-215, doi:10.1002/jbm.820240207 (1990).
9. Jockisch, K. A., Brown, S. A., Bauer, T. W. & Merritt, K. Biological response to chopped-carbon-fiber-reinforced peek. Journal of biomedical materials research 26, 133-146, doi:10.1002/jbm.820260202 (1992).
10. Bowers, C. A. et al. Minimizing bone gaps when using custom pediatric cranial implants is associated with implant success. Journal of neurosurgery. Pediatrics 16, 439-444, doi:10.3171/2015.2.Peds14536 (2015).
11. Abu-Ghname, A. et al. Outcomes and Complications of Pediatric Cranioplasty. Plastic and Reconstructive Surgery 144, 433e-443e , doi:10.1097/prs.0000000000005933 (2019).
12. Qiu, Z.-Y., Tao, C.-S., Cui, H., Wang, C.-M. & Cui, F.-Z. High-strength mineralized collagen artificial bone. Frontiers of Materials Science 8, 53-62, doi:10.1007/s11706-014-0237-9 (2014).





