![]()
《World Neurosurgery》杂志2021年5月11日在线发表韩国首尔Seoul National University Hospital,的Hangeul Park , Sang Soon Jeong , Hyun-Tai Chung ,等撰写的《与接受伽玛刀治疗的三叉神经痛患者远期预后相关的治疗计划因素。Treatment planning factors associated with long-term outcomes of Gamma Knife surgery in patients with trigeminal neuralgia 》(doi: 10.1016/j.wneu.2021.05.008.)。

目的
伽玛刀放射外科治疗(GKS)是一种确定性的三叉神经痛(TN)的治疗选项。然而,GKS对TN患者的长期疗效尚未得到充分研究。本研究的目的旨在评估GKS治疗后疼痛控制的顺序过程,并分析与长期镇痛效应相关的因素,重点关注放射剂量学和神经血管冲突(NVC)因素。
方法
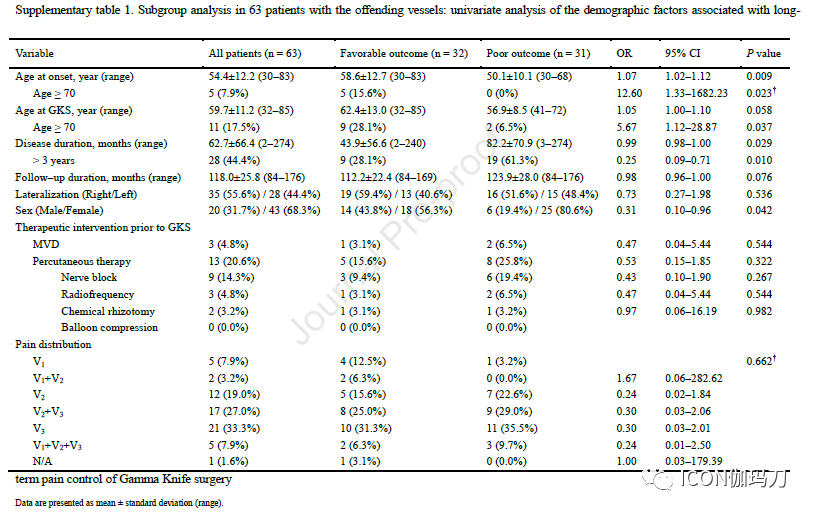
我们分析了2005年至2013年在我们医院接受GKS治疗随访时间>7年的83例TN患者。增加药物治疗的可耐受疼痛、持续性顽固性疼痛和复发被归类为不良结果,其他结果被归类为良好结果。我们分析了NVC与靶区之间的剂量学因素和位置关系与良好结果的相关性。
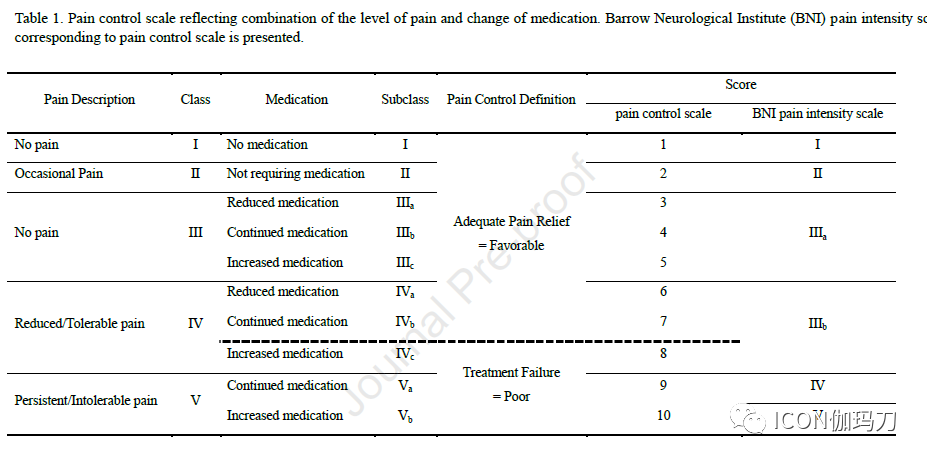
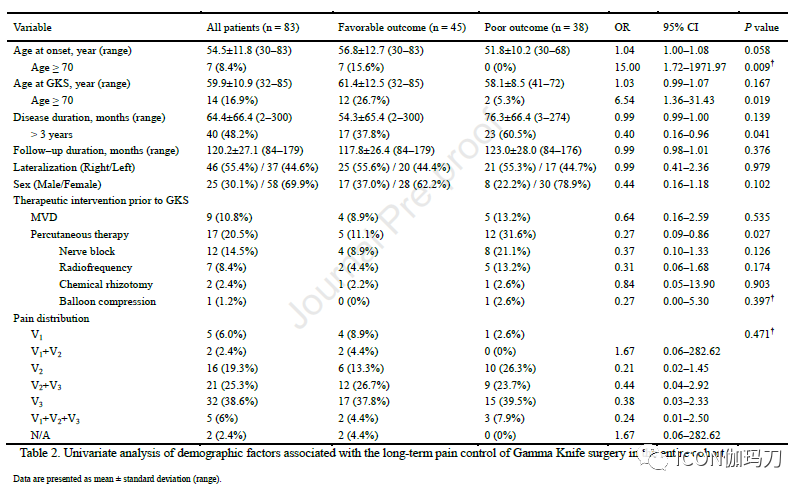
GKS使用Leksell伽玛刀(瑞典斯德哥尔摩Elekta AB公司生产的)C型(n = 29)或Perfexion 型(n = 54)进行。所有患者接受磁共振(MR)成像,包括1.5毫米层厚T2加权,1.5毫米层厚T1加权,和1毫米层厚对比增强T1加权序列,240x240的视野和矩阵大小256x256,识别三叉神经(CN V)并进行放射外科治疗的计划。采用Leksell GammaPlan (Elekta Instrument AB)系统制定治疗方案。我们针对76例患者的REZ区和对7例患者的半月神经节后根(retrogasserian)区,处方以中位最大剂量80Gy(范围80-85 Gy)。
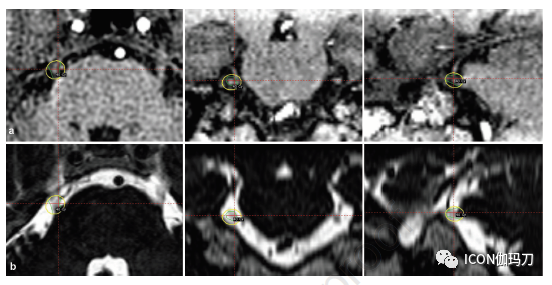

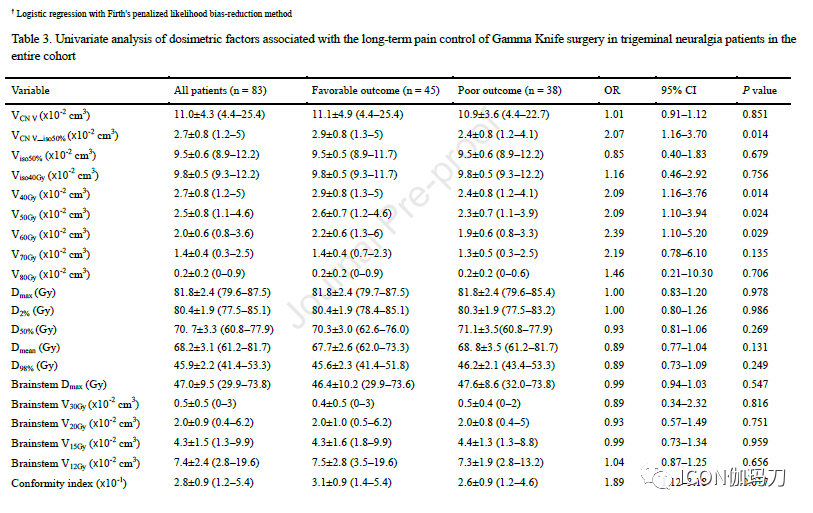
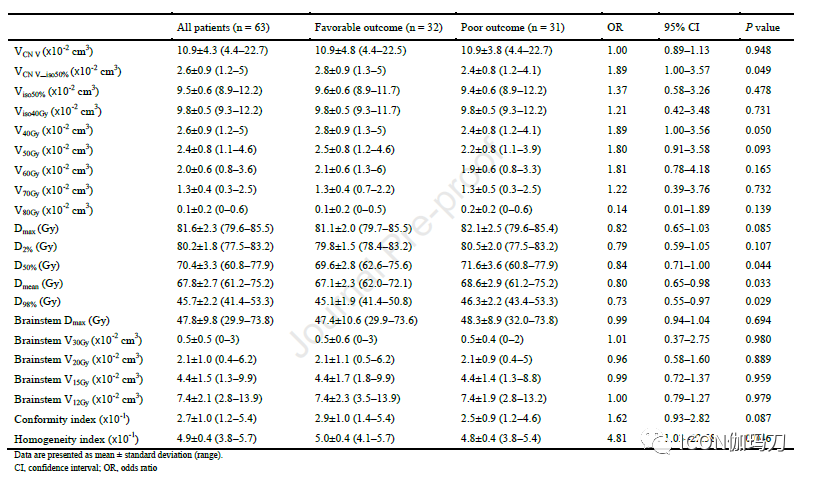
对从REZ到Meckel腔的三叉神经(CN V)、在50%等剂量线内的三叉神经(CN )V和脑干进行勾画,并从Leksell GammaPlan中提取辐射剂量学数据,参数如下:体积VCN V (CN V体积), VCN V_iso50% V (50%等剂量线内CN V的体积),Viso50%(50%等剂量线体积),Viso40Gy (40 Gy等剂量线体积), CN V的Dmax,D2% D50%, Dmean, D98%, V40Gy, V50Gy, V60Gy, V70Gy,和V80Gy以及脑干的距离,V12Gy, V15Gy, V20Gy, V30Gy。用下列公式计算适形性指数和均匀性指数:
适形性指数= 50%等剂量线内CN V的体积/50%等剂量线内CN V的体积;
均质性指数=(D2-D98)/D50
结果
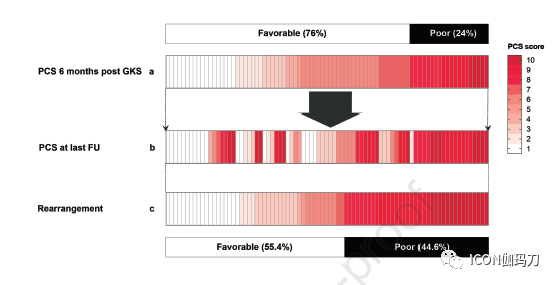
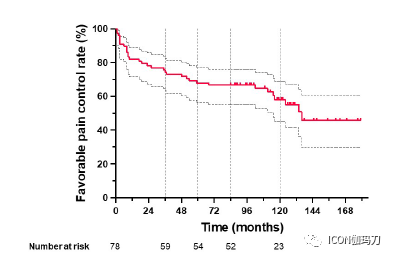
93%的患者在GKS治疗后1个半月疼痛得到了充分的缓解,但41.5%的患者在治疗后平均36个月疼痛复发。较大的V40Gy (P = 0.002)和较高的同质性指数(P =0.027)与长期良好的预后显著相关。大约40%的患者有多个NVC位点(sites),而NVC在靶区包含不足(insufficient inclusion)与长期不良预后显著相关(P =0.002)。







讨论
神经血管冲突在三叉神经痛发病机制中的意义
经典TN的阵发性电休克样疼痛或刺痛是三叉神经痛(CN V)兴奋过度(hyperexcitation)的结果。据认为,在三叉神经的发病机制中至关重要的,是在80 - 90%的患者中常见神经血管冲突(NVC)。三叉神经的组织病理学研究表明,在神经束的周围有一个边界清楚的脱髓鞘轴突。连续血管的慢性压迫可导致神经纤维缺血,妨碍维持神经完整的有效能量供应,导致神经鞘脱髓鞘,偶尔发生轴突变性。随后,紧密相联的脱髓鞘轴突能允许无害的刺激(closely apposed stripped axons allow innocuous stimuli),如通过感受器传递的神经冲动,轻触触发剧痛(light touch totrigger excruciating pain, through the ephaptic transmission of nerve impulses )。受损的神经纤维引起炎症,炎症细胞因子激活神经元中的一系列信号通路,导致离子通道和各种受体等功能蛋白在细胞内不适当的过度合成。在脱髓鞘的轴突的轴突膜中,电压门控Na+和机械敏感离子通道的表达显著升高。上调的Na+通道簇包括一些具有低阈值的同构体被认为在容易产生异位传导电位中起主导作用(Uspangulated Na+ channel clusters including some isoforms with a low threshold are thought to play a leading role in readily generating ectopic actional potentials)。
GKS在TN中的作用机制
尚未完全阐明GKS的作用机制。最主要的假设是GKS可能通过消融机制影响TN,阻断通过受损的CN V 的病理传导。实验研究表明,电离辐射以剂量依赖的方式促进神经传导的消除,电离辐射引发的Na+通道的结构或功能破坏被认为是介导这一现象的原因。Schwarz和Fox报道了6-10 kR (52.6-87.7 Gy)剂量x射线照射后神经膜的钠峰值电流下降,而钾电流变化不大。同时,利用非人类灵长类动物进行的组织学研究表明,对完整的CN V进行80Gy或100Gy的放射外科会导致神经局灶性损伤,其特征是水肿、脱髓鞘、轴突变性(80Gy)和坏死(100Gy) 。人类组织病理学研究从接受放射外科治疗的TN患者的根毁损术标本中也发现了神经纤维纤维化和髓鞘异常,以及轴突变性。基于这些发现,我们推测GKS在一定程度上诱导神经纤维变性,这有助于阻断病理性神经传导。
同时,利用非人类灵长类动物进行的组织学研究表明,对完整的CN V进行80Gy或100Gy的放射外科会导致神经局灶性损伤,其特征是水肿、脱髓鞘、轴突变性(80Gy)和坏死(100Gy) 。人类组织病理学研究从接受放射治疗的TN患者的根毁损术标本中也发现了神经纤维纤维化和髓鞘异常,以及轴突变性。基于这些发现,我们推测GKS在一定程度上诱导神经纤维变性,这有助于阻断病理性神经传导。
同时,也可以假设放射外科也会影响责任血管(offending vessels)。GKS可能通过诱导血管壁纤维化缓解疼痛,从而降低血管搏动,防止去甲肾上腺素从血管壁渗漏,或者改变TN的神经血管结构,从而缓解NVC 。GKS减轻了大部分患者的TN,但没有引起面部感觉异常 ,这表明辐射可能会选择性地阻断神经传导,而不是造成完全的神经麻痹。最被接受的假设是,脱髓鞘的轴突通过上调的Na+通道作为一个自主的超兴奋起搏器,对辐射诱导的传导阻滞比未受损的轴突更敏感 。也就是说,一般认为GKS剂量不足以抑制正常的轴突传导,但足以阻断异常轴突的过度兴奋。此外,鉴于不同亚型的神经纤维对传导阻滞有不同的辐射阈值,可想而知,携带疼痛感觉的直径较小的A�和C纤维相比高速传递触觉和本体感受信号的直径较大的A�和A�纤维可能有更容易传导阻滞的较低的辐射剂量阈值。这个假设需要用实验来证实。最后,值得注意的是,部分感觉神经根毁损术,即使达到50%或以上,可以在很大程度上保留CN V 的感觉功能的同时减轻疼痛。这意味着CN V有足够的储备纤维来替代感觉纤维受损,只有当相当比例的感觉纤维被破坏时,感觉丧失才会发生。
以神经血管冲突部位为靶区
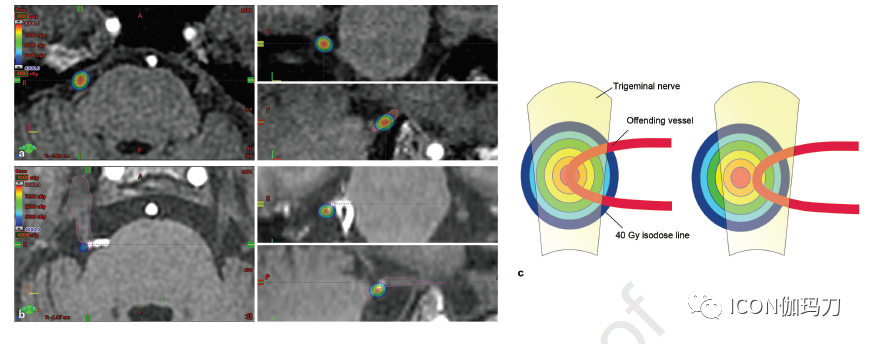
三叉神经感觉REZ区常被用作GKS治疗TN 的靶点。REZ区是许旺细胞形成的外周髓鞘转变为少突胶质细胞形成的中央髓鞘的过渡区。中央髓鞘易因慢性压迫而受损,组织病理学研究报道,中央髓鞘轴突发生脱髓鞘。此外,在REZ经常观察到有责任血管。由于这些原因,REZ已经成为GKS治疗TN 的一个概念性目标。然而,Jannetta和他的同事从他们的4400例MVD手术中断言,从脑桥的软膜表面到Meckel腔的过渡区长度可以不同。此外,其他研究表明,REZ区并不是NVC的唯一位置,38%的病例中发现了多根责任血管。Sindou等人报道了579例TN患者的MVD手术,发现冲突部位位于REZ区的占52%,位于脑池中段的(mid-cisternal segment)占54%,近岩骨段(the juxta-petrous segment)占10% 。本研究还显示,38%的患者存在多根冲突血管,且压迫部位不同。NVC诱导神经纤维局灶性脱髓鞘,这在TN的发病和症状产生中是必不可少的,脱髓鞘的轴突更容易受到辐射的影响。考虑到以上事实,GKS的靶区是神经实际上被冲突血管压迫的区域,而不仅仅是理论上的REZ区或半月神经节后部(retro-Gasserian)区域,将有助于提高治疗效果。Sheehan等人报道了NVC剂量增加与接受GKS治疗TN 患者最终疼痛缓解之间的相关性。本研究还表明,靶区内充分包含NVC的区域与长期良好的预后显著相关。同时,虽然VCN V和Viso40Gy在两组之间均无差异(表3),但较差结局组V40Gy更大,同质性指数值更高。这意味着在更多有利的情况下,辐射是通过瞄准CN - V中心对称传递的。将这些结果放在一起,我们认为,将CN V的中心部分定位于NVC部位,可以使更可靠的以高于阈值的剂量均匀照射CN V纤维,从而改善GKS治疗TN的结果。
综上所述,GKS缓解了大多数患者的疼痛,但相当比例的患者在平均3年后疼痛复发。然而,获得长期良好的疼痛缓解与在NVC区域照射CN V中心有关。有必要通过未来的前瞻性研究来验证本研究的结果。这些结果是基于一个小样本量的回顾性研究。由于我们处方的最大剂量范围很窄(即80-85 Gy),我们无法在患者中发现剂量反应。同时,我们也不能明确靶向NVC对GKS后面部麻木的影响,以及靶向NVC时是否需要调整剂量。需要未来的前瞻性和大规模研究来验证NVC靶向治疗GKS对TN患者的有效性和安全性。
结论
GKS以三叉神经中心为靶点,在GKR治疗NVC区有较好的长期镇痛效果。




