CD31是一种在血小板、白细胞和内皮细胞上专一表达的跨膜糖蛋白类受体,参与内皮功能和维持血管内稳态。因此,CD31仿生多肽可能是增强血流导向装置覆盖处动脉壁新生、预防支架引起的炎症和血栓形成的理想材料,本研究评估CD31仿生涂层的血流导向装置对置入处血管内皮化的潜在益处。
——摘自文章章节
【REF:Cortese J, et al. Stroke. 2021;52(2):677-686. doi:10.1161/STROKEAHA.120.030624】
研究背景
血流导向装置(FDs)在完成动脉瘤闭塞时,金属材料的异质性,可引起体内血管的不良反应,使得动脉瘤颈的内皮化和颅内动脉瘤愈合变得十分困难。血流导向装置术后的动脉瘤闭塞失败可导致围手术期并发症发生和死亡率为7.1%,其发生原因可能有动脉瘤内血栓的蛋白分解活性、动脉瘤血流的持续性,以及金属支架固有的炎症反应。此外由于栓塞并发症的风险,在血流导向装置植入前必须进行双重抗血小板治疗,这增加了出血并发症风险。在实际应用血流导向装置后因抗血小板药物使用不当可导致危及生命的缺血性或出血性并发症发生,从而限制了其使用范围和适应症。CD31是一种在血小板、白细胞和内皮细胞上专一表达的跨膜糖蛋白类受体,参与内皮功能和维持血管内稳态。因此,CD31仿生多肽可能是增强血流导向装置覆盖处动脉壁新生、预防支架引起的炎症和血栓形成的理想材料,本研究评估CD31仿生涂层的血流导向装置对置入处血管内皮化的潜在益处。
研究方法
首先,在体外通过评估血液成分和内皮细胞与CD31仿生涂层金属盘接触后的反应;随后,为了分析体内真实血流导向装置覆盖处内皮化和新动脉壁的形成,我们将CD31涂层血流导向装置植入与人体病理组织学、形态学、生物学和血液动力学相似的兔动脉瘤模型中。镍钛合金血流导向装置(Silk Vista Baby)和对照金属盘分别浸染CD31仿生肽和聚多巴胺涂层,用平板法评价血管内皮细胞和血液中各成分与异物接触后的体外反应。在兔动脉瘤模型上,比较CD31仿生物(n=6)、聚多巴胺(n=6)和无涂层血流导向装置(裸露,n=5)植入后4周动脉壁的反应,同时在12周时对其长期安全性进行评估。具体采用组织化学、免疫荧光和多光子分析技术。
研究结果
体外实验表明,与聚多巴胺和裸露镍钛合金盘对照组相比在CD31仿生涂层金属盘上红细胞和血小板明显减少,几乎看不见。3组的粘附EC密度相似,但CD31仿生物上CD31和VE-钙粘附素的密度显著高于聚多巴胺和裸表面。
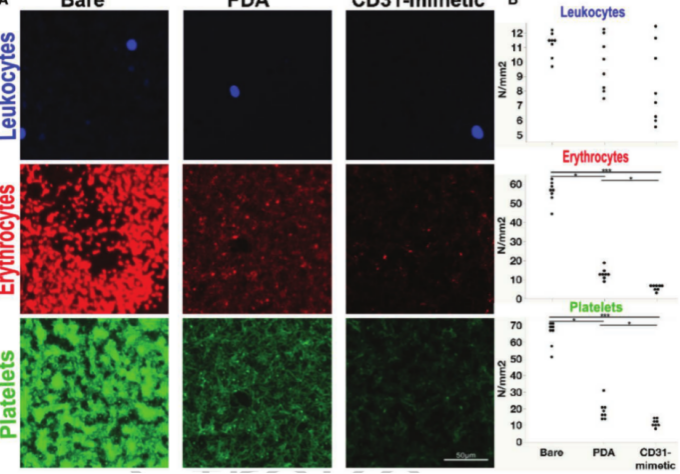
图1. 不同涂层材料金属盘的生物相容性体外试验荧光显微图。于37°C全血中孵育1小时后,裸露金属支架,聚多巴胺(PDA)和CD31仿生的镍钛合金盘片的代表性荧光显微照片。A、绿色荧光:粘附的血小板(CD41/CD63)。红色荧光:粘附的红细胞(糖蛋白A)。蓝色荧光:白细胞。B、白细胞,红细胞和血小板的定量显示。

图2. 内皮细胞恒温培育48小时后的定量自动分析结果。裸露金属,聚多巴胺(PDA)和CD31仿生的镍钛合金盘的代表性荧光显微照片。绿色荧光:CD31。红色荧光:VE-钙粘附素。蓝色荧光:4’,6-二氨基-2-苯基吲哚(DAPI)。第一排:低倍率。第二排:高放大倍率。B,DAPI、VE-钙粘附素和CD31的定量分析。
动物试验中,先制作不同大小的动脉瘤,不同的支架植入后行血管造影随访。在体外,与裸金属支架和多巴胺涂层盘块相比,CD31仿生涂层显示出对血液各成分的粘附性降低,同时有利于内皮细胞的粘附和融合再生。值得注意的是,位于动脉瘤颈部CD31仿生涂层血流导向装置上形成的新生动脉壁具有动脉中层的特征,与对照组相比,连续完整分化的内皮细胞下方拥有明显的厚胶原层和平滑肌细胞。3组血管造影动脉瘤完全闭塞率和支架覆盖处动脉通畅率均相似。
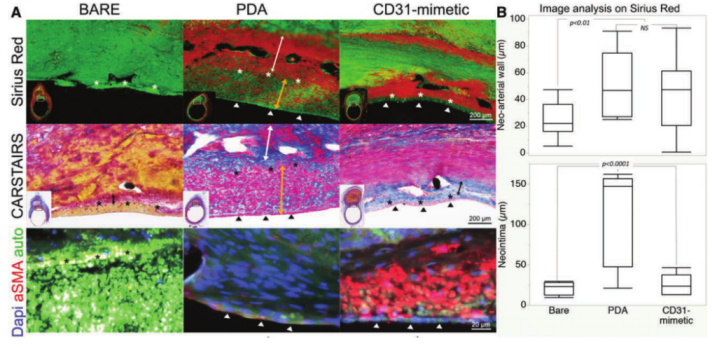
图3. 术后4周闭塞动脉瘤颈的新生动脉壁和新生内膜进行不同染色的代表性组织切片定性和定量分析图。A.顶部图:胶原蛋白(红色)。绿色是自发荧光。3种情况下,星号标志着富含ECM(细胞外基质)层的管腔界限(比如,新生动脉壁的内弹力层)。在聚多巴胺(PDA)和CD31仿生涂层的情况下,箭头指向动脉管腔内连续的内皮细胞(见中)。中间图:卡斯特拉斯染色结果。橙红色显示裸露金属状态下的纤维蛋白和红细胞。在聚多巴胺PDA和CD31仿生涂层的情况,动脉壁内侧的粉红色细胞层(箭头如上图)提示存在连续的内皮细胞。蓝色显示胶原蛋白/细胞外基质。底部图:在仿生涂层CD31的情况下,新生内膜中的粉红色显示平滑肌细胞。免疫荧光检测显示ASMA(α平滑肌肌动蛋白)分布在平行于动脉壁的纤维之间。内皮细胞层与这些细胞直接接触,没有新生内膜。相反,在PDA样本中,最内侧细胞层的粉红色显示大量ASMA阴性的间充质细胞,表明较厚的新生内膜形成。B.3种情况下动脉瘤颈处的新动脉(顶部)和新内膜(底部)厚度定量分析。
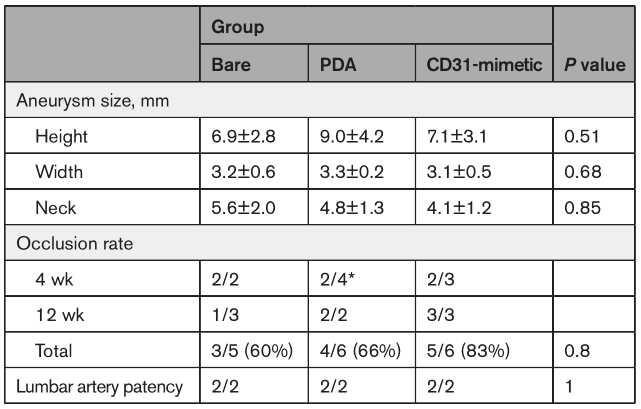
用基于二次谐波信号、胶原纤维定量和胶原纤维弥散分析的多光子显微图结果显示:兔主动脉内置入血流导向装置后4周,CD31仿生组的ECM厚度与对照组相比显著增加。三组诱发动脉瘤大小相同(表1)。裸瘤组、聚多巴胺组和CD31仿生组的1级闭塞率分别为3(60%)、4(66%)和5(82%),其余动脉瘤均未行3级栓塞。在聚多巴胺组,2个支架在4周时自发闭塞。所有其他载瘤动脉、椎动脉和腰动脉保持通畅,无狭窄。
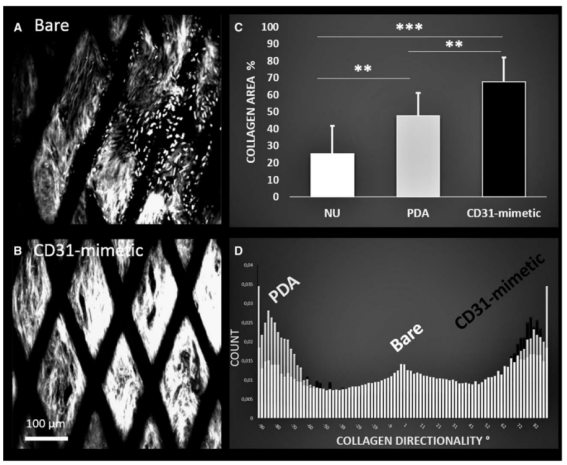
图4. 在兔主动脉内置入血流导向装置4周的多光子显微图片对比图。A、裸露金属支架。B、CD31仿生涂层支架。C、CD31仿生涂层和聚多巴胺涂层支架的胶原细胞外基质(细胞外基质)厚度均大于裸金属支架,CD31仿生涂层支架的胶原率最高。D、胶原纤维分散性测量显示,与裸金属支架相比,CD31仿生涂层和聚多巴胺涂层支架的纤维分散性总体较低。
表1. 动物动脉瘤大小(mm,Mean±SD)和血管造影随访结果
研究结论
CD31仿生涂层有利于血管内金属装置的定植,内皮细胞表现出完全正常的生理表型,同时防止血小板和白细胞的粘附。这些生物学特性导致动脉瘤颈处新生动脉壁的内皮化迅速改善。因此,CD31仿生涂层可以提高血流导向装置的生物相容性,并促进动脉瘤的有效愈合。这些结果是其转化为临床应用的关键一步。





