
该研究旨在为成人UIA的处置提供参考因素;并通过回顾UIA及患者特征对比手术夹闭与血管内治疗的利弊;最后基于PHASES评分提出一种新颖、简单、实用的方法用于UIA的干预决策,报道如下。
——摘自文章章节
【REF: Vikram A. Mehta, et al. Neurosurgical Review. 2020 Oct 06. doi:10.1007/s10143-020-01407-y】
未破裂颅内动脉瘤(UIA)的发病率占人口总数的3-5%。近年来随着CT和MRI的普及应用,意外检出UIA不断增多。对于医患双方,UIA的处置均颇具挑战,因为需要权衡UIA破裂和蛛网膜下腔出血(SAH)与手术夹闭或血管内治疗的风险。此外其它因素,包括患者对于UIA破裂的焦虑也在决策中发挥重要作用。该研究旨在为成人UIA的处置提供参考因素;并通过回顾UIA及患者特征对比手术夹闭与血管内治疗的利弊;最后基于PHASES评分提出一种新颖、简单、实用的方法用于UIA的干预决策,报道如下。
UIA的组织病理学特点是内膜弹力层缺失,内膜和中膜组织结构破坏。家族性UIA或常染色体显性遗传性多囊肾病家族史均增加UIA发病率。UIA的发病率在女性和40岁以上人群呈上升趋势。高血压病或吸烟均增加UIA的发病率。UIA最常见于颅内动脉连接/移行部位。大多数UIA位于前循环,最常见于前交通动脉(Acom)与大脑前动脉(ACA)连接处。其它常见部位是颈内动脉(ICA)与后交通动脉(Pcom)连接处和大脑中动脉(MCA)分叉处。后循环的UIA最常见于基底动脉尖部。
UIA通常保持长期稳定,并且大多数UIA罕见破裂。然而,UIA出现不规律快速增长时,其破裂和引起SAH的风险相应增加。业已明确影响UIA生长和破裂的因素有高血压病、吸烟、女性和UIA的特征(例如UIA的大小、位置和形态)。自发性SAH的发病率为每年每100,000人6-10例,大多数由UIA破裂导致(aSAH),aSAH预后较差,约10-15%的患者在入院前死亡。因而预防aSAH是UIA处置的重要目标。
ISUIA和UCAS是关于UIA自然病史的两项大型前瞻性研究。表1总结了ISUIA研究中UIA 5年累积破裂率和UCAS研究中UIA年破裂率。两项研究发现UIA破裂风险与其大小呈正相关。直径小于7mm的UIA破裂风险较低(ISUIA为0.00-2.50%,UCAS为0.36-0.50%)。此外,ISUIA发现相比后循环UIA,前循环UIA破裂风险较低。而UCAS发现相比MCA的UIA,Acom和Pcom UIA破裂风险较高。
表1. ISUIA和UCAS中根据UIA的大小和位置报告UIA破裂率
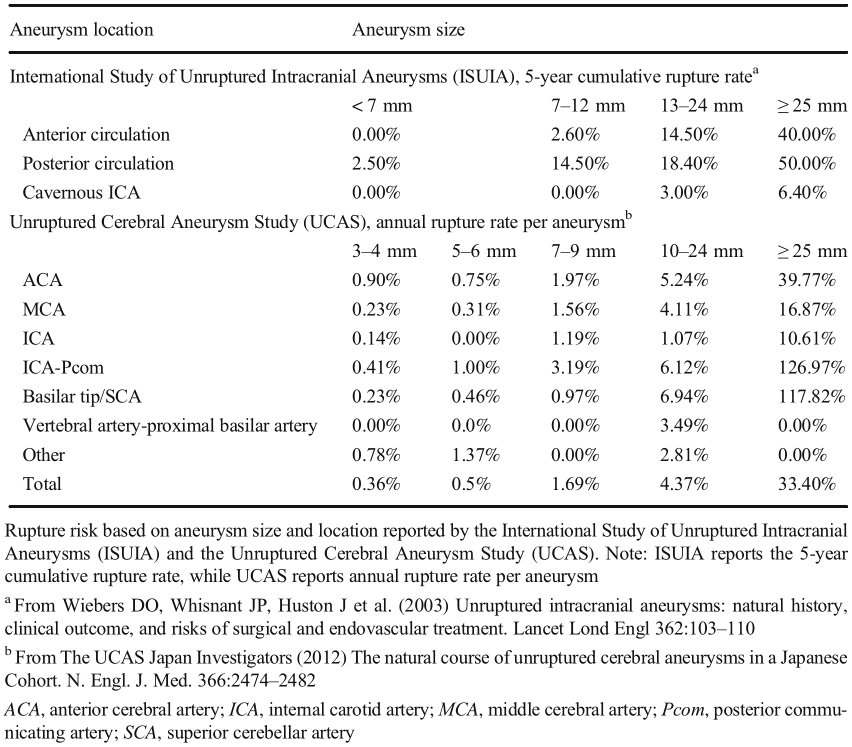
根据ISUIA、UCAS和其它研究的数据进行荟萃分析开发的PHASES(人口、高血压病、年龄、大小、早期SAH和部位)评分可用于预测UIA破裂风险(表2)。PHASES评分未纳入的其它危险因素包括SAH家族史、吸烟、血流直接流入和形态不规则,尤其是存在子瘤。
表2.PHASES评分预测UIA破裂风险

UIA的干预决策除了预防aSAH,还应最大程度地延长患者的质量调整生命年。一般而言,手术夹闭和血管内治疗的并发症发生率分别为8%和5%。因此小型(直径小于5-7mm)、无症状、位于前循环的UIA可保守治疗,连续影像随访,这尤其适用于危险因素较少的老年患者,这些患者(>70岁)终生累积破裂风险较低。而对于无症状的年轻患者(≤50岁)终生累积破裂风险较高,可以考虑更加积极的治疗。此外,对于有子瘤或形态不规则的小型UIA,或者有两个以上直系亲属有SAH家族史的患者,可以考虑积极治疗。对于>12mm的UIA建议积极治疗。而对于7-12mm的UIA需要根据具体情况处置。在UIA的处置中倾向于观察的因素参见表3。
表3. 在UIA的处置中倾向于观察、手术夹闭和血管内治疗的因素

PHASES评分<3的UIA破裂风险较低,可随访观察;PHASES评分>4的UIA破裂风险较高,应尽早干预(表4)。而PHASES评分为3和4的UIA尚不明确如何处置。该研究根据PHASES评分提出了一种新的方法用于UIA的干预决策(图1)。
表4. 根据PHASES评分预测UIA生长的风险
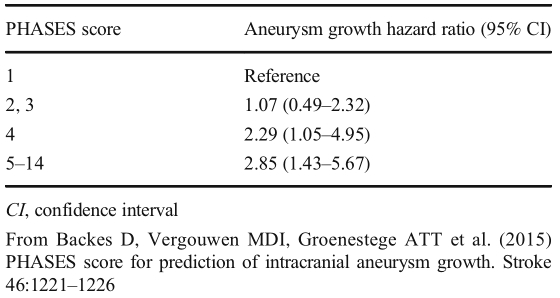
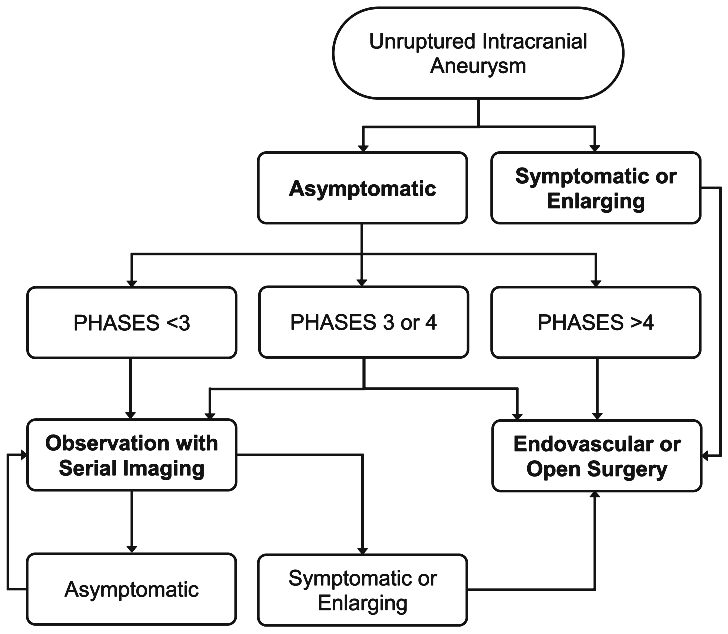
图1. 用于UIA处置决策(观察与积极治疗)的方法。
手术夹闭与血管内治疗比较
手术夹闭UIA疗效确切,而血管内治疗则具有微创的优势。除了考虑治疗相关的并发症发生率和死亡率,影响UIA干预决策的因素还有但不限于:患者自身因素(例如年龄、合并症和干预后抗血小板治疗的风险);UIA的因素(例如UIA的位置、形态和类型);以及术者的因素(例如经验和舒适度)(表3)。
50岁以上的患者手术夹闭不良结局的风险增加,因此首选血管内治疗。而年轻患者则推荐手术夹闭,因为手术疗效确切、彻底、安全、有效、经济。目前,手术夹闭和血管内治疗UIA 1年的失败率和并发症发生率相近,因此可根据术者经验、个人偏好和可用材料进行选择。
形态复杂的UIA可能更适宜手术夹闭。UIA颈宽和顶颈比是评估能否安全栓塞的重要因素。UIA颈宽≥4mm或体颈比≤1.5mm(即宽颈UIA)不适宜单独栓塞治疗。随着血管内治疗技术的发展,球囊或支架辅助栓塞以及血流导向装置可治疗宽颈UIA。
UIA的可及性是权衡手术夹闭或血管内治疗的重要因素。位于MCA、Acom和Pcom的UIA可通过翼点或眶颧入路手术夹闭。位于MCA的UIA常因为颈宽和形态复杂,血管内治疗较困难。小脑后下动脉(PICA)、小脑前下动脉(AICA)和小脑上动脉(SCA)的UIA手术可及性较好,可通过手术夹闭。而后循环UIA手术夹闭困难,因此更倾向于血管内治疗,特别是基底动脉UIA。海绵窦或床突旁ICA UIA首选血管内治疗。此外,血管迂曲和闭塞是评估能否血管内治疗的重要因素。
血管内治疗UIA若放置支架,术后需要双联抗血小板治疗至少三个月,以预防血栓形成和缺血性脑卒中。因而,如果患者有抗血小板治疗的禁忌症(例如药物不良反应、依从性差或药效差),则不宜行血管内治疗。为评估患者抗血小板治疗效果,可检测血小板功能,但是其效能临床还存在争议。如果抗血小板治疗效果差,可以考虑抗凝治疗,但有增加出血的风险。
对于小型、稳定、无症状UIA可行保守治疗,并通过DSA、CTA或MRA随访观察。UIA增大或出现症状,则破裂风险也相应增加,应考虑手术夹闭或血管内治疗。此外,应控制影响UIA形成和生长的危险因素(例如高血压病和吸烟)以及心血管疾病的危险因素(例如2型糖尿病和高脂血症)。
UIA的处置决策是医患双方在权衡观察过程中UIA破裂出血的风险与积极治疗相关并发症发生率和死亡率的基础上共同制定的。因此,UIA增大时需要积极治疗,尤其是出现神经功能障碍时。该研究基于PHASES评分提出一种新颖、简单、实用的方法用于UIA的干预决策。对于PHASES评分<3的UIA,强烈建议保守治疗,而PHASES评分>4的UIA,推荐手术干预。对于PHASES评分为3和4的UIA尚不明确如何处置。对于无明显增大的UIA需要考虑的因素包括:(1)年龄,年轻患者倾向于积极治疗;(2)UIA的位置,后循环UIA倾向于血管内治疗;(3)UIA的大小,较大的UIA需要积极治疗;(4)UIA的形态,存在子瘤或形态不规则的UIA需要积极治疗;以及(5)患者个人偏好。
☞ 双重抗血小板药物联合新型p64MW HPC血流导向装置治疗前循环未破裂动脉瘤的初步经验





