01
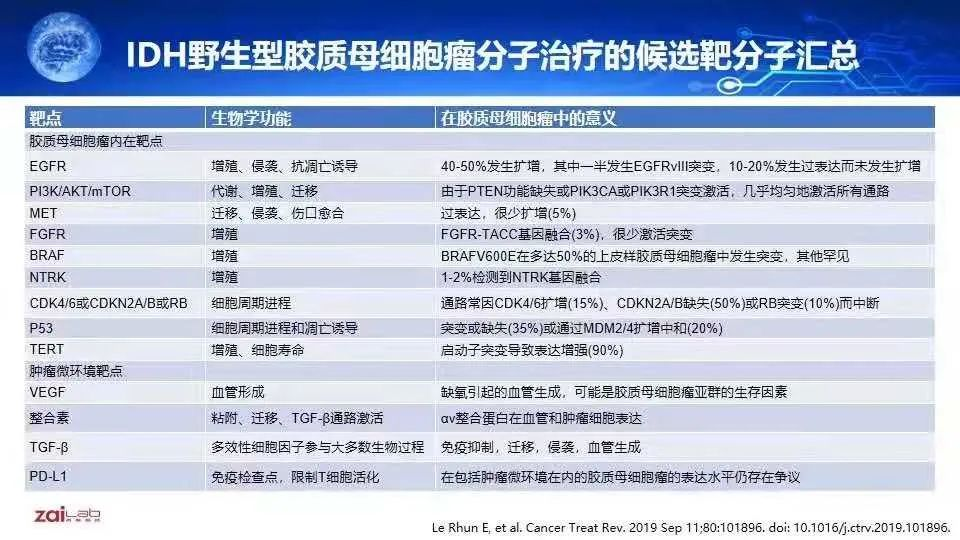
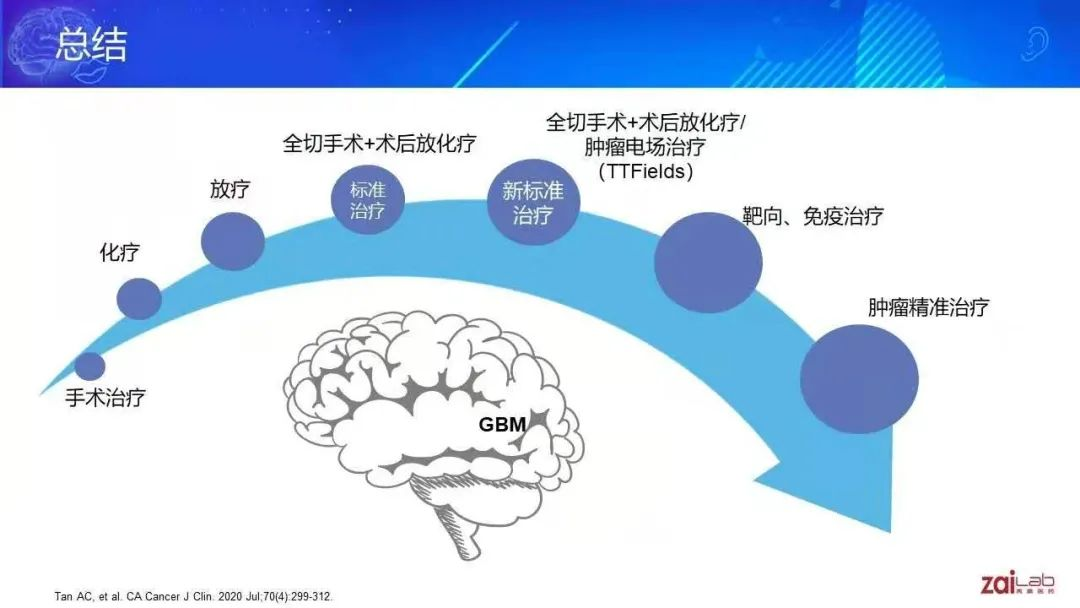
GBM领域最新进展综述
(点击标题即可查看原文)
精彩回顾:
(点击标题即可查看原文)
精彩回顾:
(点击标题即可查看原文)
精彩回顾:

(点击标题即可查看原文)
精彩回顾:

02
肿瘤电场治疗在GBM的进展
(点击标题即可查看原文)
03
手术在GBM中的进展
04
免疫治疗在GBM的进展
05
靶向治疗在GBM的进展

2020年度说文解惑-GBM前沿汇总
01
GBM领域最新进展综述
(点击标题即可查看原文)
精彩回顾:

(点击标题即可查看原文)
精彩回顾:

(点击标题即可查看原文)
精彩回顾:

(点击标题即可查看原文)
精彩回顾:

02
肿瘤电场治疗在GBM的进展
(点击标题即可查看原文)
03
手术在GBM中的进展
04
免疫治疗在GBM的进展
05
靶向治疗在GBM的进展
