神经外科医生都知道三叉神经痛微血管减压术(Microvascular Decompression MVD)是目前治疗三叉神经痛疗效最佳、缓解持续时间最长的方法,那为什么三叉神经痛的首选治疗方法却不是MVD呢?《三叉神经痛诊疗中国专家共识》中给出了答案:“微血管减压术的远期预后优于其他外科方法,但可能承担更严重的风险”。近几年,我科三叉神经痛MVD手术量逐年增多,并取得了很好的治疗效果,但随着MVD手术病例的积累,笔者亦发现在MVD手术中仍存在一些需要改进的地方:比如手术切口和骨窗是否可以更小一些?怎样可以尽可能的避免术后并发症?等等。于是,笔者参考了Jannetta教授名著《三叉神经痛》、《三叉神经痛诊疗中国专家共识》、《三叉神经痛显微血管减压术无效或复发的原因与外科处理》、《Neurovascular Surgery》、《RHOTON颅脑解剖与手术入路》、《Keyhole Approaches in Neurosurgery》等书刊中的相关章节,参考Neurosurgery Greifswald、Microneurosurgery网站以及Penn Neurosurgery网站上的手术视频,制作了本文。
本文将重点介绍三种手术方法:
● 1.显微镜下三叉神经痛MVD锁孔入路
● 2.内镜辅助显微镜下三叉神经痛MVD锁孔入路
● 3.全内镜下三叉神经痛EMVD锁孔入路
由于笔者水平所限,错误之处敬请指正。

三叉神经术中解剖
本文简要介绍MVD术中涉及到的三叉神经解剖:
▼ 1.三叉神经3个分支的相对位置关系:
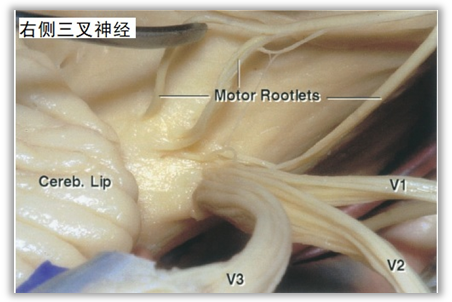
三叉神经感觉根切断术(sensory rhizotomy of trigeminal nerve):三叉神经第3支痛时,切断感觉根下外侧50%。第2、3支痛时,切断80%。3支全痛时,全部切断感觉根。位于感觉根腹侧的运动支比感觉根色较白,呈单根粗大的纤维,易识别,应保护之(引自《神经外科手术步骤点评》)。
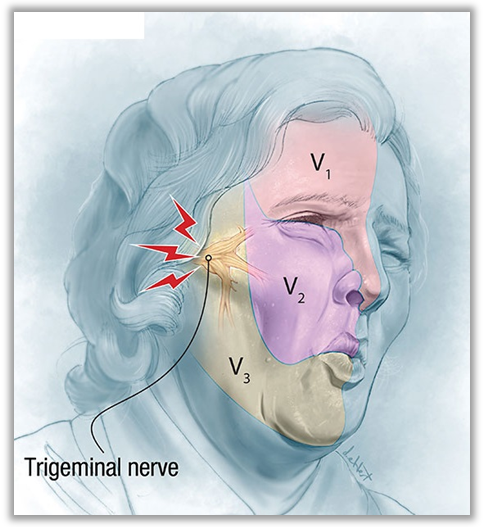
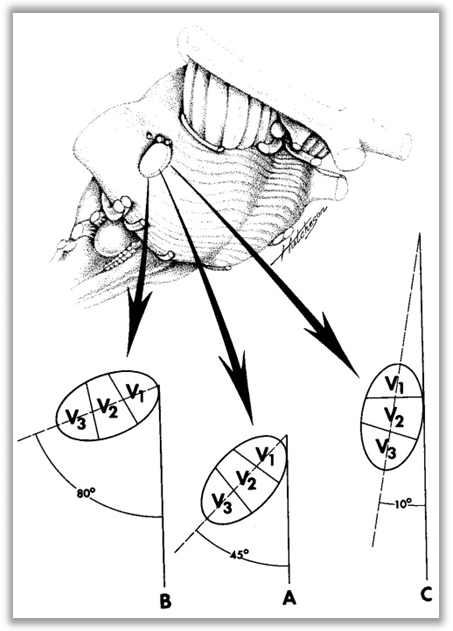
桥脑处三叉神经横切面的长轴与身体的长轴夹角的变化。大多数三叉神经的长轴与身体长轴呈40°~50°夹角(A),然而这一夹角可在10°(B)~80° (C)之间。B中第三支几乎完全位于第一支的外侧,C中第三支则几乎完全位于第一支的尾侧。(引自Rhoton解剖学)
由于三叉神经的长轴可呈10°-80°夹角,受血管压迫推移后三叉神经轴性会发生改变,神经血管接触位置与三叉神经分支对应关系会有很大变异。术者需要有良好的空间想象力,才能完成准确有效的减压。
▼2.三叉神经与岩静脉的关系
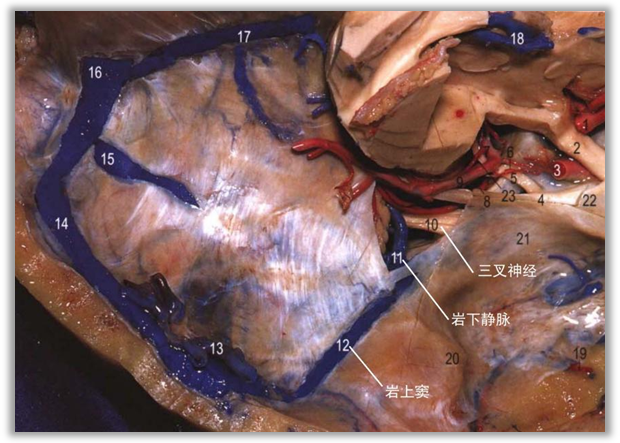
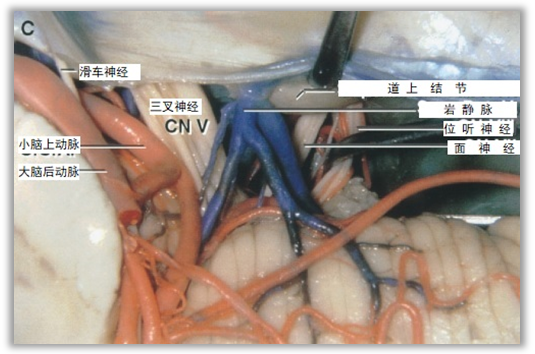
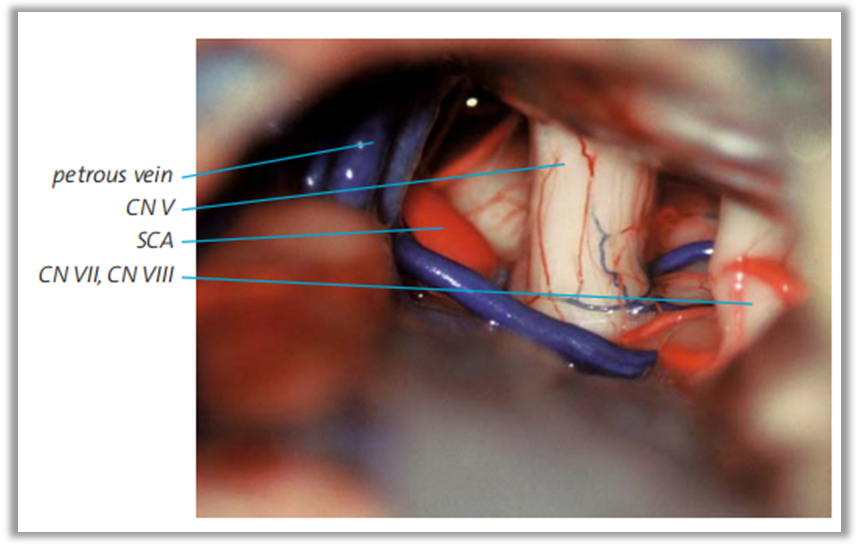
引流入岩上窦的岩静脉在到达三叉神经的手术中最常见到,也是造成三叉神经压迫的常见原因。岩上静脉是引流小脑外侧部和脑桥的一组静脉,是后颅窝内最大和最常见的静脉。岩上静脉粗细、分支变异很大,通常在穿出蛛网膜汇入岩上窦前会汇聚为1~2支Y形短粗主干。
岩上静脉可以是单支静脉的终末段或多支静脉汇合形成的总干。其汇合点通常位于三叉神经的外侧,但也可能位于三叉神经的内侧,汇入部位距离三叉神经通常不足1cm。总干在到达岩上窦之前绕行三叉神经。这些总干也可能对三叉神经造成压迫。
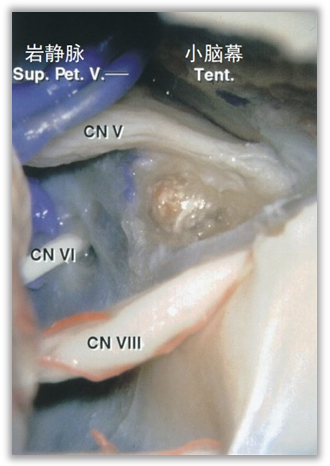
横窦乙状窦定位
要想使用锁孔入路,必须准确定位乙状窦、横窦的位置。
国内外很多文章提出了不同的定位方法,实践中发现一些方法应用起来不方便。
最准确的定位方法是术中神经导航。如果手术时间紧张,来不及使用导航,以及在那些没有导航的单位,就只能按照解剖标志去定位。

国内不少文献报道均把星点作为横窦乙状窦交界(上曲)的标志。而Martinez发现只有27.8%的星点位于交界处。星点并不是确定横窦乙状窦交界处的标志,而且60%的尸头标本上不易找到这个标志。
既往文献报道,颧弓上缘和枕外隆凸连线是横窦在颅骨表面的投影(上图)。乳突尖至顶切迹(颞鳞和顶乳缝交点为顶切迹 )的连线为乙状窦的颅外标志线(下图),而乳突根部深面即为乙状窦膝部。

而实际上上项线和横窦走行不完全一致(下图),上项线与横窦的关系多样:上项线可作近段横窦的定位标志,但是随着它们向外移行,上项线则主要位于横窦下方,并且它们的距离越来越远(下图)。而且横窦本身不是一条线,而是一个直径11mm左右的管道,且直径和形状都在变化。
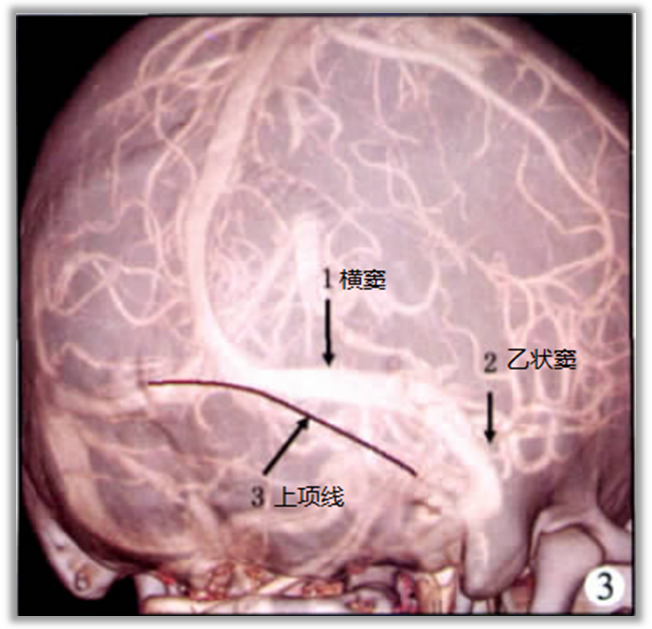
实际上,乙状窦、横窦位置经常会发生变异,如下图中,横窦距离上项线较远,直窦几乎呈垂直状态。对于该病人,不能按照常规的颅骨解剖标志来定位。

在此,笔者建议术前一定要行颅底薄层CT、颅底MRI平扫+增强检查,不仅可以区分原发性与继发性三叉神经痛、显示三叉神经根周围的血管及其与三叉神经后根之间的解剖关系。更重要的是获取每一个病人的横窦、乙状窦、乳突窦的准确定位。
笔者推荐以下几种方法:
▼1.砂轮片术前体表定位:
术前一天剃发,在枕外隆凸与颧弓根连线、乳突尖至顶切迹的连线上置一枚大小约1.5cm的医用砂轮片(砂轮片大小正好与骨窗大小一致,下图)。行颅底薄层CT扫描,获取横窦及乙状窦与外置砂轮片关系,在头皮上用龙胆紫描记出横窦及乙状窦之体表投影。
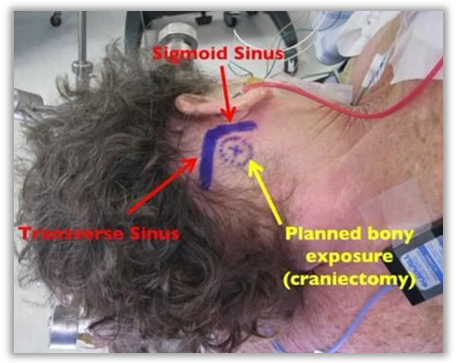
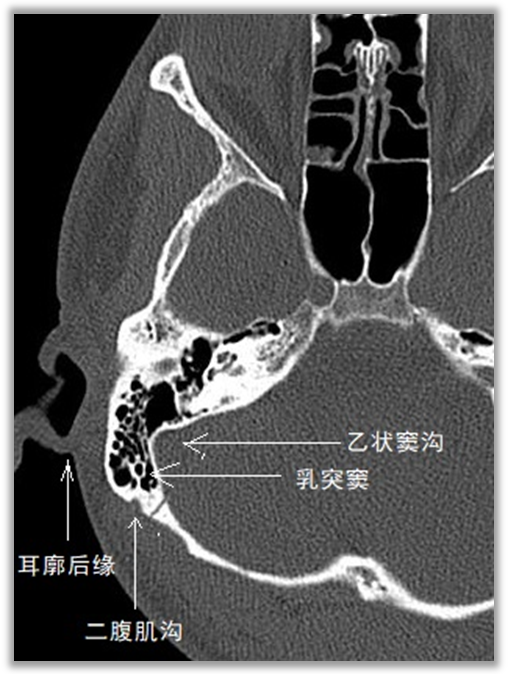
此外,还可以测量耳廓后缘与乙状窦沟的体表距离,作为术前皮肤划线的参考(只作为参考,并不准确)。上图中还可以看到乳突窦发育良好,术中需要打开乳突窦才能良好暴露乙状窦,因此术中注意无菌操作,碘伏冲洗术野有助于预防术后感染。
▼2.二腹肌沟顶点术中定位横窦
切开肌肉和皮肤后就只能利用颅骨骨性标志去定位。二腹肌沟(乳突沟)顶点在颅底CT扫描以及手术中均易于寻找,可以作为解剖标志定位横窦(引自《宣武神外夜校》)。首先,在CT薄层扫描上识别二腹肌沟顶点、横窦与乙状窦拐角位置(下图),计算层距×层数得出二腹肌沟顶点与横窦的距离,即可在术中确定横窦的位置。
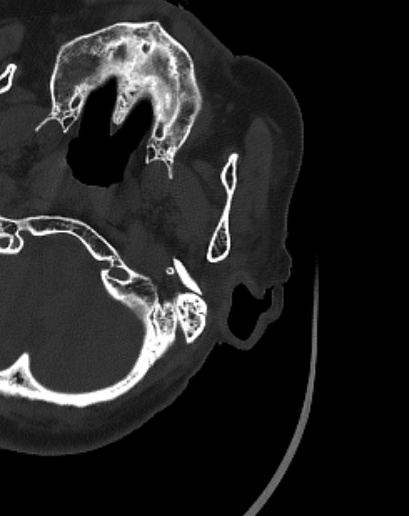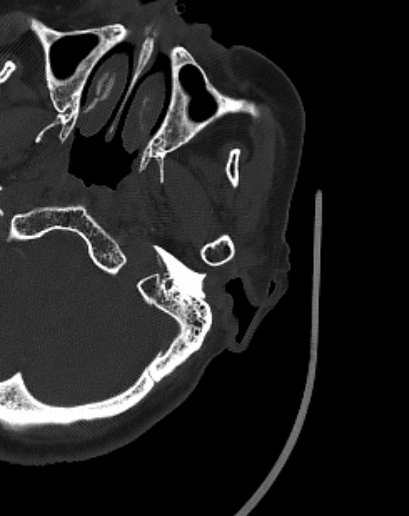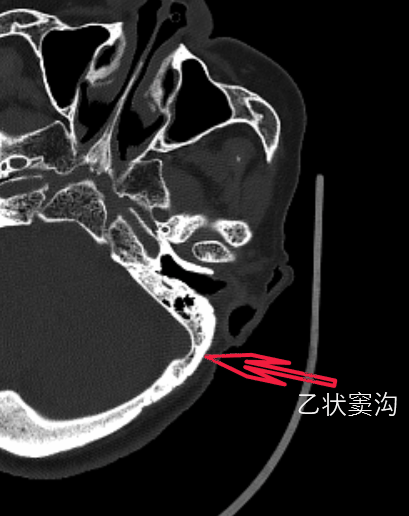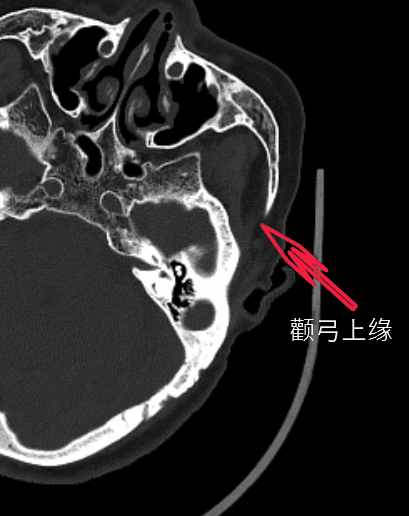
▼3.乳突导静脉术中定位乙状窦
通常乙状窦后缘位于乳突导静脉前方5mm处。乳突导静脉往往并不直接位于乙状窦的表面,相反,乳突导静脉在进入乙状窦之前,要向外上方蜿蜒潜行一段距离后汇入乙状窦的上曲或者垂直部。文献报道92%的乙状窦有乳突导静脉(引自Neurovascular Surgery)。因此,乳突导静脉是一个定位横窦和乙状窦交汇处的很好标志。
手术体位
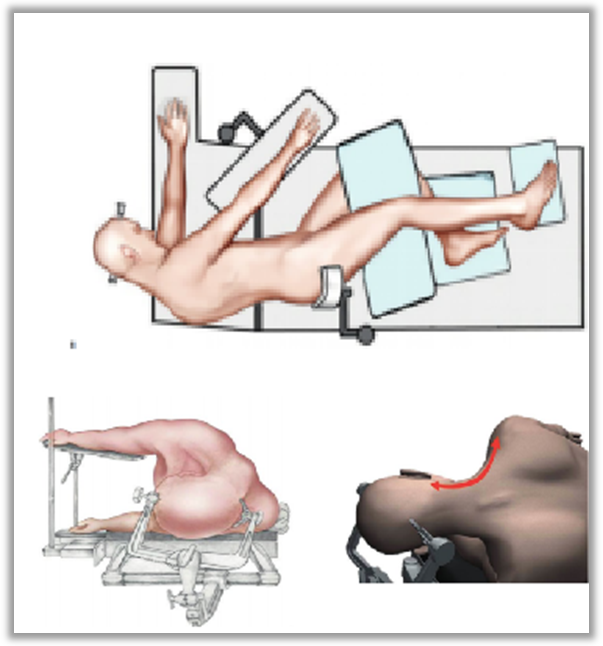
健侧俯卧位,腋下垫起,健侧上肢外展小于80°。上半身略抬高5°,头部略下垂,使患侧乳突位于头部最高点,同时要略高于心房水平,使颅内静脉窦保持较低压力。患侧肩部用肩带轻拉向床尾端,使颈肩角>100°,确保手术操作不受肩部阻挡影响(上图),需注意不可牵拉过重,以免造成臂丛神经损伤。
头部由一个三钉的Mayfield头架固定。两个钉固定在对侧枕下骨质(上钉位于枕外隆突和下钉位于乳突体)。另一个单钉固定在发际线内的额正中线上。
麻醉要求
采用口腔插管静脉复合全身麻醉,可以使病人彻底松弛,保证手术安全。麻醉诱导时应尽量平稳,更重要的是麻醉终了时病人要逐渐清醒,避免带着气管插管发生躁动。术中保持收缩压100~120mmHg。手术3小时内补液量一般不超过1500ml。过快和过量补液会导致脑组织张力过高,影响手术入路进入。保持轻微过度通气状态,使CO2分压处于30~32mmHg范围为佳。
手术切口与入路
切口的位置是可变的,取决于患者颈部的长短和粗细。
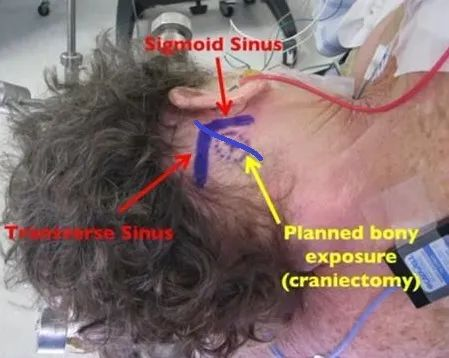
手术前,剃除患者耳后3cm×5cm区域的头发,触摸确定骨性标志:乳突,二腹肌沟、枕外隆凸。按照术前颅底CT薄层扫描,画出横乙窦的体表定位,按下图所示在乳突后上部发际内平行于发际斜行作一3-4cm的直形切口。切口的3/4应位于横窦和乙状窦的交界处的下方,1/4位于其上方。
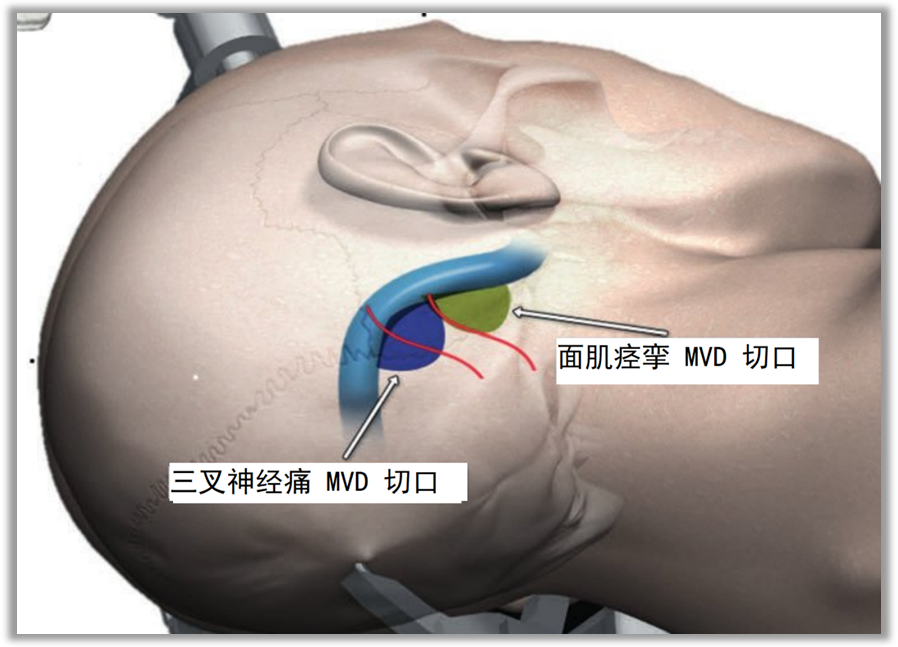
乳突后区上部切口适于三叉神经痛,乳突后下区下部切口适于面肌痉挛和舌咽神经痛。
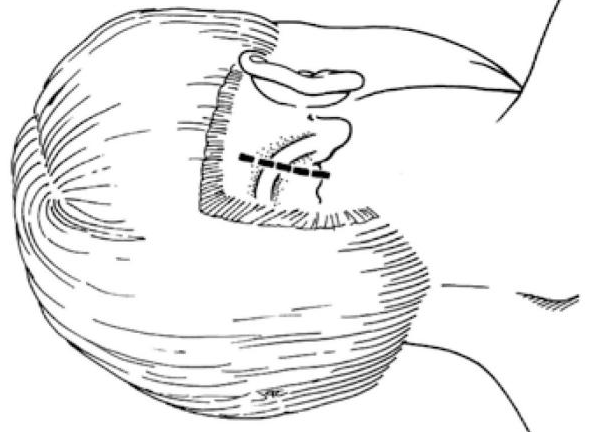
脖子细长的患者的切口可以略短。而脖子粗短的患者,手术切口应略长,且更靠后(内)一点,切口的下极应更向后方(内侧)倾斜。这种切口需要对乳突、二腹肌沟附近的肌肉进行更广泛的分离,将肥厚的颈部肌肉置于后方(内侧)。
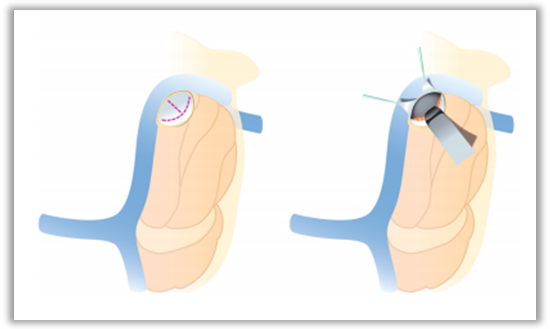
对于三叉神经痛的微血管减压术,通常采用小脑上外侧入路。此入路缺点是常常会受到岩上静脉的阻挡,需切断岩上静脉。近年来改良采用小脑外侧经水平裂入路(paracerebellar trans-horizontal fissure approach),在三叉神经和面听神经之间通过打开小脑水平裂蛛网膜,利用此裂隙到达三叉神经根部,可避开大部分岩上静脉对入路的影响(引自《神经外科锁孔手术学》)。
显微镜下三叉神经痛MVD锁孔入路
本视频来自Microneurosurgery网站,文字介绍部位节选自Jannetta教授名著《三叉神经痛》以及Aaron教授《The Neurosurgical Atlas》。视频中省略的一些步骤本文将以文字介绍的方式进行补充。
▼1.手术切口(详述见上)
▼2.术区常规消毒、铺单,切开头皮。单极电凝切开头皮直达枕骨。软组织用骨膜剥离器分离,必要时可以使用单极电凝。应首先向前方(外侧)剥离骨膜,然后再向后方(内侧)分离。乳突后方的软组织必须清除。单极分离项部肌肉。定位、结扎、切断枕动脉。
放置一个小的后颅窝牵开器。可以从枕下筋膜层取下一薄的筋膜片,用于硬膜修补以实现水密缝合。定位乳突导静脉,予以电凝,骨蜡封闭之。
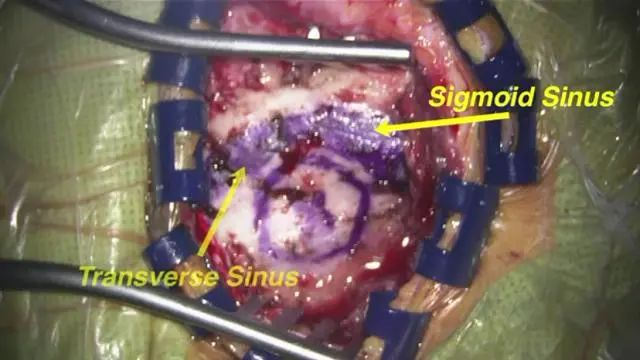
▼3.钻孔前,应充分暴露骨性标志。软组织应向前分离至二腹肌沟的前方,二腹肌沟顶点应该清晰可见,按照二腹肌沟顶点、乳突导静脉位置,标记横窦乙状窦夹角处。采用高速磨钻开颅时,钻孔位置应位于乳突导静脉的上方或内下方。
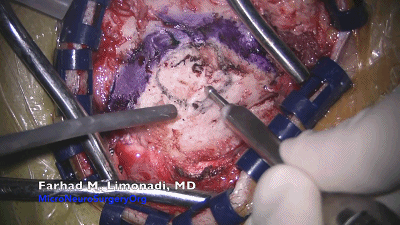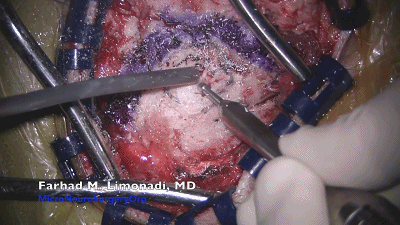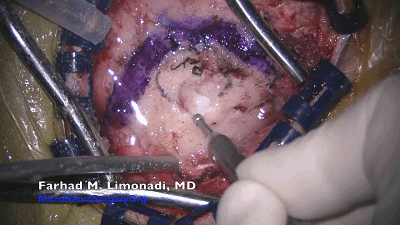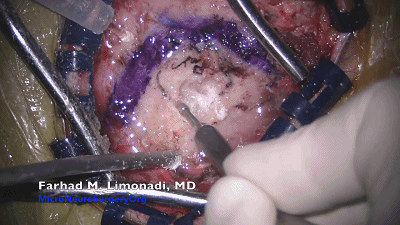
▼4.使用4mm的金刚石磨头磨出一个直径1.5-2cm的锁孔骨瓣。位于横窦和乙状窦交界的内角,上缘暴露部分横窦,外侧暴露乙状窦后缘。最后的薄层皮质骨(蛋壳)用尖的A型咬骨钳或刮匙轻轻将其去除。骨缘内板应予以磨除以提供充分的操作空间。
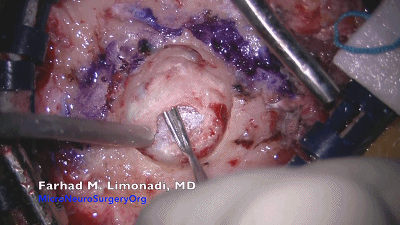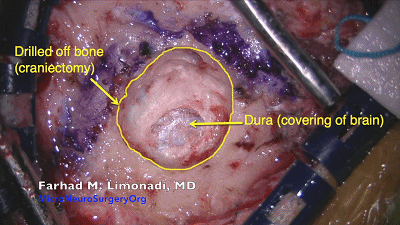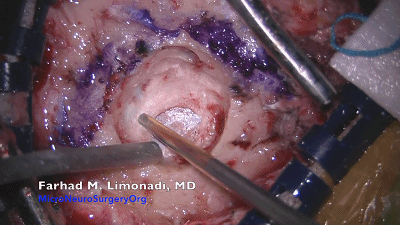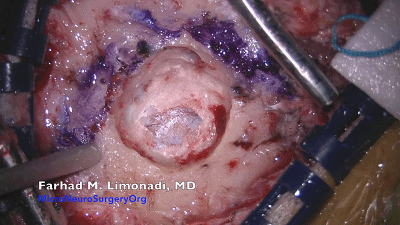
▼5.开放的乳突气房应用骨蜡彻底封闭。笔者建议乳突气房封闭后用碘伏冲洗术野,预防感染效果良好。有医师建议乳突封闭之前不要用水冲洗术野,避免术后乳突积液。
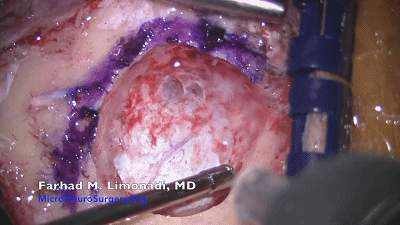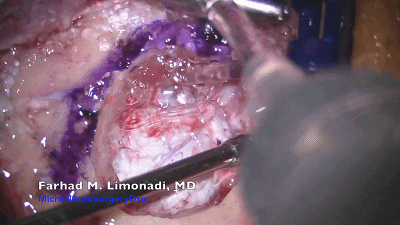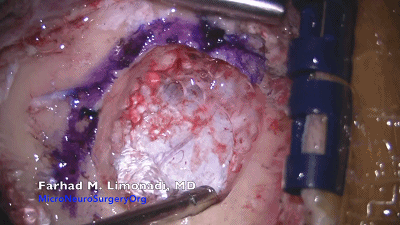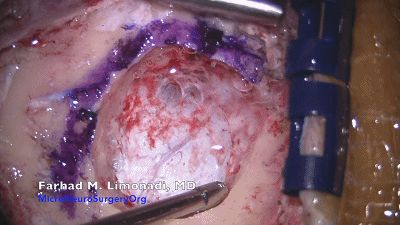
▼6.采用尖刀片切开硬脑膜,齿镊上提硬膜缘,用精细的硬膜剪刀,沿着窦缘切开硬脑膜。弧形切口即可很好暴露。接近静脉窦时,硬脑膜会变厚。使用精细剪刀一点一点地剪开硬脑膜,即使出现小破口也可以较容易地用双极电凝处理。

▼也可以在横窦和乙状窦交界处做倒T形切开。
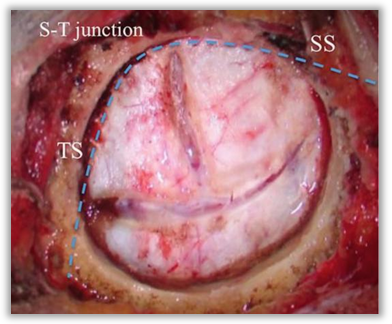
▼对于锁孔骨窗,由于空间狭窄,硬膜切开操作有时比较困难,笔者推荐采用细线将硬膜悬吊拉起,方便尖刀或剪刀切开硬膜。
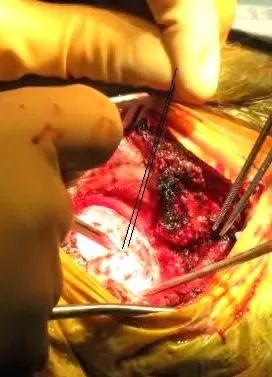
▼7.悬吊硬脑膜,使硬膜开口最大化。
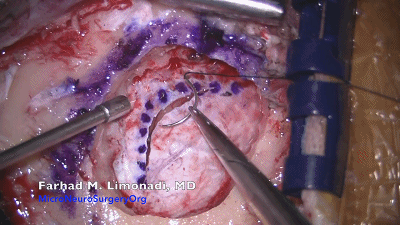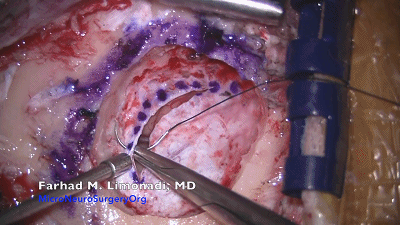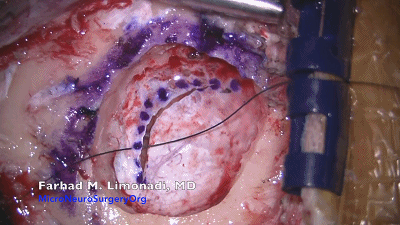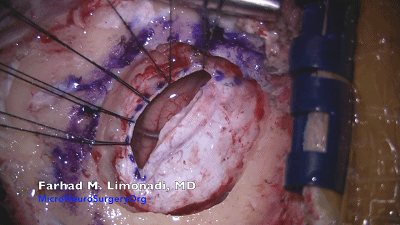
▼8.湿明胶海绵置于硬膜边缘,防止硬膜干燥,利于止血,便于硬膜后期缝合。
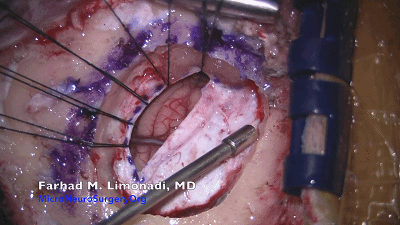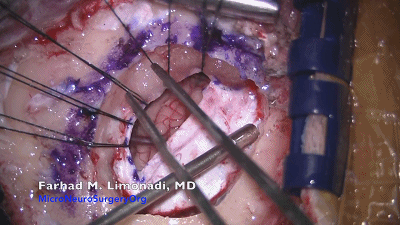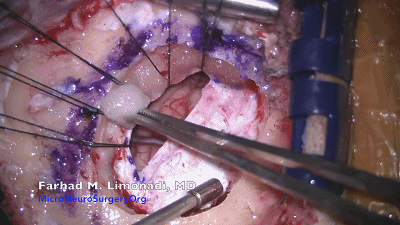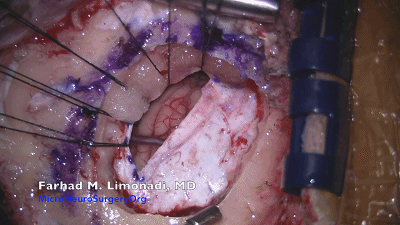
▼9.剪一小片手套(剪成略大于脑棉)作为橡胶垫片,橡胶片可以防止与小脑的粘连,并可以让棉片在小脑表面较容易移动。
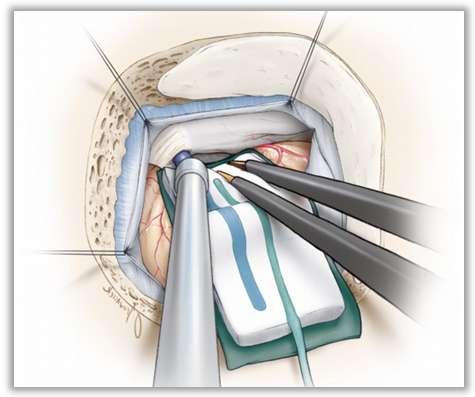
▼10.将保护小脑皮层的橡胶片-棉片置于小脑上外侧后,采用自动牵开器,轻轻地牵开小脑、将尖端细窄的脑压板弯曲呈30°~60°角(而不是呈弧形),置于橡胶片和棉片表面。
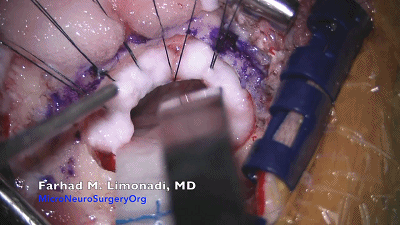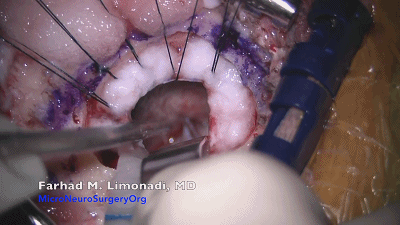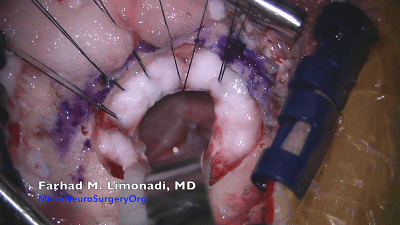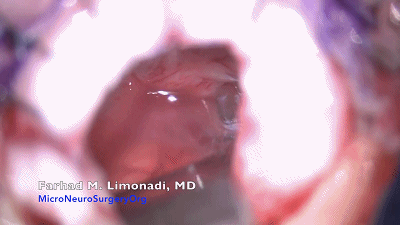
使用自动牵开器的目的是将小脑向着术者的方向抬起,而不是简单地将小脑牵拉到内侧。这有利于脑脊液引流,从而最大限度地减少对小脑的牵拉。笔者不建议使用脑压板和自持牵开器,采用无牵拉或少牵拉技术可以大大降低小脑和脑神经挫伤的并发症。
建议没有经验的外科医生放置腰大池引流以避免小脑肿胀。
如遇脑张力高切忌用力牵拉,应了解有无补液速度过快,体位有无异常造成静脉回流受阻,CO2浓度是否过高等情况;可以快速滴入20%甘露醇250ml、过度换气等可有助于小脑松弛,并缓慢释放脑脊液,待小脑自然退缩后开始显微镜下操作。
▼11.在手术显微镜下,术者必须先在小脑上表面或外侧面下方操作,以便进入蛛网膜下腔,释放脑脊液,使小脑充分回缩而获得足够的操作空间。我们必须要耐心,否则可能会导致桥接静脉被撕裂(尤其是在硬脑膜窦汇合处)或小脑受损伤。
岩静脉的一个或多个属支可能遮盖部分三叉神经。岩静脉上的蛛网膜予以锐性分离,将其分支牵开,远离小脑表面。只有这样,大多数情况下,才能保护岩静脉。
三叉神经常位于岩静脉之下的较深处。不应解剖内听道和前庭神经上方的蛛网膜。
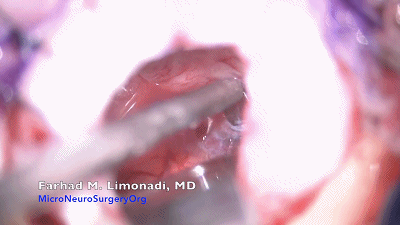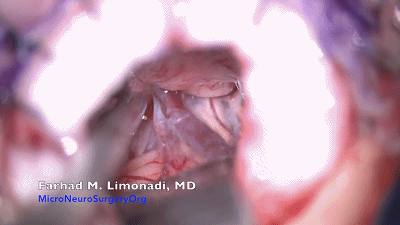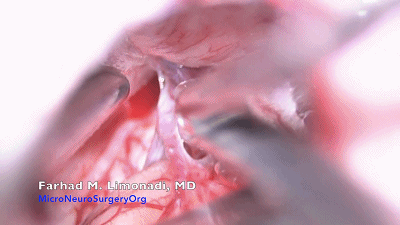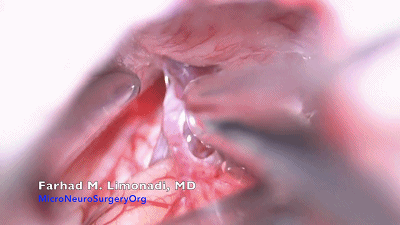
▼12.用球头剥离子探查岩静脉。为了保护岩静脉及面听神经,应该使其上覆盖的蛛网膜保持完整。
岩静脉复合体通常包括两到三支引流入小脑幕缘的静脉。如果遇到出血,它通常是由于静脉在入窦处被部分撕裂所致。静脉出血可以通过轻轻压迫和用止血纱及小棉片填塞得以控制。患者头高脚低位会减少静脉压力和出血。
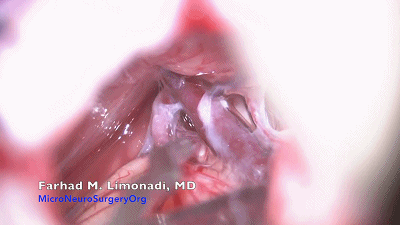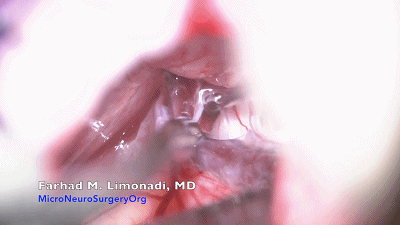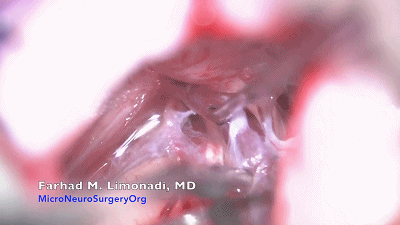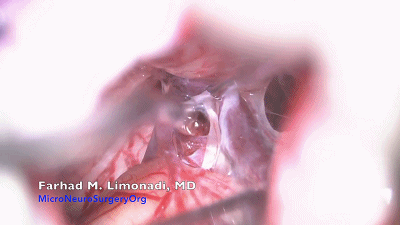
▼13.依次可见岩静脉、三叉神经、附着在三叉神经上的静脉、小脑上动脉、面听神经。
最常见的责任血管是位于神经前上方的小脑上动脉。

▼14.聚四氟乙烯(PTFE,Teflon)棉撕碎呈蓬松状,像雪茄样卷曲成各种大小(Fukushima建议将Teflon棉制作成螺纹状)。将蓬松Teflon毛毡置于血管、三叉神经REZ区之间。未曾蓬松的Teflon棉可作为继发性压迫,将血管波动传递到神经。
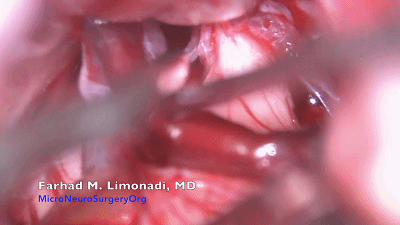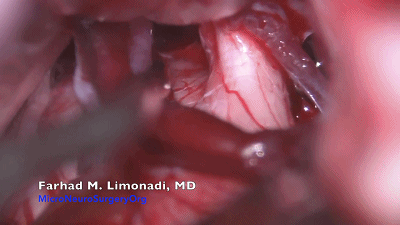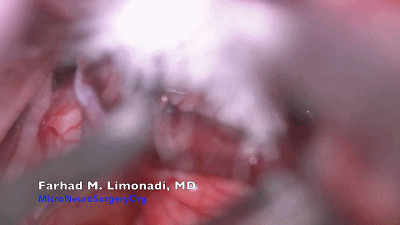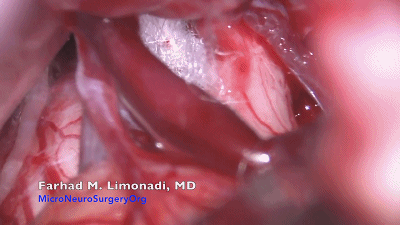
▼15.需注意的是,超过50%的三叉神经痛患者存在多根血管压迫或者多个部位压迫,术中强调全程探查避免责任血管遗漏。此病例可见一条静脉与三叉神经关系密切,将Teflon棉置入其间。
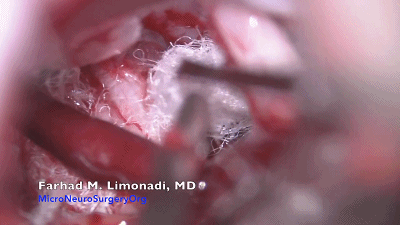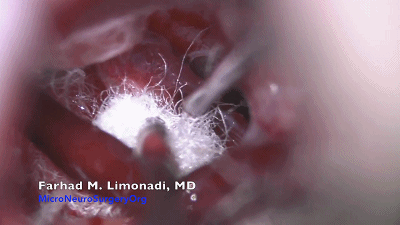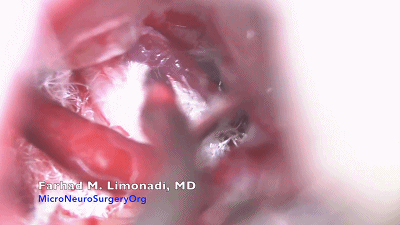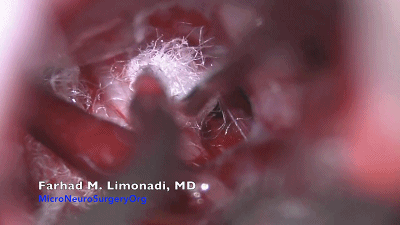
▼16.关颅:充分止血,要求麻醉师将动脉收缩压逐步回升至120~130mmHg。用温生理盐水彻底冲洗硬脑膜下腔,一是再次检查术野是否有出血,二是防止低颅压和颅内积气。冲洗时应检查垫片有无脱落。
脑表面覆盖一条明胶海绵,硬脑膜水密缝合,硬脑膜无法严密缝合时可用皮下筋膜或人工硬脑膜修补。硬膜外无须放置引流。
骨蜡再次封闭乳突气房。碘伏冲洗术野。磷酸钙材料均匀涂抹在硬膜上或钛板可用于颅骨修补。
最后,逐层缝合肌肉和头皮。缝皮时,每层的冲洗对于预防感染很重要。
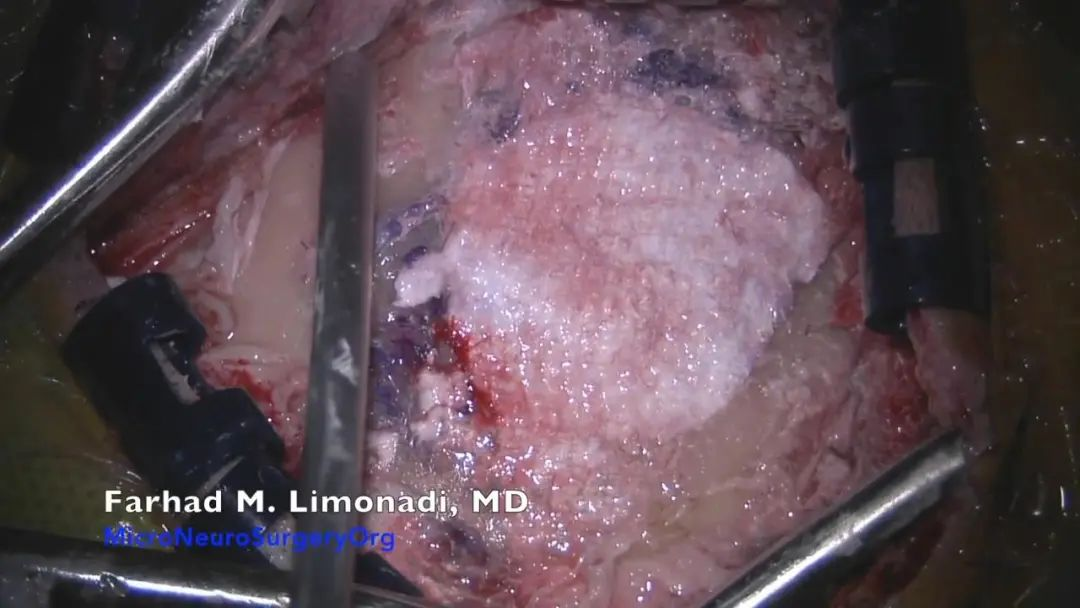
内镜辅助显微镜下
三叉神经痛MVD锁孔入路
本示教视频由Neurosurgery Greifswald制作。笔者进行简要文字介绍。详细文字介绍请参考上文。
▼1.术前CT定位,设计右侧耳后头皮切口,切开头皮。
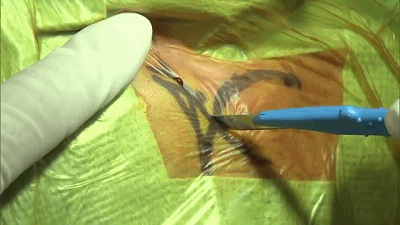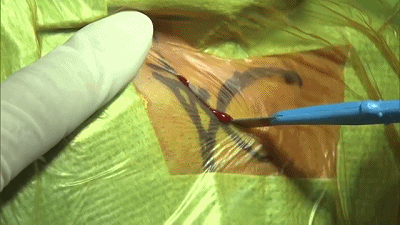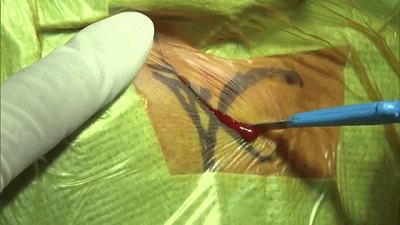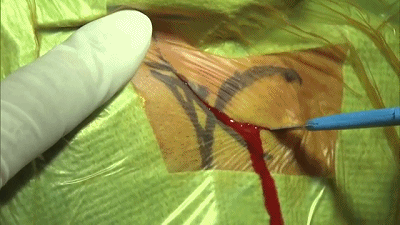
▼2.软组织用骨膜剥离器分离,必要时可以使用单极电凝。放置一个小的后颅窝牵开器。定位乳突导静脉,予以电凝,骨蜡封闭。
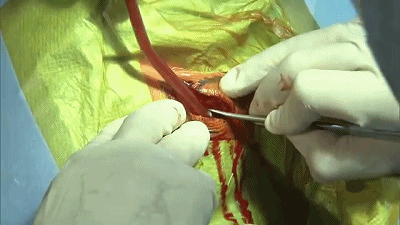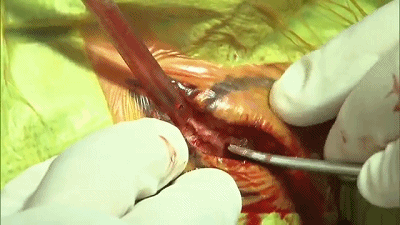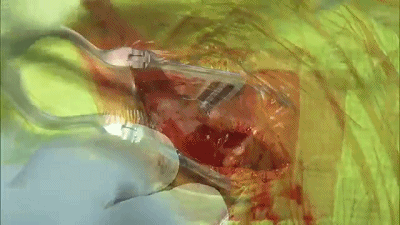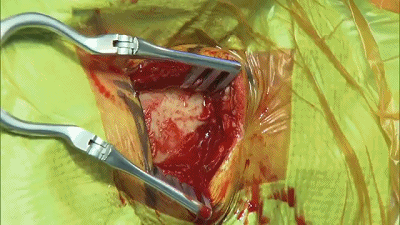
▼3.高速电钻钻孔一个或两个,钻孔位置应位于乳突导静脉的上方或内下方。
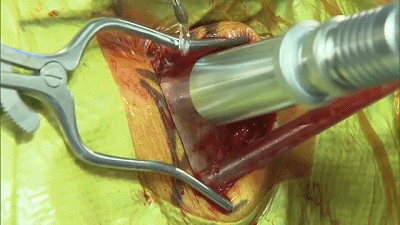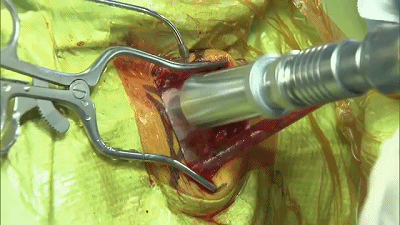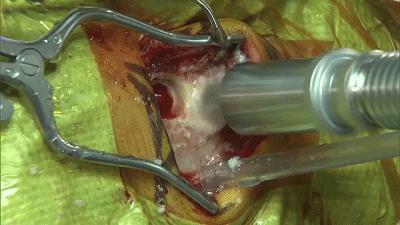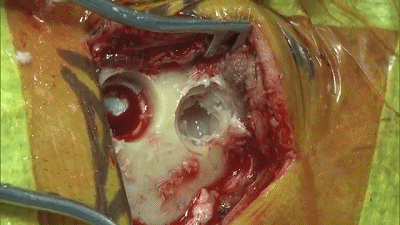
▼4.铣刀成一个直径2cm的锁孔骨瓣。位于横窦和乙状窦交界的内角。
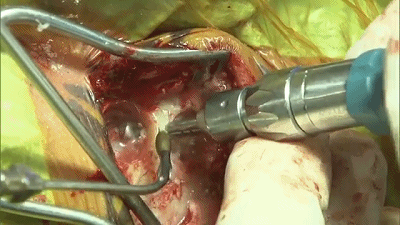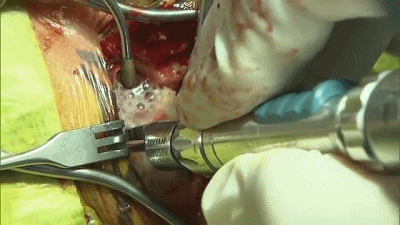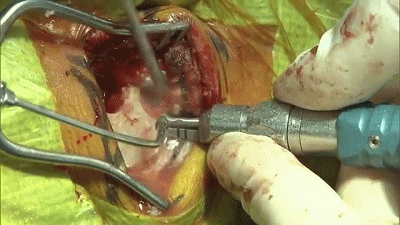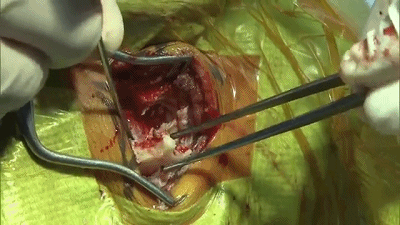
▼5.骨窗上缘暴露部分横窦,外侧暴露乙状窦后缘。骨缘内板应予以磨除以提供充分的操作空间。开放的乳突气房应用骨蜡彻底封闭。碘伏冲洗术野。
▼6.弧形切开硬脑膜,悬吊硬脑膜,使硬膜开口最大化。
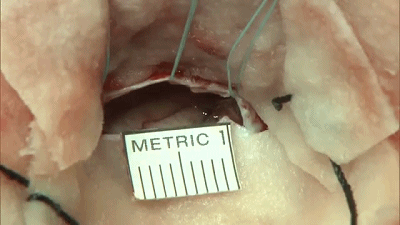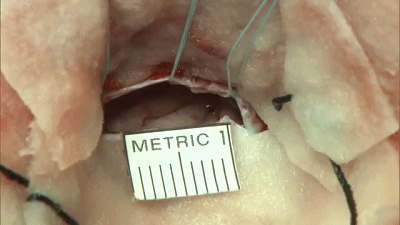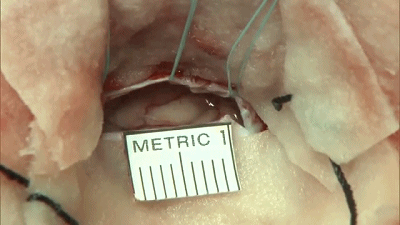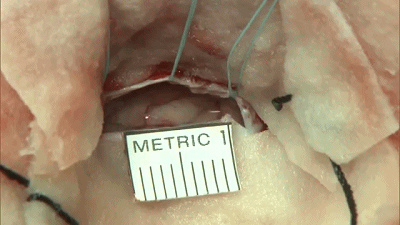
▼7.首先,在显微镜下,将保护小脑皮层的橡胶片-棉片置于小脑上外侧。缓慢释放脑脊液,待小脑自然退缩。不使用牵开器或脑压板。岩静脉上的蛛网膜予以锐性分离,
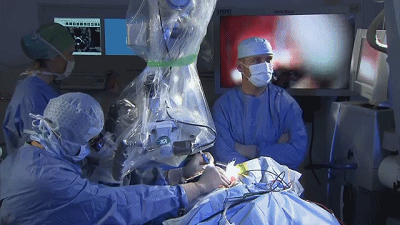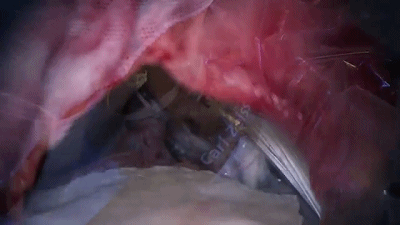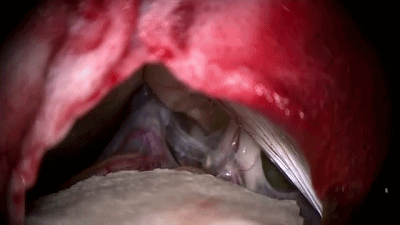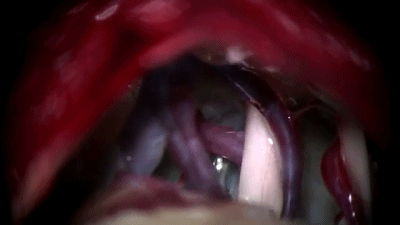
▼8.置入0度内镜,首先遇到的颅神经通常是第7-8颅神经复合体,位于三叉神经的浅表和尾侧,而三叉神经位于最上方和最深面。
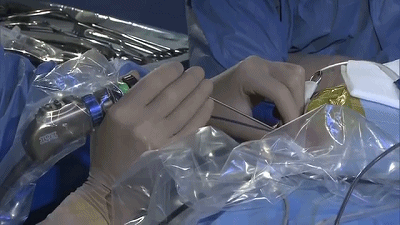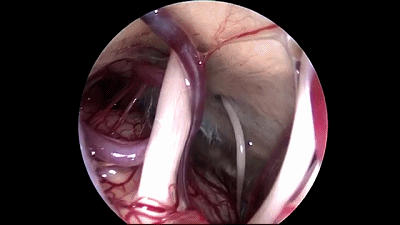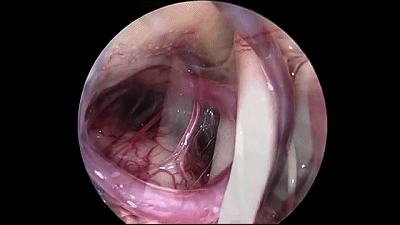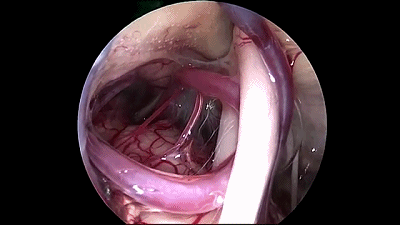
▼9.更换30°内镜,可更好的观察岩静脉、小脑上动脉与三叉神经的关系。
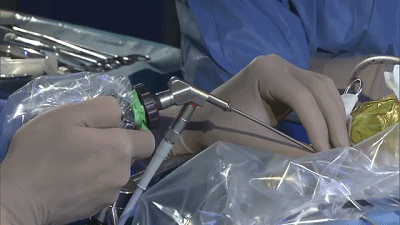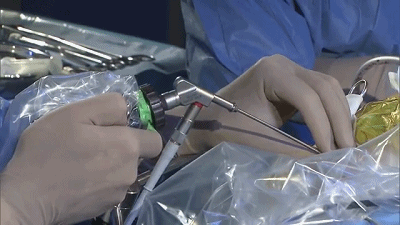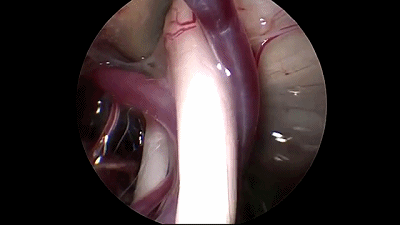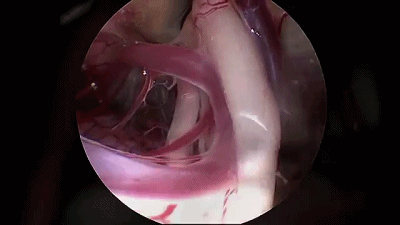
▼10.转到显微镜下,用钝头剥离子分离三叉神经与小脑上动脉。

▼11.将蓬松Teflon棉将小脑上动脉包裹起来。
▼12.将第二块Teflon棉置于小脑上动脉、三叉神经之间。
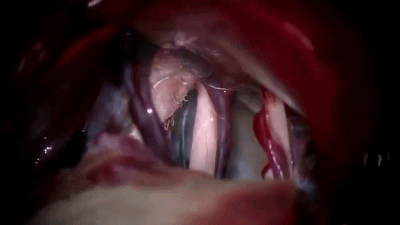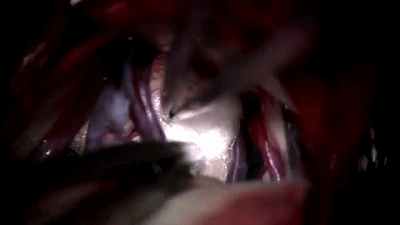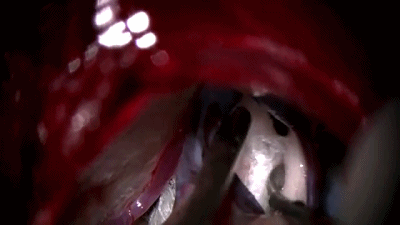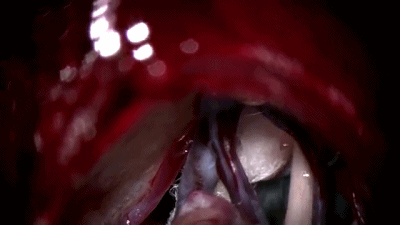
▼13.关颅∶充分止血,硬脑膜水密缝合,碘伏冲洗,骨瓣复位。逐层缝合肌肉和头皮。
全内镜下三叉神经痛
EMVD锁孔入路
本示教视频由Penn Neurosurgery制作,本视频充分显示了神经内镜在MVD手术中的优势(感谢“全国神经解剖交流微信群”提供该视频)。笔者进行简要文字介绍。详细文字介绍请参考上文。
▼1.术前CT定位,右侧耳后皮肤切口,长约3cm。单极电凝切开头皮直达枕骨。
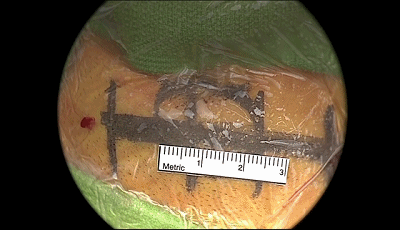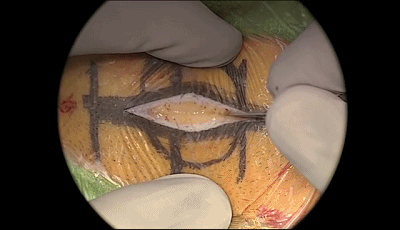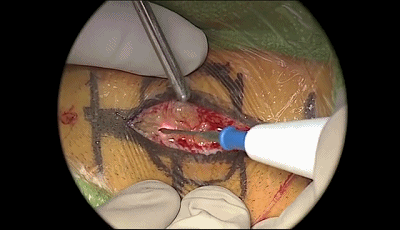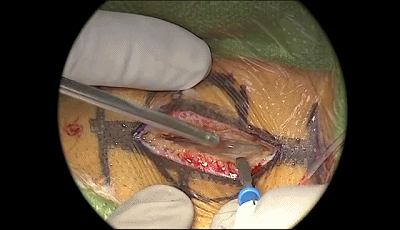
▼2.放置后颅窝牵开器。软组织用单极电凝分离。应首先向前方(外侧)剥离骨膜,然后再向后方(内侧)分离。定位二腹肌沟顶点、乳突导静脉,予以电凝,骨蜡封闭。
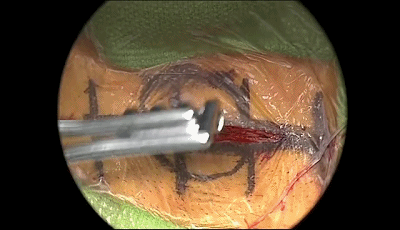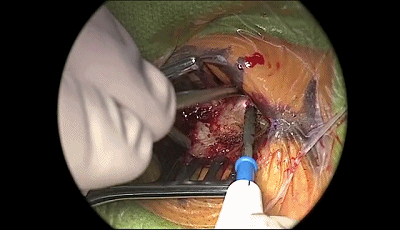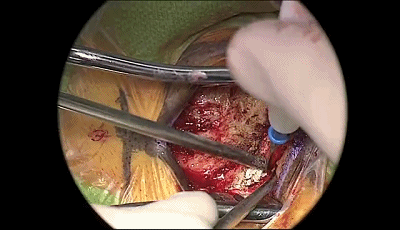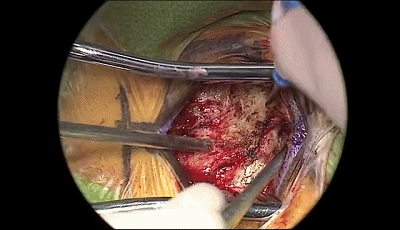
▼3.电钻钻孔一个,位置应位于乳突导静脉的上方或内下方。
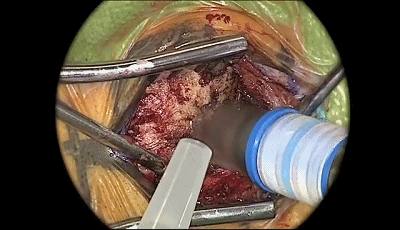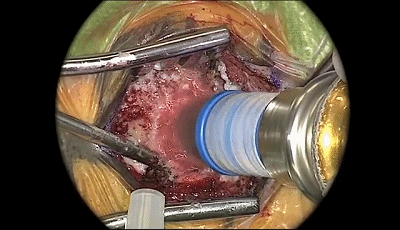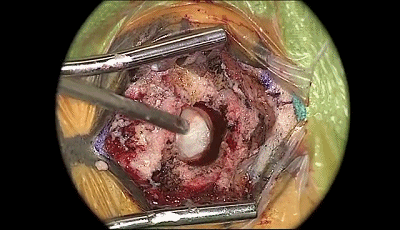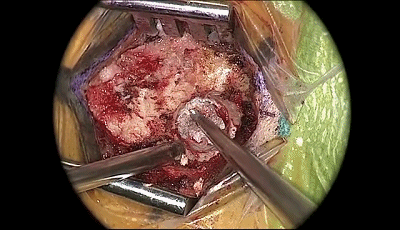
▼4.磨钻继续扩大骨孔,上缘暴露部分横窦,外侧暴露乙状窦后缘。最后的薄层皮质骨(蛋壳)用椎板咬骨钳或刮匙轻轻将其去除。骨缘内板应予以磨除以提供充分的操作空间。开放的乳突气房应用骨蜡彻底封闭。碘伏冲洗术野。
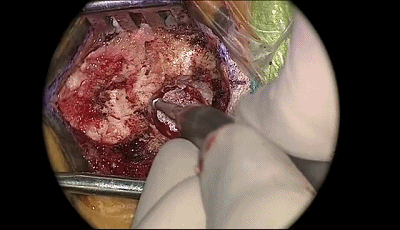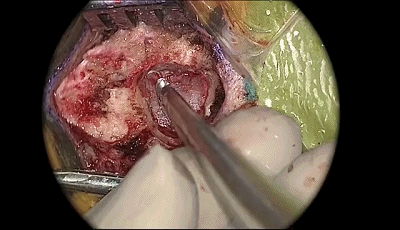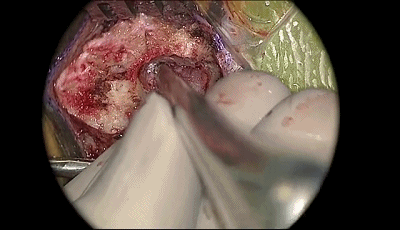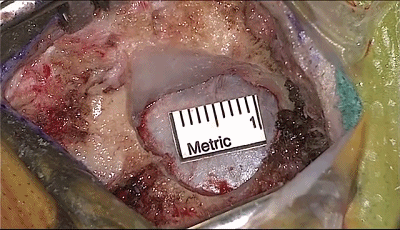
▼5.如图中弧形剪开硬脑膜。
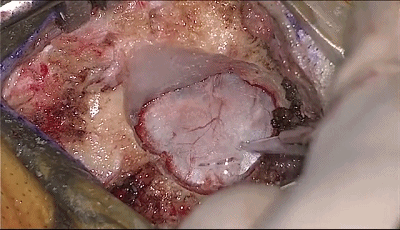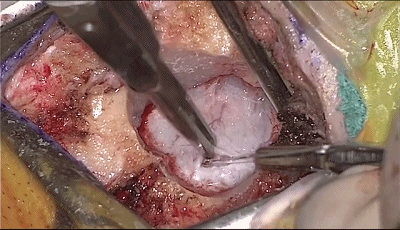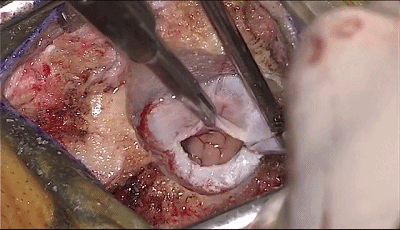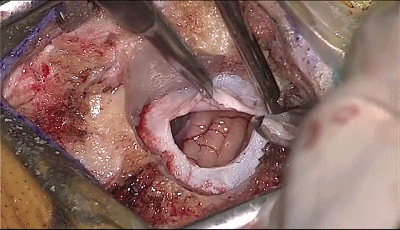
▼6.悬吊硬脑膜,硬膜开口1cm。
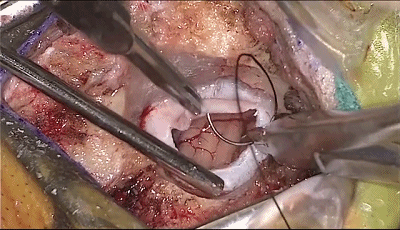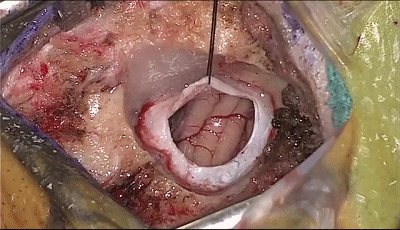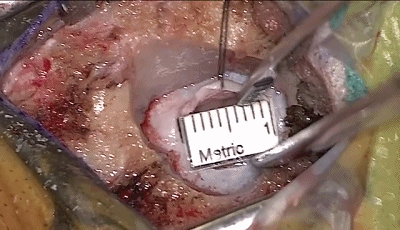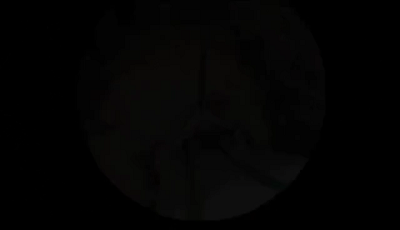
▼7.采用小脑外侧经水平裂入路,将橡胶片-棉片置于小脑表面,不使用牵开器或脑压板。
用非优势手把持0°神经内镜,用优势手持吸引器。吸引器在小脑幕、岩骨和小脑之间向前移动,内镜跟踪着吸引器头和前方的解剖结构。
释放脑脊液直到小脑变得很松弛。把内镜固定在固定臂上。
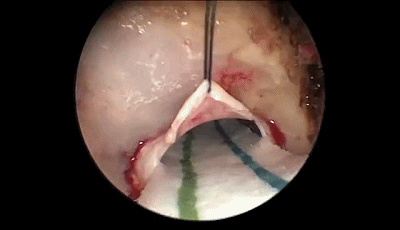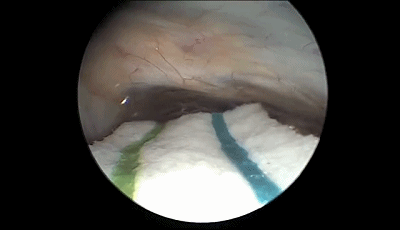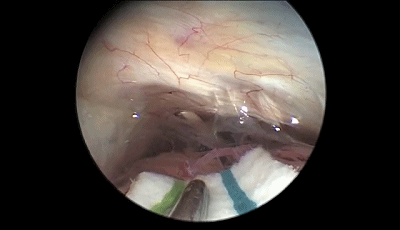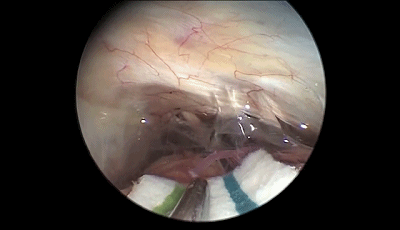

▼8.采用与显微镜手术相同的双手操作技术(上图),蛛网膜予以锐性分离。首先遇到的颅神经通常是第7-8颅神经复合体,位于三叉神经的浅表和尾侧,而三叉神经位于最上方和最深面(下图)。
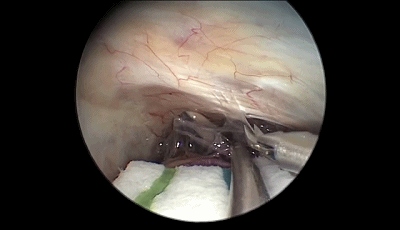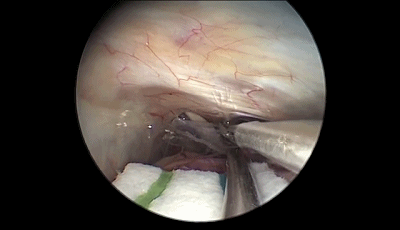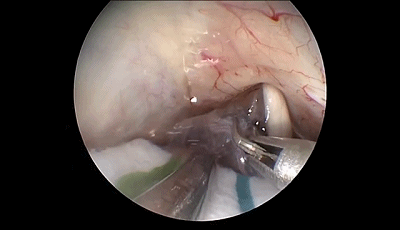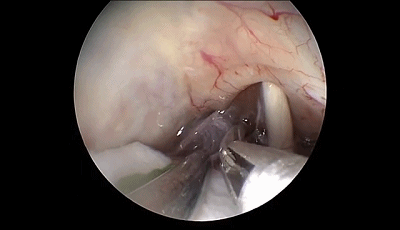
▼9.内镜继续深入,暴露三叉神经和前庭蜗神经的头端。为避免损伤前庭蜗神经,后者应该在内镜视野内。岩静脉上覆盖的蛛网膜保持完整状态。
内镜可以观察到从Meckel腔入口到进入脑桥的三叉神经全程。在显微镜下看不到的被岩骨隆起(道上结节)遮挡的静脉在内镜下也可以很容易看到。
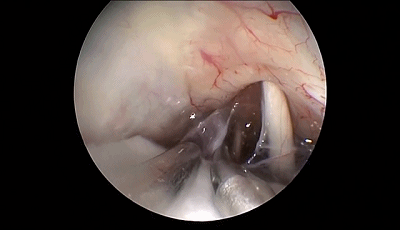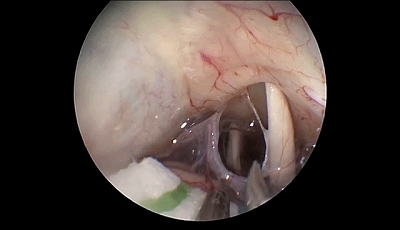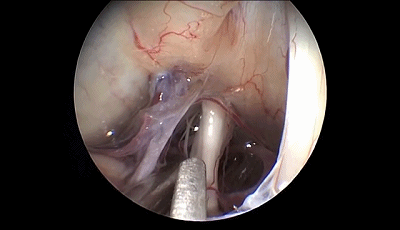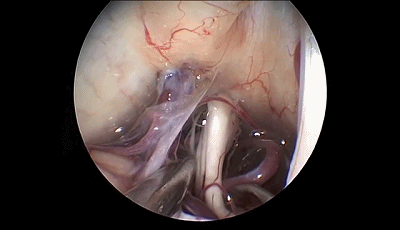
▼10.探查三叉神经的全程,可见三叉神经前方的小脑上动脉为责任血管。
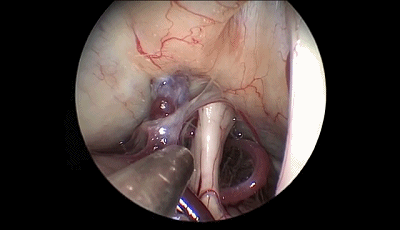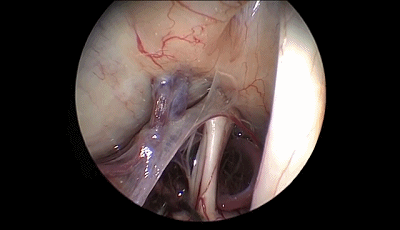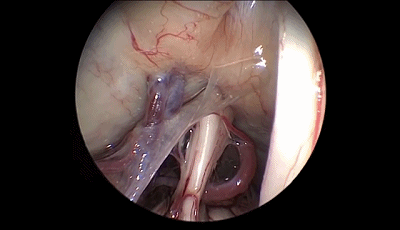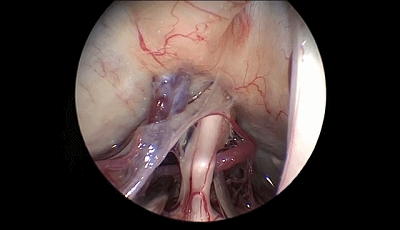
▼11.把小脑上动脉与三叉神经分离,其间垫入螺纹状Teflon棉。
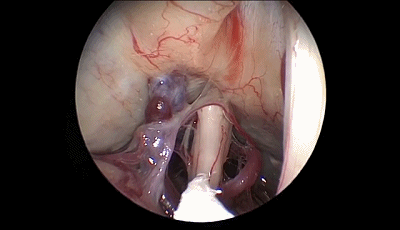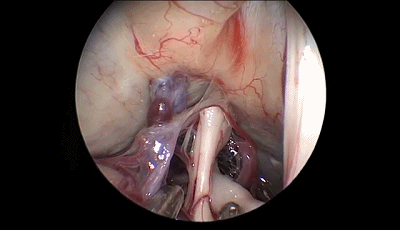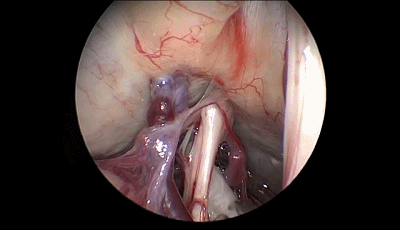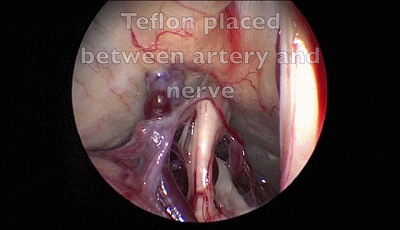
▼12.关颅∶充分止血,硬脑膜水密缝合。
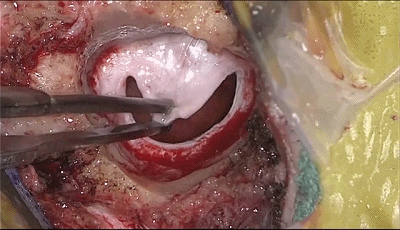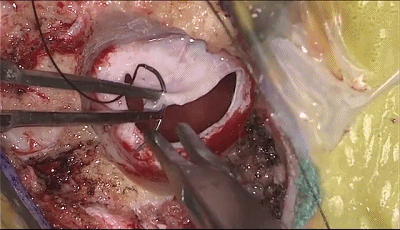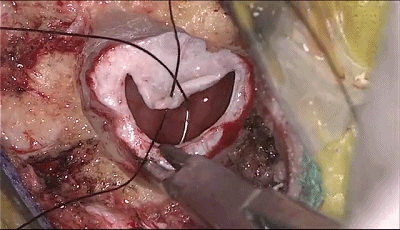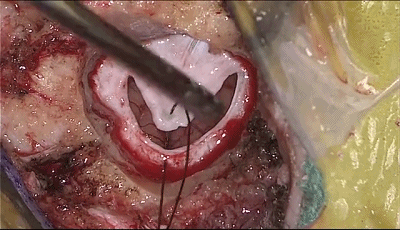
▼13.硬脑膜表面放置明胶海绵。用钛网修补颅骨缺损。逐层缝合肌肉和头皮。
MVD减压要点
▼1.责任血管的判断
根据影像学和疼痛影响三叉神经的不同分支常可估计到责任血管的来源和位置。如三叉神经V2-3痛,责任血管压迫部位往往在三叉神经后背侧,视野清晰,一般容易减压。当三叉神经痛涉及V1时,压迫部位往往位于神经腹侧,责任血管部分被神经阻挡,观察和减压有时比较困难 。
压迫三叉神经的责任血管来源依次是小脑上动脉(SCA)、小脑前下动脉(AICA)和椎基底动脉(VA-BA)。
SCA常从内侧压迫推挤三叉神经,而AICA则从外侧压迫推挤,粗大冗长的椎基底动脉常将三叉神经推挤紧贴于岩骨面。此时,宜先从后组脑神经及面、听神经间将椎基底动脉垫起牵向下方,然后再处理椎基底动脉与三叉神经的压迫。
局部动脉硬化的血管与神经接触、血管成直角张力状与神经接触以及三叉神经根上存在明显压迹和局部萎缩是神经血管接触的最佳佐证。
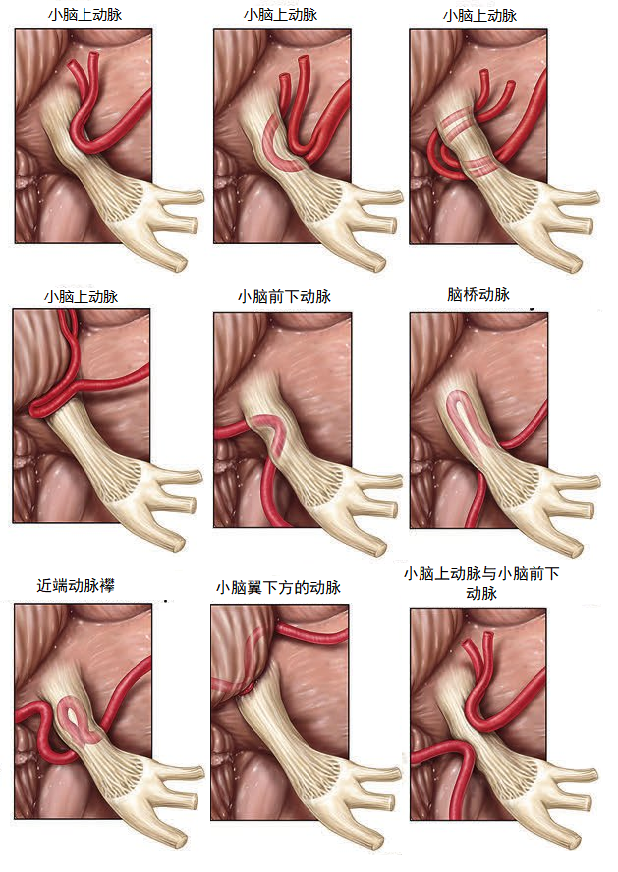
暴露三叉神经根和找到责任血管是该手术的关键。
由于三叉神经颅内段的无髓鞘部分较长,其抵御周围血管压迫能力差,其神经根的任何部位都有可能发生神经血管压迫。因此,行三叉神经根减压术时应该从最内侧的脑干端至最外侧的离开脑桥小脑角出口探查神经全程,任何与三叉神经后根存在解剖接触的血管都可能是责任血管。所有责任动脉环都需仔细解剖,并垫离神经根。
许多患者有多根责任血管,识别了其中一根责任血管后,仍需继续寻找其他责任血管,术中,责任血管与神经关系也许会随着患者体位改变而变化。术中牵拉及脑脊液的释放可能会导致血管与神经分离,以及年龄老化可能会继续拉长动脉向脑干的下方滑动,因此,责任血管可能在距真正的神经血管压迫区 1-2mm 距离之外被发现。所以该区域内的所有血管均应处理。
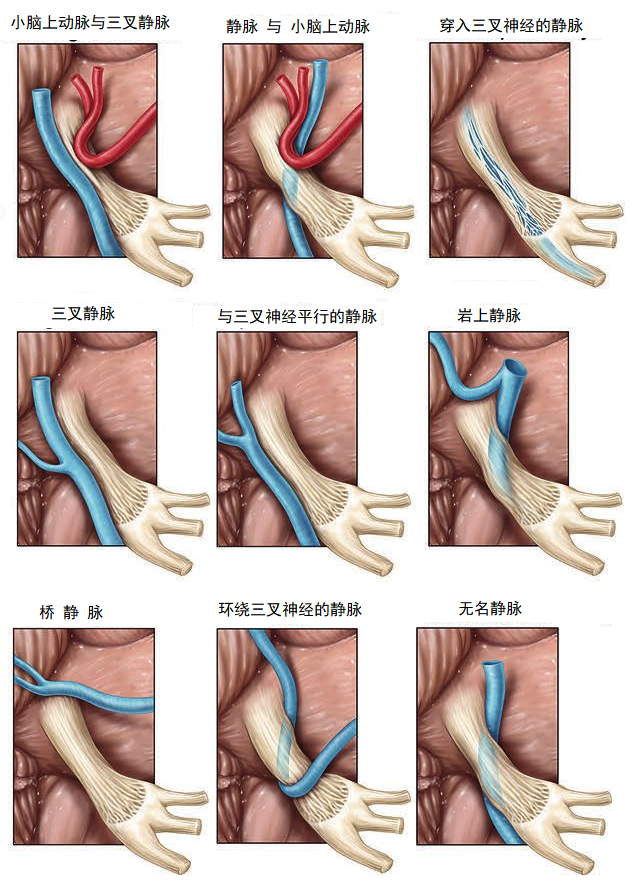
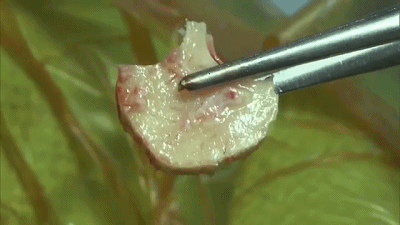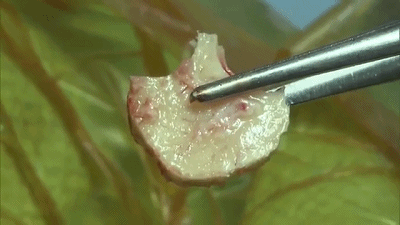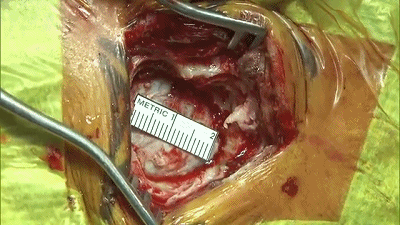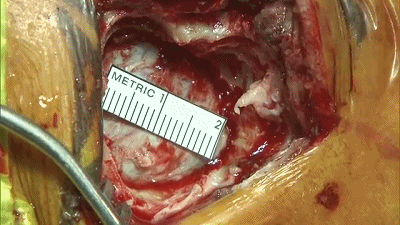
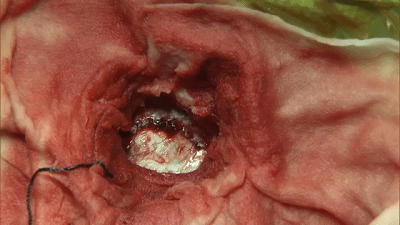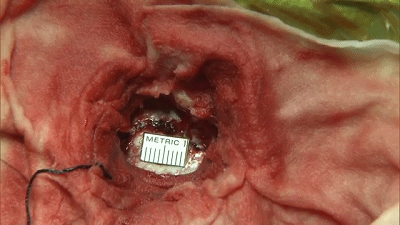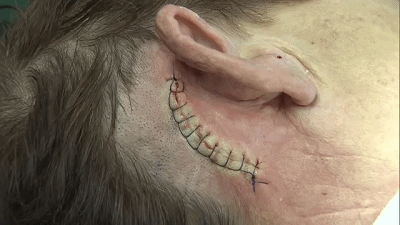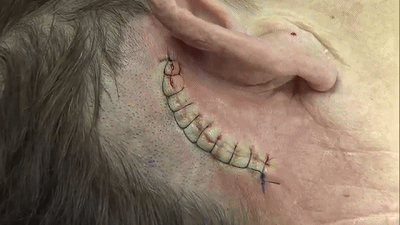
有时探查未见明显动脉压迫血管,需注意紧贴在三叉神经根部脑桥表面或穿入三叉神经的静脉也可能是责任血管(上图示三叉神经与静脉的关系)。从神经表面走行或从中穿越的静脉,似乎特别容易形成侧支而导致复发(复发在术后6周即可发生),需要仔细游离后电凝并剪断,只有将电凝后收缩闭塞的静脉条索切断才能真正达到减压目的(下图示 穿入三叉神经的静脉)。
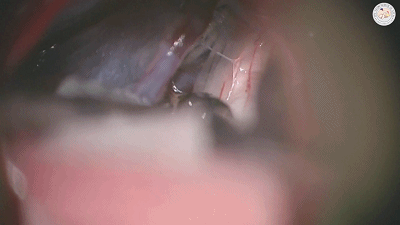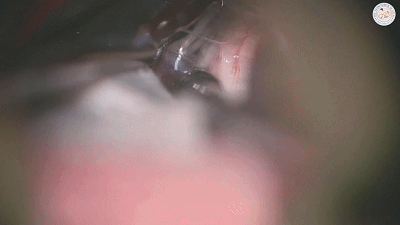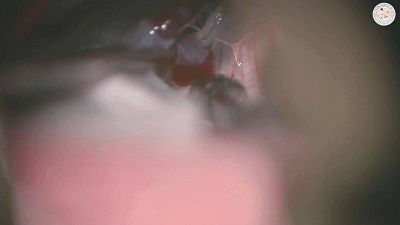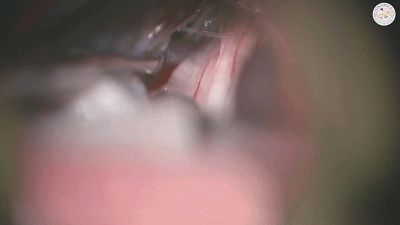
▼2.减压方法
微血管减压术的原则是通过将责任血管从三叉神经根分离移位而实现减压的目的。并不仅仅是在神经与责任血管之间垫入隔离物,更重要的是将责任血管移开,使其远离神经。可以采用聚四氟乙烯(Teflon)单点支撑、桥型支撑、棉条悬吊(下图①)、胶水黏附悬吊(下图②)等方法移位责任血管,确保血管不再压迫和接触三叉神经根。传统MVD是一种“插入式”手术方式,而“责任血管悬吊法”是一种“转位式”手术方式,理论上讲后者可永久性将责任血管与三叉神经根隔开,从而可有效降低术后三叉神经痛复发(引自《海奥视界 显微血管减压术手术策略》)。
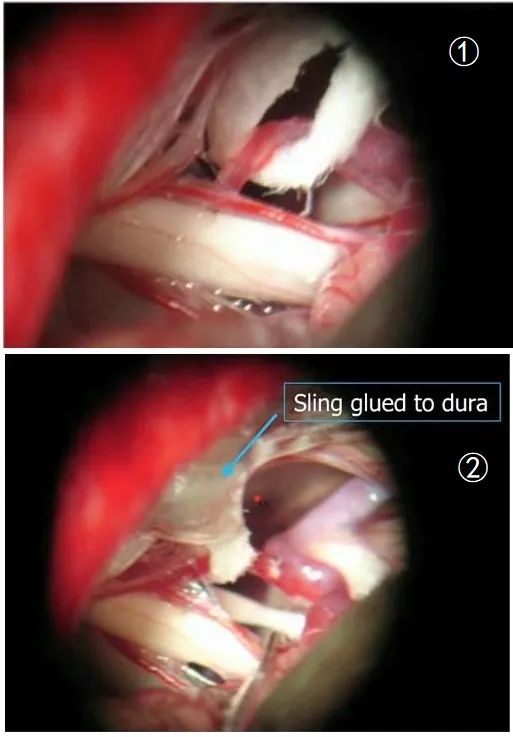
目前,Teflon或涤纶材料在MVD手术中的应用最为广泛,其排斥反应小,不易吸收,较其他材料并发症少。Teflon的作用仅是为了防止血管弹回造成对神经再次压迫,因此,垫片的位置和数量应该适当,尽可能避开神经受压迫的部位。但作为植入异物,仍可产生自体排斥反应,引起粘连并形成肉芽肿。要避免使用过多Teflon棉,防止肉芽肿形成,这可能导致疼痛复发。Teflon棉肉芽肿是一种相对公认的,可能导致复发的主要原因。
▼3.未发现责任血管如何处理
如果反复仔细探查神经周围后,未发现责任血管。Aaron建议用细镊轻轻钳夹三叉神经(下图)。这个动作起到神经切断效果,通常对疼痛控制有效。在部分微血管减压术中,只发现责任静脉存在,Aaron也会使用这种手术操作。
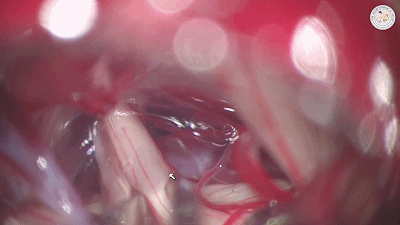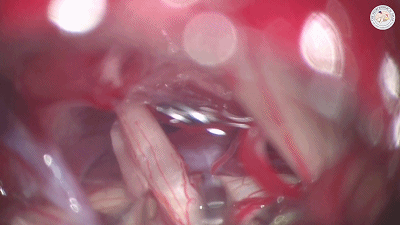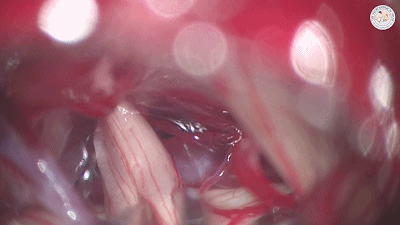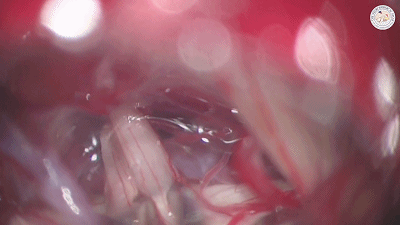
Fukushima建议当未发现血管压迫时,可彻底解剖和清理整个三叉神经根,用速即纱片包裹神经根部,并用地塞米松溶液(2mg入20ml生理盐水)冲洗。松解三叉神经脑池段全程蛛网膜粘连,使牵拉扭转的三叉神经复位有时也能达到理想效果。
▼4.岩静脉处理
当遇到岩上静脉出血,可以将一片脑棉盖在明胶海棉上,轻柔地压迫在出血的静脉上,可以有效控制幕-岩交界处水平的岩上窦撕脱性出血。同时可避免因电凝引起的硬膜皱缩,造成静脉从硬膜上撕脱损伤。
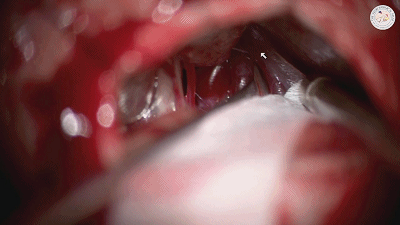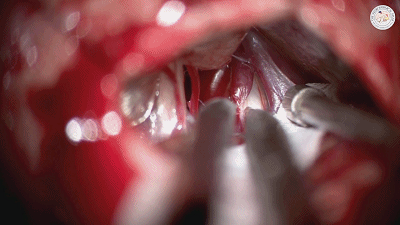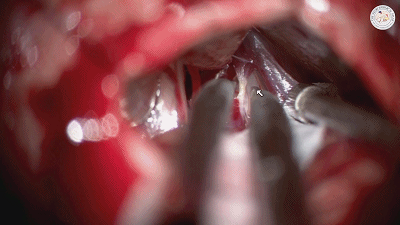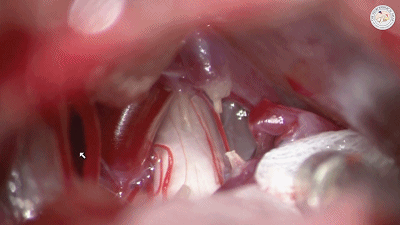
有无需要切断一支或多支岩上静脉,通常以是否妨碍观察三叉神经从根部到接近Meckel囊的脑池段全程为考量。若术中探查未能显示责任血管(在全程暴露之前就将静脉切断是探查“阴性”的原因之一)以及因桥静脉遮挡而无法充分移动动脉襻时,应先将岩静脉周围袖套状蛛网膜剪开松解,增加游离度进行观察,最好将静脉妥善保护,避免撕裂它。必需时再切断岩静脉增加显露。电凝部位应远离岩静脉汇入岩上窦的薄弱部位,电凝从小功率开始,避免大功率电凝时静脉剧烈收缩造成静脉撕裂大出血。通常仅需切断岩静脉的分支而保留岩静脉的主干回流,可以减少小脑静脉性梗死的可能性(下图示3支岩静脉牺牲一支)。
▼5.道上结节处理
岩骨内突起可以部分或完全阻碍三叉神经的显露而妨碍减压,最常见的就是道上结节。术前详细MRI检查可以发现这类情况的存在。术中磨除骨性突起后才能完全显露责任血管,有助于获得彻底减压(下图,引自宣武神外夜校)。
笔者推荐当遇到道上结节阻碍视野时,利用30°内镜抵近观察更安全一些。

术后并发症
▼1.颅内出血
颅内出血是微血管减压术后24h内出现的最严重的并发症,需密切观察患者的生命体征、神志、呼吸、瞳孔、肢体活动等,一旦有顽固性头痛、剧烈而频繁呕吐、意识障碍等,应立即复查CT并采取相应措施。
▼2.低颅压综合征
低颅压综合征是MVD术后最常见的并发症之一,表现为头痛、头晕、眩晕、恶心、呕吐等、血压偏低、脉率较快,部分高龄患者还可表现为一过性的烦躁不安、精神异常,抬高头部症状加剧,放低头位后症状可部分缓解。MVD术后1~2 d应采取平卧位,鼓励患者多饮用淡盐水,适当加快补液速度,以加快CSF的补充和循环。勿用高渗盐水及脱水剂。症状一般持续12 h~2 d,很少超过3 d。
▼3.颅内感染
MVD术后颅内感染多发生在术后3~4 d,表现为头痛加重、体温升高、颈抵抗,重症者可出现意识障碍。外周血常规白细胞数增高,腰穿CSF外观混浊,甚至呈脓性,白细胞数可达数千,并伴有糖的降低。常见致病菌多为革兰阳性球菌,最常见葡萄球菌。治疗方面需注意:(1)早期经验性应用对葡萄球菌敏感的抗生素;(2)尽快确定致病菌后足量、足疗程应用敏感抗生素;(3)必要时需行腰大池置管CSF持续引流;(4)加强全身支持治疗,如维持内环境稳定、间断输注血浆、营养支持等;(5)积极处理糖尿病等合并症。
▼4.无菌性脑膜炎
MVD术后无菌性脑膜炎发生率远高于颅内感染,临床症状难以同感染相鉴别。发病相关因素:(1)硬膜切开后往往难以严密缝合,CSF漏出至皮下及肌层下,局部渗血及坏死组织易于混入CSF并进入颅内;(2)MVD术中血管减压应用的人工材料为Teflon(聚四氟乙烯)或涤纶(聚对苯二甲酸乙二醇酯纤维)减压垫片,术中还应用人工硬膜、颅骨修补材料等植人物,这些人工材料、植入物导致的排斥反应是导致无菌性脑膜炎的主要因素之一。患者主要表现为发热、较重的头痛,脑膜刺激征阳性,外周血白细胞数正常或稍高。腰椎穿刺是必要的诊疗手段,测量CSF初压多升高,色淡红或淡黄,白细胞计数高,蛋白含量高,而糖含量正常,培养无细菌生长。腰椎穿刺3~5次以后,高蛋白、高免疫细胞的CSF被释放,由新生的CSF替换,患者症状可逐渐缓解。必要时可行腰大池置管引流术,可以加用激素治疗(甲强龙静滴→口服)。
▼5.脑脊液漏
(1)CSF漏的临床表现:
CSF漏是MVD术后常见并发症之一,分为切口漏、鼻漏、耳漏,表现为切口渗液或患者在侧卧或低头时有无色透明液体从鼻腔或耳道流出,或感觉咽喉部间断有含有咸味的液体流入。发生率为2%~8%,多出现在术后2~3 d内,可引起逆行性颅内感染而致严重后果。
(2)CSF漏的预防:
预防术后CSF漏的对策包括:①硬膜应尽可能严密缝合;②术中如遇乳突气房开放,应及时充填骨蜡封闭,关颅时硬膜修补后,应再次用骨蜡对骨缘进行涂抹封闭;③切口分层严密缝合,消灭死腔;④术后保持血压及颅内压平稳,保证患者足够的营养摄入,监测并控制血糖,慎用激素。
(3)CSF漏的治疗:
术后切口漏渗出量不多者,可采用局部加压包扎或加强缝合并加压包扎的方法处理;如切口愈合不良、渗出量多者,应及时切口清创,封闭硬膜,严密缝合肌层。症状较轻的CSF鼻漏或耳漏,可采用半卧位或抬高头位并偏向健侧,置漏口于高位以利于愈合;严禁填塞或冲洗鼻腔和外耳道,防止逆行感染;同时避免用力打喷嚏、剧烈咳嗽、便秘等能引起ICP增高的动作;经上述措施治疗3~5d仍有CSF漏者,可行腰大池置管CSF外引流术,一般在1周左右可以治愈。对于CSF漏量较大、保守治疗无效者,应及时进行切口清创,用骨蜡完全充填乳突气房,修复硬膜漏口,切口严密缝合。
▼6.听力障碍
手术侧听力障碍是MVD术后最常见的严重并发症之一,多为感音神经性听力损害。可能原因包括:①前庭蜗神经机械损伤,部分可逆;②内听动脉供血障碍,多不可恢复;③乳突开放、乳突炎,大部可恢复。究其主要原因,对神经的直接机械性损伤并不重要,而在于处理责任血管时引起了内听动脉的痉挛缺血所致。患者高龄、动脉迂曲硬化、后颅窝容积狭小、困难减压是发生听力障碍的高危因素。
除了尽量避免对前庭蜗神经的过多骚扰及保护内听动脉之外,术中使用脑干听觉诱发电位(BAEPs)监测可减少MVD术后听力障碍的发生率。但BAEPs无法真正做到实时监测神经功能,当术中发现BAEPs变化时,有时神经功能已无法恢复,但在目前的技术水平下,BAEPs监测仍然是降低听力损害最有效的措施。患者全麻清醒后应立即进行听力粗测,发现听力障碍时应行电测听检查,同时给予营养神经、防治脑血管痉挛及改善微循环等药物,并尽早行高压氧治疗。
▼7.切口并发症
此处所指MVD切口并发症主要针对因排异反应(对切口下应用的人工材料如缝线、骨蜡、钛合金网板等产生的迟发性超敏反应)而导致的切口不愈合或延迟愈合,表现为切口愈合不良、红肿、部分或全层裂开、溢液,同时可伴有顽固性头痛和发热。如反复腰椎穿刺无效,局部麻醉下切口下方人工材料取出往往是最终的选择。术中要去除所有残留的缝线、骨蜡残渣和修补用钛网,仔细观察硬脑膜是否严密缝合,有无CSF漏,必要时予以修补。此外,手术切口有可能损伤枕小神经而导致术后患侧枕部皮肤感觉障碍。
MVD术后无效或复发处理
以下内容引自“邓竹,张黎,于炎冰,刘睿全.三叉神经痛显微血管减压术无效或复发的原因与外科处理[J].中国微侵袭神经外科杂志,2019,24(11):525-528.”
三叉神经痛MVD术后无效的定义:术后疼痛减轻很少或没有减轻。一般疼痛复发的时间界定于术后1个月以上,而术后1个月以内疼痛仍无缓解则视为无效。对首次MVD术后无效和复发病例,初始治疗仍以药物治疗为首选。此类病人只有在使用药物无法控制症状或病人不能耐受药物副作用时,才考虑再次外科手术治疗。
![]()
原因分析
![]()
▼1.蛛网膜增厚黏连
首次MVD术后复发病例,在行二次手术探查时,部分病例三叉神经根处仅存在着严重蛛网膜黏连,且并未发现任何责任血管。
▼2.责任血管
以静脉或动脉联合静脉为责任血管的三叉神经痛病人,首次MVD术后更容易出现无效或复发。首次MVD术后复发三叉神经痛病人,在行二次手术探查时,可能发现三叉神经根处出现新的责任血管压迫,这些血管可是动脉、静脉或动脉联合静脉。
▼3.垫棉因素
如果首次MVD术中置入的垫开物体积过小或位置不当,责任血管搏动性压迫会通过垫棉冲击到三叉神经根,从而导致首次手术无效或复发。首次MVD术中置入Teflon或涤纶垫棉脱落或移位,均会导致之前被推开的责任血管再次压迫三叉神经根,从而导致三叉神经痛复发。垫棉也可因为体积过大或放置位置不当而直接对三叉神经根造成压迫,从而引起三叉神经痛无效或复发。
▼4.手术操作
在三叉神经痛病人的首次MVD时,术者手术经验、对手术细节的处理等,均会影响手术效果。首次MVD减压不充分,垫棉放置位置错误,置入过多垫棉等,都将可能导致术后无效或复发。AMADOR和POLLOCK在无效三叉神经痛病人的二次术中探查发现,存在首次MVD错误将面神经或听神经进行减压。
▼5.垫棉肉芽肿形成
垫棉肉芽肿造成首次MVD术后三叉神经痛复发是一个十分罕见的原因,其形成机制尚不明确,可能与垫棉周围局部慢性炎症反应有关。垫棉肉芽肿可黏附在血管、神经或脑干,造成三叉神经根扭曲甚至在三叉神经根上形成压迹,并最终引起三叉神经痛复发。
▼6.三叉神经痛病程
BARKER等研究发现从三叉神经痛发病到首次MVD,间隔时间超过8年的病人,往往预示着更高复发率。但也有学者观察发现三叉神经痛病程并不会影响MVD疗效。
▼7.中枢神经性疼痛
多发性硬化引起的三叉神经痛是中枢神经性疼痛的常见类型。多发性硬化的三叉神经痛病人采取MVD本身就存在着很大争议,多发性硬化病人行MVD治疗无效率与复发率,较特发性三叉神经痛明显升高。
▼8.其他原因
在首次MVD时,使用自体肌肉作为神经与责任血管之间的垫开物,术后常会发生三叉神经痛复发。在这样病例中进行二次手术探查发现,首次MVD放置的自体肌肉会包裹责任血管并且同时与三叉神经根黏连,导致血管搏动性压迫传导至神经。此外,有学者发现首次MVD术后三叉神经痛没有立即缓解的延迟治愈病例,其复发可能性也较大。部分复发的三叉神经痛病人在二次手术探查时,并无任何阳性发现,其复发原因不明确。
![]()
复发处理方法
![]()
▼1.二次MVD
三叉神经痛病人首次MVD无效或复发后,再次进行MVD治疗仍是一种很好的选择。二次术后67%~83.3%的病例可获长期治愈。但进行二次MVD时,手术难度和风险将会增大。在决定是否进行二次MVD前,病例评估和筛选至关重要:典型的三叉神经痛病人,首次MVD术后存在无痛间期,发现垫棉肉芽肿,MRI或MRTA提示三叉神经根处存在血管压迫等,均是进行二次MVD的手术指征。在进行二次MVD时,可沿原手术入路进入CPA,松解黏连蛛网膜,找到新的责任血管并放置新的垫棉进行减压。
对因垫棉肉芽肿形成而导致三叉神经痛复发的病人,在进行二次MVD时,应该完全切除肉芽肿,然后再置入新的垫棉进行减压。二次MVD术后常见并发症:面部麻木、听力丧失、面瘫、暂时性共济失调、脑脊液漏、无菌性脑膜炎与切口感染等。
▼2.乙状窦后入路三叉神经感觉根部分切断术
在首次MVD无效或复发的三叉神经痛病人中,特别是在进行二次乙状窦后入路手术探查时,并未发现任何责任血管压迫三叉神经根的病人,可行三叉神经感觉根部分切断术(partial sensory rhizotomy, PSR),术后长期治愈率约97%。故认为可将MVD联合PSR作为首次MVD术后三叉神经痛复发病人的首选治疗方案。
PSR术后最常见并发症是部分切断的三叉神经感觉根所支配的面部区域出现麻木,但随着时间推移这种面部麻木会出现一定程度好转,并不会影响病人生活质量。其他术后并发症包括:复视、听力障碍、面瘫、脑脊液漏等。
▼3.责任血管悬吊法
MVD时在责任血管和神经之间放置的垫开物会引起一些不良反应,这些不良反应可能会导致首次MVD术后三叉神经痛复发,因此,“责任血管悬吊法”可能比传统MVD会有更好疗效,也更加适用于首次手术后无效或复发的病例,术后中期治愈率几乎接近100%。“责任血管悬吊法”是使用丝线、动脉瘤夹、明胶海绵、生物蛋白胶等,将责任血管悬吊于邻近的小脑幕或颅壁硬膜,使责任血管远离三叉神经根,不使用或使用少量垫棉。
二次手术中,在三叉神经根处发现新形成的动脉血管袢压迫者,可采取这种方法,而对探查时发现严重蛛网膜黏连的病人并不适用。这与传统的MVD相比,在进行责任血管悬吊术过程中,需要更大的手术操作空间;同时,其所造成血管损伤的可能性也增大。
▼4.二次MVD联合三叉神经感觉根梳理术
对首次MVD无效或复发的三叉神经痛病人,可行二次MVD联合神经梳理术。沿原手术入路再次探查,先再次进行MVD,然后进行神经梳理术,沿三叉神经根纤维纵向进行梳理,术中使用切削刃为0.90mm的神经梳理术刀具松解神经纤维之间的黏连;术后中期治愈率约为93.75%。
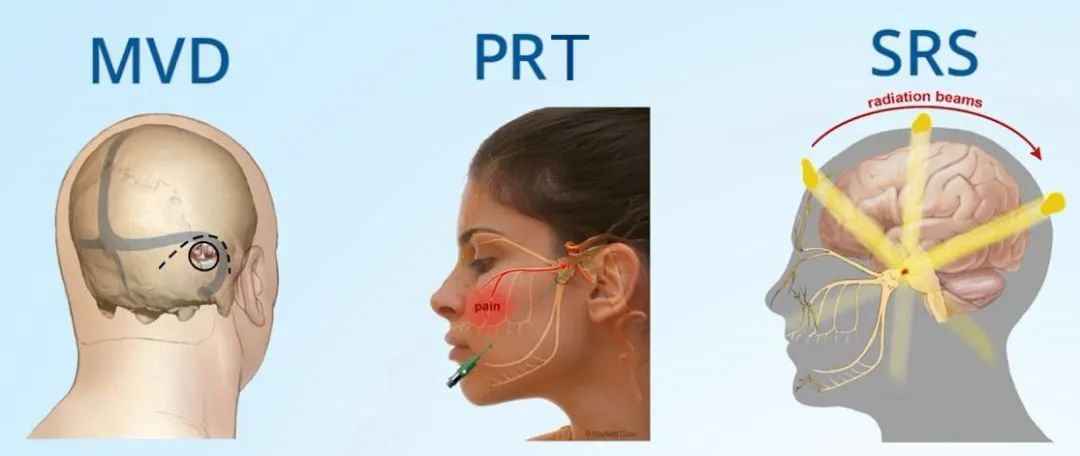
▼5.经皮穿刺三叉神经射频热凝术PRT
在CT引导下,经皮穿刺三叉神经射频热凝术(percutaneous radiofrequency thermocoagulation,PRT),术后长期治愈率仅为41%;通过CT扫描定位卵圆孔以确定最佳穿刺路线,插入22号5mm的射频绝缘针,当针到达卵圆孔时,以CT再次确认针的位置,将三叉神经半月节在75℃条件下射频热凝120s。PRT术后并发症包括:面部麻木、睁眼受限、无泪与味觉减退等,这些并发症会逐渐减轻,一般不会严重影响生活质量。
▼6.伽玛刀SRS
伽玛刀SRS手术可应用于包括MVD在内的其他手术方式治疗后复发或无效的三叉神经痛病人,术后短期治愈率为79.54%,但约49.11%病例会再次复发。对首次MVD术后无效或复发三叉神经痛病人进行伽玛刀治疗时,治疗总剂量可大于120Gy。也有部分学者认为安全剂量为70~90Gy。伽玛刀术后常见并发症:①面部麻木最常见,在少部分伽玛刀术后病人中,面部麻木程度可能难以忍受;总放射剂量与术后面部麻木程度有一定相关性;②面部感觉丧失,面部感觉迟钝;③角膜反射异常,角膜干燥;④咀嚼肌无力等。通常这些并发症会在术后1年内出现,并且会一直持续。
▼7.经皮穿刺三叉神经微球囊压迫术PBC
经皮穿刺三叉神经微球囊压迫术(percutaneous balloon compression, PBC)可应用于首次MVD术后无效或复发三叉神经痛,是有效、安全、经济的微创手术,术后中长期治愈率为82.7%~85.7%。术中使用C形臂进行定位,经卵圆孔穿刺将4号FOGARTY球囊导管缓慢推入Meckel腔,缓慢注入造影剂充盈球囊,同时边注射边调整球囊位置和形态,直到球囊最终变成倒梨形,球囊体积控制在0.4~0.8ml,球囊压迫时间目前尚无定论,对三叉神经痛复发病人可控制在4~8min,整个手术过程大约需要20min。PBC术后并发症包括:面部麻木(常见且可耐受)、咀嚼肌无力、感觉异常、痛性感觉丧失、继发于展神经麻痹的复视与单纯疱疹等。
希望对大家有所帮助。




