尽管神经介入进展很快,但非侵入性成像技术不能提供足够的分辨率来充分评估潜在的病理状态动脉、小穿支动脉以及器械引起的血小板聚集等。神经血管高频光学相干成像系统(HF-OCT)有可能解决以上问题,它可通过迂曲的脑血管,对颅内动脉进行全面的容积显微镜检,可用于神经血管器械的围手术期评估;为最佳血管内治疗提供依据。
——摘自文章章节
【REF:Ughi GJ, et al. Nat Commun. 2020 Jul 31;11(1):3851. doi: 10.1038/s41467-020-17702-7.】尽管在微创治疗方面取得了巨大的进步,但非侵入性成像技术不能提供足够的分辨率来充分评估潜在的病理状态动脉、小穿支动脉、以及器械引起的血小板聚集等。
具有整个神经血管装置和体内血管壁微结构的可视化显微成像可能对神经介入手术产生深远影响。具有微米级的分辨率并且可以在小型光纤探头中实现的内镜光学成像技术是应用于临床的有前景的技术。在过去十年中,光学相干断层扫描 (OCT)或光学频域成像(OFDI)已成为通用的模式,因为它能够准确测量冠状动脉管腔形态和疾病严重程度;OCT/OFDI已被广泛用于研究新一代冠状动脉内支架器械。除冠状动脉应用外,血管内成像还将彻底改变脑血管病的诊断和管理;然而,目前市售的成像导管缺乏在迂曲的脑血管解剖结构中推进所需的灵活性,也并非设计用于在迂曲程度高的情况,并且与神经介入临床工作不兼容。因此,在临床环境中使用血管内成像仅限于少数选定的有限迂曲患者的后循环和颈内动脉的近端、非迂曲节段。此外,现有装置的视野(即采集的图像直径)不足以描述直径为5mm或更大而且复杂的颈动脉以及颅内动脉瘤。在本研究中,我们引入了高频OCT(HF-OCT)成像系统,包括成像控制台和专为脑血管设计的光纤内镜探头,以满足临床需求,从而实现脑血管活体显微镜原位成像。
采用体外、体内实验,从以下几方面论证HF-OCT用于脑血管成像的可行性。
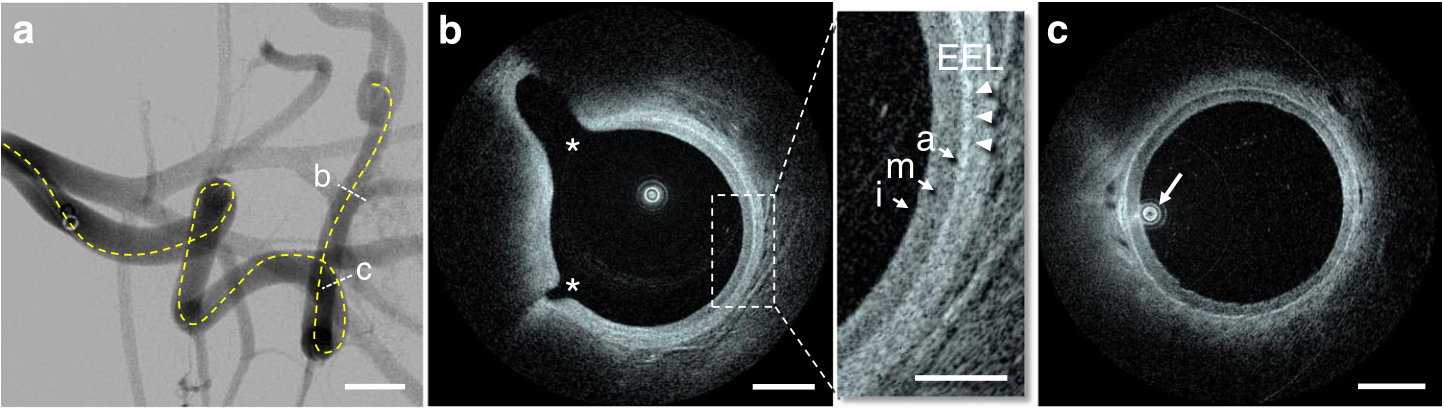
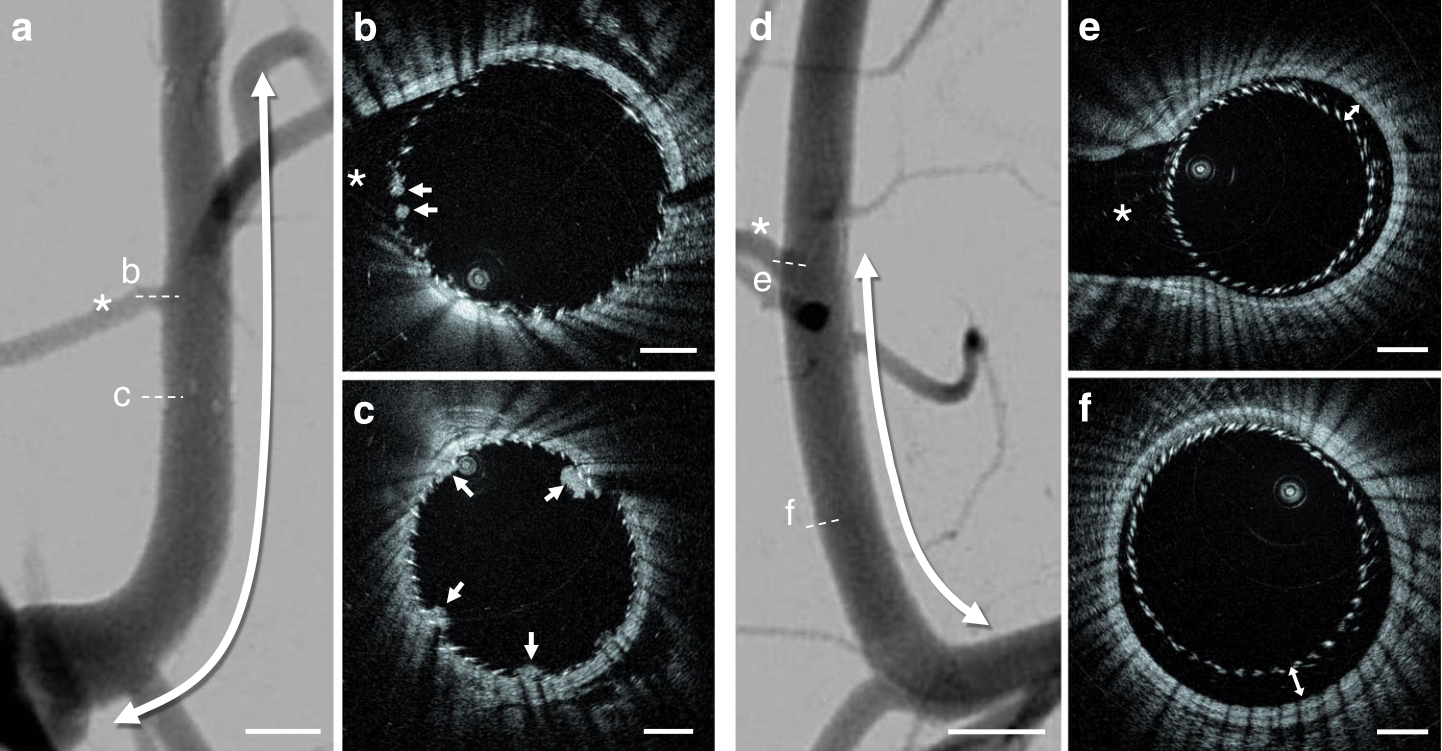
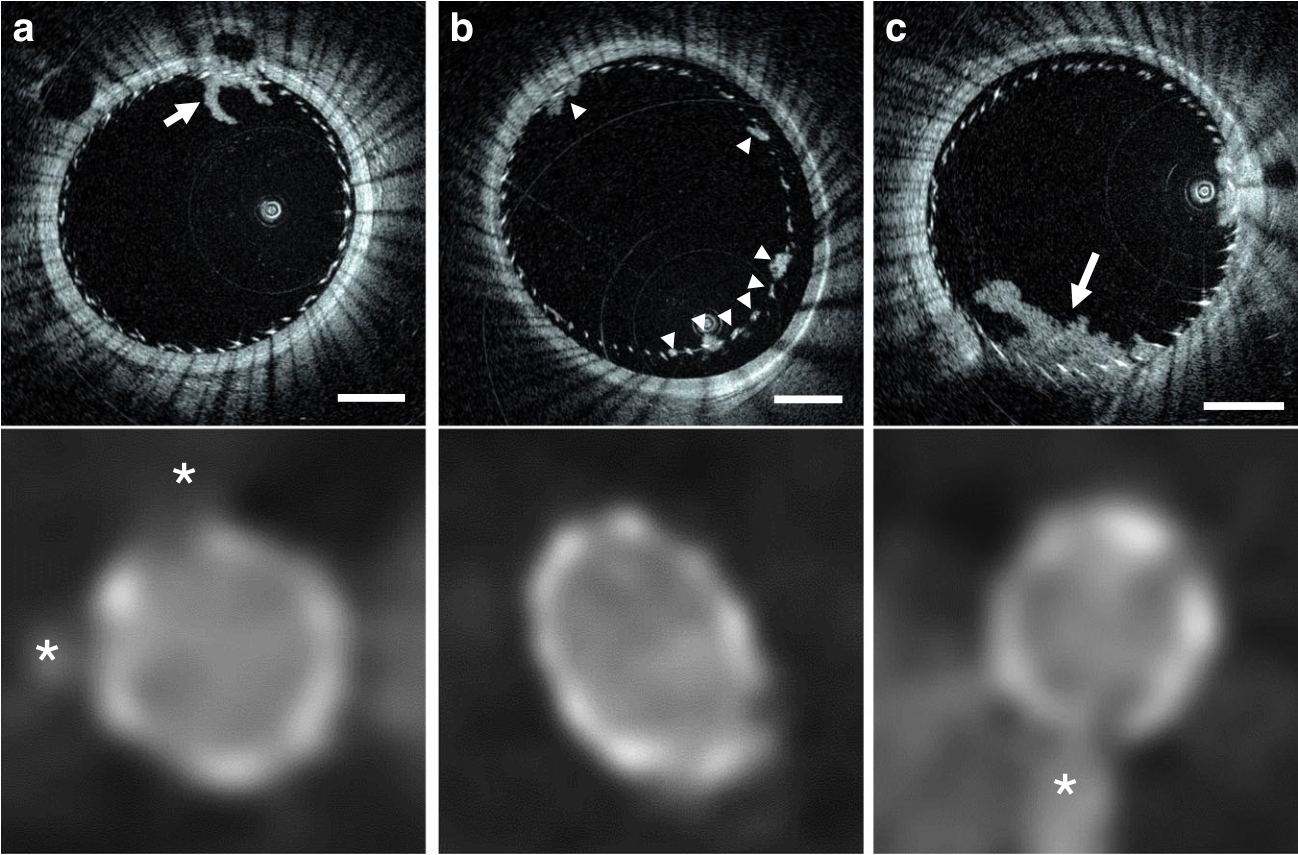
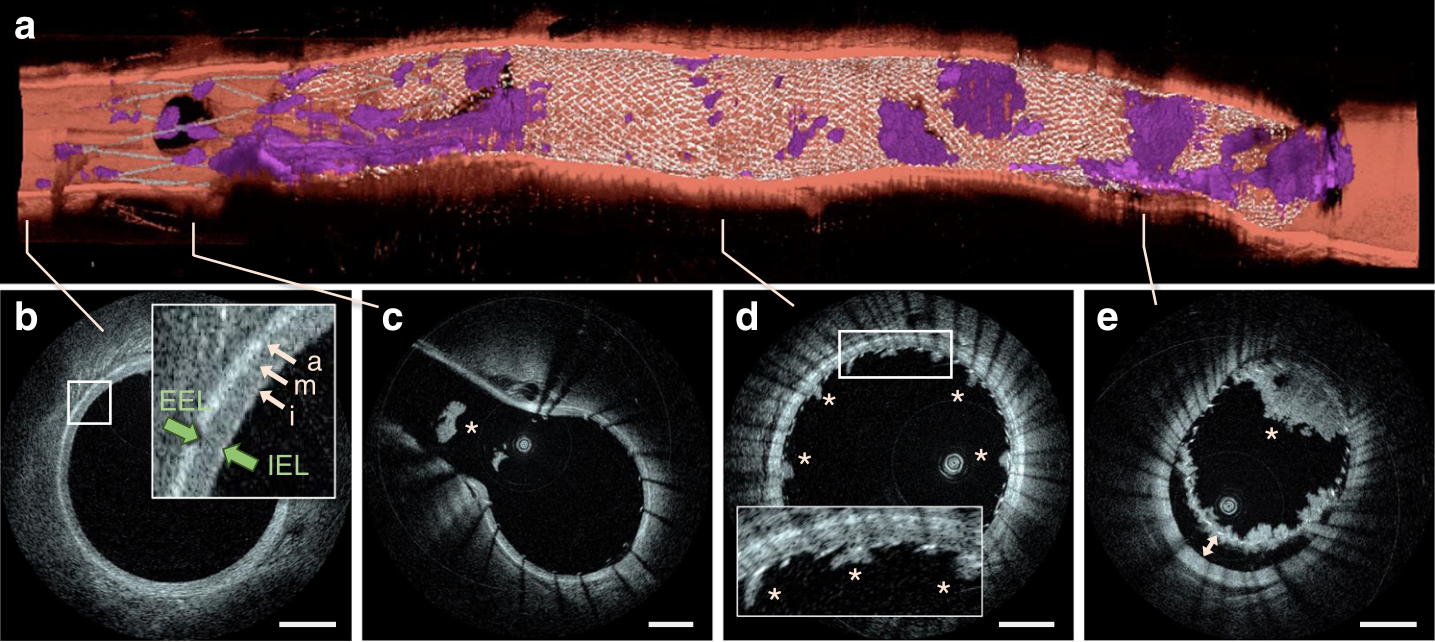
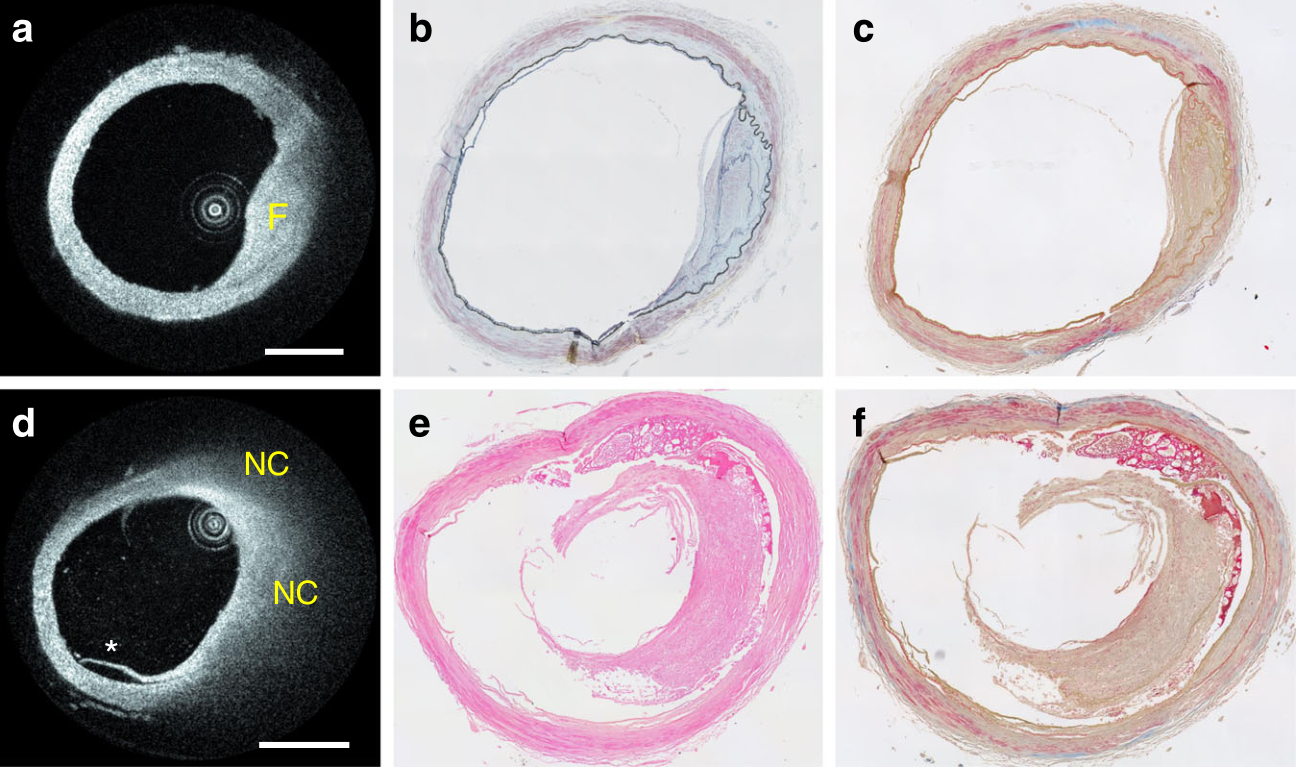
神经血管高分辨内镜成像系统。本研究中引入的探头被命名为Vis-M,是一种灵活的0.016英寸(~400µM)的金属丝样导管,用于在迂曲的颅内解剖结构中导航。与现有的血管内成像解决方案相反,Vis-M器械不需要导丝支持的导航,并且可以通过标准的血管导管输送(图1)。图1. 颅内血管的HF-OCT成像原理。在5F通路导管内短暂注射造影剂(蓝色)的过程中,Vis-M器械缩回,同时快速旋转其内部光学器件,进行螺旋扫描,获得动脉壁、神经血管器械和支架腔内物体的显微结构。Willis环体外模型中的血液清除。在完整Willis环的主要解剖位置上进行了模拟实验。Omnipaque 350被确定为首选造影剂,通常以5mL/s的速度灌注,并在注射约2-3s后观察颈内动脉(ICA)。大脑中动脉(MCA)和椎动脉(VA)的注射速率为3mL/s,基底动脉(BA)需要注射5mL/s。体内血管迂曲度升高的成像。迂曲的猪前肢模型(n=8)肱动脉血管严重迂曲,其曲率与人颈内动脉虹吸部相似。使用现有IV成像溶液进行成像,通过Vis-M器械(n=16),采集HF-OCT数据集,有效成像长度为65±13mm。通过评估迂曲解剖结构对IV成像中图像伪影的影响,如不均匀旋转失真(NURD),评价Vis-M器械的性能。在肱动脉迂曲度升高的情况下(n=16),HF-OCT数据集未观察到NURD伪影(图2)。均匀血管壁照明条件下的无失真成像可实现单个组织层的精确可视化,包括内弹性层和外弹性层、管腔精细解剖结构和两个侧支的开口(图2b、c)。图2. 猪肱动脉前肢弯曲模型的体内成像。a.虚线突出显示了Vis-M器械通过迂曲血管的路径。b. HF-OCT显示外弹力层(箭头)和单层血管壁(箭头)。明亮的内膜后是深色的中膜和明亮的外膜(插图)。星号表示两个侧支的开口,直径分别约为0.2和0.7mm。c.箭头表示HF-OCT设备在动脉腔中的偏心位置。图像显示照明均匀,无NURD伪影。本研究纳入的所有动物(n=8)总计16条动脉,弯曲猪前肢模型的血管成像可以重复获得。DSA图像上的比例尺等于1cm(a)。HF-OCT图像比例尺等于1mm(b和c),插图中为0.5mm。体内神经血管支架和血流导向装置的成像。在猪上颌内动脉(IMAX,n=16)植入血流导向装置(FDS,n=16)和自膨式颅内支架(ICS,n=15),通过对数字血管减影(DSA)图像、增强锥形CT(CBCT)图像和HF-OCT图像进行比较。使用Fleiss’kappa分析发现0.90(HF-OCT)、0.67(CBCT)和0.49(DSA)阈值可用于FDS表面的急性血栓形成评估。同样,发现0.87(HF-OCT)、0.67(CBCT)和0.18(DSA)的阈值用于诊断 FDS 贴壁不良。ICS器械的重复分析显示血栓积聚的一致性为0.81(HF-OCT)、0.39(CBCT)和0.71(DSA),贴壁不良的一致性值为0.78(HF-OCT)、0.45(CBCT)和0.41(DSA)。假设HF-OCT的观察是真实的,DSA图像上一半以上的病例为假阴性。FDS植入后的成像数据示例见图3。HF-OCT捕获了血栓的存在,不完全与器械并置(图3a)。同样准确描绘了被多个血栓覆盖的闭塞侧支,以及FDS边缘贴壁不良(图3b、c)。三维内镜数据显示待保护的两个血管分支a FDS(图3d),包括其开口上是否存在凝块(图3e、f)。HF-OCT和相应的DSA和CBCT数据显示在图4和图5中。小至30µm的血凝块(图4b、c和5b)、器械贴壁不良(图4e、f)和侧支血栓形成(图5a、c)被HF-OCT显微图像捕获,但在相应的DSA和CBCT图像上看不到。HF-OCT在体内评估神经血管器械微米级特征能力的进一步示例为如图6所示,包括两个重叠器械之间的相互作用。此外,由于FDS近端边缘贴壁不良导致的明显血栓形成,导致侧支开口血栓脱落和部分血管闭塞,如图6b,e所示。 图3. 猪上颌内动脉植入支架后HF-OCT容积显微结构。a. HF-OCT三维切片(顶部=远端;底部=近端)。血流导向装置表面可见贴壁不良(箭头)和不同大小的血凝块(紫色)。b.横断面HF-OCT成像显示一个血管分支(星号)和表面的血栓(箭头)。c.血流导向装置近端边缘,对合不完全(3点钟),装置表面有几个血凝块(箭头)。d.HF-OCT容积显示的内镜视图,可以看到被支架截留的小型穿支样侧支。e.图左侧示侧支(箭头)无血凝块,导向装置与载瘤动脉贴壁良好。f.图右侧示分支(用星号表示)示导向装置表面有血凝块。在16头猪的上颌内动脉中重复采集植入支架动脉的数据,包括16个血流导向装置和15个自膨式颅内支架。所有HF-OCT图像上的比例尺等于1mm。三维配色方案:红色,动脉壁;紫色,血凝块;银色,金属支柱。图4. HF-OCT成像与DSA的比较。使用分流支架和神经血管支架植入颌内动脉的数字减影血管造影术(DSA)。植入支架的节段由箭头指示,器械部分重叠。相应的HF-OCT图像显示,在x线透视下未观察到血栓形成(箭头),位于侧支b水平的分流栓支柱上,以及分流栓和重叠段颅内支架上。使用分流栓支架治疗的第2支IMAX动脉的DSA。相应的HF-OCT横截面图像描述了在DSA上未观察到的不同位置的器械贴壁不良,最大延伸约为0.35mm e和0.45mm f。在分流后(n=16)和自膨式颅内支架植入后(n=15),对所有猪上颌内动脉(n=16)重复进行了HF-OCT与DSA的比较。DSA图像上的比例尺等于5.0mm;HF-OCT比例尺等于1.0mm。图5. 横断面HF-OCT图像与相应CBCT切片的比较。a.在HF-OCT图像上可见侧支血栓形成(箭头)。b.在1点至8点之间的HF-OCT图像上可见最大严重度约为400µm的分流器贴壁不良。箭头表示分流支柱上的小血栓形成,厚度在~30到220µm之间。在相应的锥形束CT图像上通常无法检测到血栓和器械贴壁不良的存在。c.大侧支开口血栓形成。在分流(n=16)和自膨式颅内支架植入(n=15)后,对所有猪颌内动脉(n=16)重复进行了HF-OCT与CBCT的比较。HF-OCT图像上的比例尺等于1mm。CT图像上的星号符号(*)表示侧支的位置。图6. 颅内支架的HF-OCT容积显微镜检查与血流导向装置的远端部分重叠。a.三维渲染显示显著的血栓聚集。b. HF-OCT显微镜描绘血管壁微观结构,包括单血管层,包括明亮的内膜、低散射中膜和外膜(箭头)。内弹力层(IEL)和外弹力层(EEL)用绿色箭头表示。c.可见大分支内器械表面脱落的血栓,用星号表示。d.星号表示厚度在100-200µm之间的血栓形成,并分布在FDS表面。e.在FDS近端可见与显著贴壁不良(>500µm)相对应的血凝块形成。对共计15头猪的颌内动脉进行重复HF-OCT成像。比例尺等于1.0mm。三维内镜渲染配色方案:红色,动脉壁;紫色,凝块;银色,分流支架支柱;灰色,神经血管支架支柱。大动脉成像。为了研究HF-OCT对颈动脉成像的能力,在一个动物亚组中对猪颈总动脉进行了额外的支架植入术(n=5)。发现植入支架节段的平均直径为 5.5±0.3mm,最大直径为5.9mm。在所有情况下,Vis-M器械的扩展视场提供了充分的照明,可准确评估支架-血管在支柱水平上的相互作用。颅内动脉粥样硬化成像。在尸检时从有血管疾病史的70岁以上患者中获得病变颅内动脉节段(n=10)。专家图像阅读器识别了动脉节段的一个子集,包含三种主要斑块类型的代表性病例。发现了代表性的纤维化、纤维钙化和坏死核心 (NC)动脉粥样硬化疾病病例(n=3)。通过组织病理学技术处理组织,并使用苏丹黑、苏木精和伊红(H&E)等染色。对HF-OCT成像结果设盲的血管病理学家分析染色切片,并标识斑块和组织类型。图7a显示了位于97岁尸体MCA M1段的纤维斑块。在HF-OCT图像上,纤维化组织被确定为动脉壁的较厚区域,在近红外光谱中表现出光学背向散射升高和强度均匀。组织病理学评估将该斑块归类为主要由纤维化组织组成(图7b、c)。图7d显示了含有NC的二个斑块。在HF-OCT图像上,NC被识别为纤维帽覆盖的动脉粥样硬化斑块内边界轮廓不清的信号缺乏区域,坏死组织在近红外范围内呈现强烈的光学衰减,导致图像强度信号随进入组织的距离增大而快速下降,影响位于后方的血管壁区域。与HF-OCT结果一致,组织病理学将该斑块归类为含有NC和潜在中膜变性的纤维化(图7e、f)。最后,在86岁尸体的硬膜内椎动脉远端节段发现了一个纤维斑块。HF-OCT显示纤维钙化斑块,含有纤维化和钙化组织的证据,其特征为信号缺乏和异质性区域,边界清晰。钙化斑块,圆周分布87°最大厚度约为 900µm,如图8b所示。钙组织在近红外范围内呈现较低的后向散射和衰减系数,因此HF-OCT可以准确对厚度和周向分布可视化。组织病理学评估将该斑块大部分归类为钙斑,与HF-OCT图像评估一致,有潜在中膜变性和正性重塑的证据。图7. MCA动脉离体节段的颅内斑块。b.纤维化斑块的HF-OCT成像以及相应的三色和Movat染色。c.纤维化组织的HF-OCT特征为均质信号区域,由后向散射升高和光学衰减系数降低所致。d.坏死核心斑块的HF-OCT成像以及相应的H&E。e.和Movat染色。f.在HF-OCT图像上,坏死核心斑块的特征是边界不清晰的区域,随后是动脉粥样硬化斑块内的光学衰减系数升高。星号表示血管壁夹层。在10例颅内动脉尸体标本中,共识别出3个代表性动脉粥样硬化斑块,处理后进行组织病理学分析,并与HF-OCT成像进行比较。比例尺等于1.0mm。图8. 硬膜内椎动脉节段的颅内钙化斑块。a.图像中可见2个钙化斑块。钙厚度在100-300µm之间,较小斑块位于11点钟位置。最大钙厚度为900µm的较大斑块位于图像的左下象限。b.放大显示斑块微观结构的细节,包括内外边界。在HF-OCT上,钙组织的特征是边界清晰的区域,信号较弱且不均匀,这是由于低光学反向散射和低吸收系数所致。
图3. 猪上颌内动脉植入支架后HF-OCT容积显微结构。a. HF-OCT三维切片(顶部=远端;底部=近端)。血流导向装置表面可见贴壁不良(箭头)和不同大小的血凝块(紫色)。b.横断面HF-OCT成像显示一个血管分支(星号)和表面的血栓(箭头)。c.血流导向装置近端边缘,对合不完全(3点钟),装置表面有几个血凝块(箭头)。d.HF-OCT容积显示的内镜视图,可以看到被支架截留的小型穿支样侧支。e.图左侧示侧支(箭头)无血凝块,导向装置与载瘤动脉贴壁良好。f.图右侧示分支(用星号表示)示导向装置表面有血凝块。在16头猪的上颌内动脉中重复采集植入支架动脉的数据,包括16个血流导向装置和15个自膨式颅内支架。所有HF-OCT图像上的比例尺等于1mm。三维配色方案:红色,动脉壁;紫色,血凝块;银色,金属支柱。图4. HF-OCT成像与DSA的比较。使用分流支架和神经血管支架植入颌内动脉的数字减影血管造影术(DSA)。植入支架的节段由箭头指示,器械部分重叠。相应的HF-OCT图像显示,在x线透视下未观察到血栓形成(箭头),位于侧支b水平的分流栓支柱上,以及分流栓和重叠段颅内支架上。使用分流栓支架治疗的第2支IMAX动脉的DSA。相应的HF-OCT横截面图像描述了在DSA上未观察到的不同位置的器械贴壁不良,最大延伸约为0.35mm e和0.45mm f。在分流后(n=16)和自膨式颅内支架植入后(n=15),对所有猪上颌内动脉(n=16)重复进行了HF-OCT与DSA的比较。DSA图像上的比例尺等于5.0mm;HF-OCT比例尺等于1.0mm。图5. 横断面HF-OCT图像与相应CBCT切片的比较。a.在HF-OCT图像上可见侧支血栓形成(箭头)。b.在1点至8点之间的HF-OCT图像上可见最大严重度约为400µm的分流器贴壁不良。箭头表示分流支柱上的小血栓形成,厚度在~30到220µm之间。在相应的锥形束CT图像上通常无法检测到血栓和器械贴壁不良的存在。c.大侧支开口血栓形成。在分流(n=16)和自膨式颅内支架植入(n=15)后,对所有猪颌内动脉(n=16)重复进行了HF-OCT与CBCT的比较。HF-OCT图像上的比例尺等于1mm。CT图像上的星号符号(*)表示侧支的位置。图6. 颅内支架的HF-OCT容积显微镜检查与血流导向装置的远端部分重叠。a.三维渲染显示显著的血栓聚集。b. HF-OCT显微镜描绘血管壁微观结构,包括单血管层,包括明亮的内膜、低散射中膜和外膜(箭头)。内弹力层(IEL)和外弹力层(EEL)用绿色箭头表示。c.可见大分支内器械表面脱落的血栓,用星号表示。d.星号表示厚度在100-200µm之间的血栓形成,并分布在FDS表面。e.在FDS近端可见与显著贴壁不良(>500µm)相对应的血凝块形成。对共计15头猪的颌内动脉进行重复HF-OCT成像。比例尺等于1.0mm。三维内镜渲染配色方案:红色,动脉壁;紫色,凝块;银色,分流支架支柱;灰色,神经血管支架支柱。大动脉成像。为了研究HF-OCT对颈动脉成像的能力,在一个动物亚组中对猪颈总动脉进行了额外的支架植入术(n=5)。发现植入支架节段的平均直径为 5.5±0.3mm,最大直径为5.9mm。在所有情况下,Vis-M器械的扩展视场提供了充分的照明,可准确评估支架-血管在支柱水平上的相互作用。颅内动脉粥样硬化成像。在尸检时从有血管疾病史的70岁以上患者中获得病变颅内动脉节段(n=10)。专家图像阅读器识别了动脉节段的一个子集,包含三种主要斑块类型的代表性病例。发现了代表性的纤维化、纤维钙化和坏死核心 (NC)动脉粥样硬化疾病病例(n=3)。通过组织病理学技术处理组织,并使用苏丹黑、苏木精和伊红(H&E)等染色。对HF-OCT成像结果设盲的血管病理学家分析染色切片,并标识斑块和组织类型。图7a显示了位于97岁尸体MCA M1段的纤维斑块。在HF-OCT图像上,纤维化组织被确定为动脉壁的较厚区域,在近红外光谱中表现出光学背向散射升高和强度均匀。组织病理学评估将该斑块归类为主要由纤维化组织组成(图7b、c)。图7d显示了含有NC的二个斑块。在HF-OCT图像上,NC被识别为纤维帽覆盖的动脉粥样硬化斑块内边界轮廓不清的信号缺乏区域,坏死组织在近红外范围内呈现强烈的光学衰减,导致图像强度信号随进入组织的距离增大而快速下降,影响位于后方的血管壁区域。与HF-OCT结果一致,组织病理学将该斑块归类为含有NC和潜在中膜变性的纤维化(图7e、f)。最后,在86岁尸体的硬膜内椎动脉远端节段发现了一个纤维斑块。HF-OCT显示纤维钙化斑块,含有纤维化和钙化组织的证据,其特征为信号缺乏和异质性区域,边界清晰。钙化斑块,圆周分布87°最大厚度约为 900µm,如图8b所示。钙组织在近红外范围内呈现较低的后向散射和衰减系数,因此HF-OCT可以准确对厚度和周向分布可视化。组织病理学评估将该斑块大部分归类为钙斑,与HF-OCT图像评估一致,有潜在中膜变性和正性重塑的证据。图7. MCA动脉离体节段的颅内斑块。b.纤维化斑块的HF-OCT成像以及相应的三色和Movat染色。c.纤维化组织的HF-OCT特征为均质信号区域,由后向散射升高和光学衰减系数降低所致。d.坏死核心斑块的HF-OCT成像以及相应的H&E。e.和Movat染色。f.在HF-OCT图像上,坏死核心斑块的特征是边界不清晰的区域,随后是动脉粥样硬化斑块内的光学衰减系数升高。星号表示血管壁夹层。在10例颅内动脉尸体标本中,共识别出3个代表性动脉粥样硬化斑块,处理后进行组织病理学分析,并与HF-OCT成像进行比较。比例尺等于1.0mm。图8. 硬膜内椎动脉节段的颅内钙化斑块。a.图像中可见2个钙化斑块。钙厚度在100-300µm之间,较小斑块位于11点钟位置。最大钙厚度为900µm的较大斑块位于图像的左下象限。b.放大显示斑块微观结构的细节,包括内外边界。在HF-OCT上,钙组织的特征是边界清晰的区域,信号较弱且不均匀,这是由于低光学反向散射和低吸收系数所致。高分辨率IV成像可提供充分的空间分辨率,在最先进的临床成像模式无法观察到的支架水平上显示神经血管和治疗器械的细节。本研究提供的数据说明神经血管 HF-OCT系统(包括小型化、灵活的血管内成像探头)能够对颅内动脉进行全面的容积显微镜检。使用完整Willis环的患者特异性体外模型,我们提出了可转换造影剂注射方案,允许在不同的神经血管解剖位置进行IV光学成像。在动物模型中,我们收集了Vis-M器械用于高度血管迂曲度的适用性证据,这与无法可靠使用现有IV成像设备的在ICA所遇到的迂曲条件类似。与DSA和CBCT等最先进的成像模式相比,HF-OCT容积显微镜检在量化管腔内血凝块和评估神经血管器械与动脉壁之间相互作用的优势明显。此外,我们阐明了HF-OCT可视化血管壁微观结构的能力,包括颅内动脉粥样硬化的特征。综上所述,本研究结果为脑血管高分辨率血管内成像的临床转化铺平了道路。
神经血管HF-OCT系统可对动脉壁进行容积显微镜检,分辨率接近10µm。本研究已经表明,高分辨率IV成像可以在体内支架水平准确识别腔内血栓和神经血管器械。这些迂曲血管解剖结构成像结果表明,HF-OCT可在临床上用于神经血管器械的围手术期评估,以便能够展开相应处理措施,如GPIIb/IIIa抑制剂的局部给药、血管成形术或支架植入术。同时在血管造影结果模棱两可,而非侵入性成像技术无法实现的情况下,本系统优越的分辨率可实现血管夹层和支架-血管相互作用的可视化。对颅内动脉粥样硬化斑块类型的准确成像可以为治疗决策提供信息,并能够调整支架尺寸、植入策略以及与穿支动脉和残余狭窄的相互作用,以改善颅内动脉狭窄的血管内治疗。此外,HF-OCT的脑血管容积显微镜检能够在血管内治疗后进行更智能、图像引导式、个性化的抗血栓治疗。其增强的分辨率能够在高水平上研究血管和动脉瘤对植入器械的愈合反应,以体内显微镜的精确度和准确性评估器械表面上的组织厚度和血管重塑。因此,脑血管HF-OCT在临床实践中的使用为监测器械愈合、评估内皮过度生长和内膜增生提供了巨大潜力,为血管内治疗后的最佳抗血小板治疗提供了依据;同时HF-OCT将提供关键信息,支持下一代神经血管器械的开发和发展。