《Neuroendocrinology》2019年4月刊载(109(1):70-76.)法国Jacqueline Trouillas,Etienne Delgrange,Anne Wierinckx,等撰写的综述 《泌乳素细胞瘤进袭性的临床、病理和分子因素。Clinical, Pathological, and Molecular Factors of Aggressiveness in Lactotroph Tumours》( doi: 10.1159/000499382. )。
泌乳素肿瘤的行为在良性肿瘤、经治疗治愈的肿瘤、进袭性肿瘤和有转移的垂体癌之间是不同的。对临床、病理和分子因素的识别,对于早期识别可能患有这种进袭性肿瘤的患者是至关重要的。血浆泌乳素水平、肿瘤大小和肿瘤侵袭性本身,并不是影响预后的因素。然而,肿瘤出现在年轻时(<20岁),尤其是男孩中,而且存在遗传易感性(genetic predisposition)则预后较差。此外,男性的泌乳素瘤与女性的不同,它们较大,更具侵袭性,并且对多巴胺激动剂耐药。它们也常常是高级别的伴有复发和恶性的高风险。雌激素受体α的表达低于女性,与进袭性密切相关。增殖性标志物(Ki-67表达:≧3%,有丝分裂计数n >2)与侵袭性和增殖性相关,但单独来看,其预后价值尚存争议。基于5级分层的临床病理分类,并考虑到侵袭性和增殖性,2b级(进袭性)泌乳素细胞肿瘤与1a级(良性)肿瘤相比,有20倍的进展风险。此外,泌乳素肿瘤是第二常见的进袭性恶性肿瘤。其他因素,如生长因子的表达(血管内皮生长因子[VEGF]和表皮生长因子[EGF]),基因调节侵袭、分化和增殖,粘附分子(E-钙粘蛋白)、基质金属蛋白酶9,和染色体异常(染色体11、19和1),也与进袭性相关。目前,临床症状、预后分类、分子和遗传标记都可以帮助临床医师早期识别进袭性泌乳素瘤并促使对其进行分层管理。
1
引言
泌乳素细胞瘤(Lactotroph tumours)(泌乳素腺瘤[prolactinomas]或分泌泌乳素[PRL]的腺瘤)是垂体神经内分泌肿瘤(PitNETs)中最常见的亚型,约占所有垂体分泌性肿瘤的30% - 45%。女性明显较男性占优势,为10:1。泌乳素细胞瘤通常被认为是良性的。然而,这些肿瘤的行为从通过多巴胺激动剂(DA)治疗或手术治愈的微腺瘤,到进袭性和伴有转移的恶性肿瘤,差异很大。最近发现,泌乳素细胞肿瘤是第二常见的进袭性肿瘤和垂体癌(恶性肿瘤)。对临床、病理和分子因素的识别对于识别患有进袭性泌乳素肿瘤的患者是至关重要的,以便能够实施强化治疗和仔细的长期随访。在Gurlek等的极好的综述12年后,在这篇综述中,基于文献和我们的个人研究,我们还努力回答以下问题:“我们能否确定泌乳素细胞瘤的进袭性因素?”。
1
临床和生物学因素
年龄,血浆泌乳素水平,肿瘤大小和侵袭性
年纪轻(<20岁)与大的和侵袭性泌乳素细胞瘤有关。在一个年轻的患者,这样的肿瘤应该促使探索可能的遗传易感性(MEN1或AIP突变),这是与较差的预后相关的。
PRL水平与肿瘤大小之间存在相关性,而高PRL水平与手术结果不佳相关,虽然它不是多巴胺激动剂(DA)治疗反应的独立预测因子。相反,相对于肿瘤大小而言,PRL水平较低可能是分化不良的标志。然而,必须记住,这是一种罕见的可能性。通常,一个大的肿瘤与PRL血浆水平<200ng /mL是由于垂体柄阻断(stalk disconnection)。巨泌乳素细胞肿瘤通常对多巴胺激动剂(DA)治疗反应良好,PRL水平完全正常化,肿瘤显著缩小。然而,大的肿瘤更有可能是侵袭性的。海绵窦的侵袭是药物治疗耐药的独立预测因子。然而,肿瘤的大小或侵袭本身,并不能预测肿瘤的进袭行行为。
1
泌乳素细胞肿瘤与性别
自20世纪80年代以来,神经外科医生已经注意到,男性的泌乳素细胞肿瘤通常比女性的更大,手术治愈的几率较低。这些差异与男性患者的诊断延迟有关。事实上,育龄妇女通常会出现泌乳素微腺瘤,而男性和绝经后妇女通常会出现泌乳素大腺瘤。由于男性的症状不太明显而导致诊断延迟时间较久,可能与这个现象有关,但这并不是全部的解释。事实上,肿瘤大小的差异在儿童年纪很小的时候就已经存在了。男孩的肿瘤明显比女孩的更大,更经常具有侵袭性(分别为70%和38%),迄今为止报道的所有年龄<15岁的儿童的巨腺瘤病例都是男孩。我们还发现,当诊断时的年龄和症状持续时间相关联时,男性的肿瘤比女性的更大。有意思的是,男性和女性的泌乳素细胞肿瘤在磁共振成像上表现出不同的特征,T2加权成像低信号强度几乎只在男性中有发现。综上所述,这些研究证明肿瘤行为的性别差异。除了体积较大之外,男性的泌乳素细胞肿瘤更经常侵袭海绵窦,有较高的Ki-67指数,而且更经常血管化良好(well-vascularized)。与女性相比,男性的肿瘤对多巴胺激动剂的治疗更容易产生耐药性,并且在临床上表现出更强的进袭性病程,如术后更频繁的复发,在(多巴胺激动剂和放疗)治疗中肿瘤进展,并且更频繁地发展为垂体癌。一般来说,在男性,泌乳素细胞瘤表达较低水平的雌激素受体(ER) -α。这一发现可以用较低的分化程度来解释。此外,在一些动物模型中,雌激素已经被证明可以抑制肿瘤的生长。这种雌激素的抑制作用可能解释了巨泌乳素瘤在年轻和老年女性中的双峰分布。因此,在男性和绝经后女性中,ERα的低表达,结合低雌激素的产生,可能会促进增殖,导致高级别(2b级)肿瘤的发生。从此,临床和生物学上的性别相关差异已被分子和遗传学研究证实(见下文)(图1)。在2017年世界卫生组织分型中,男性泌乳素细胞瘤被确定为“通常表现出进袭性行为的”泌乳素细胞瘤,需要密切随访。
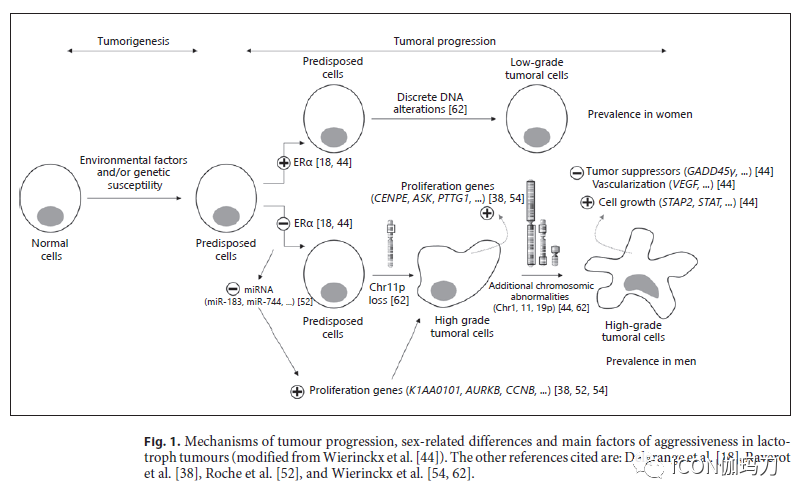
图1.泌乳素细胞瘤的肿瘤进展机制、性别相关差异及主要进袭性因素。
1
对多巴胺激动剂耐药
多巴胺激动剂治疗是泌乳素细胞肿瘤的一线治疗方法,特别是在有鞍区以外外伸展的情况下。尽管长时间高剂量治疗,血清PRL水平仍未完全正常化的情况很少见(约10%),但相比对多巴胺激动剂敏感的肿瘤,这些肿瘤表现出更严重的临床病程。对多巴胺激动剂耐药的肿瘤比对多巴胺激动剂有反应的肿瘤更大,更常有侵袭性,与其他泌乳素细胞肿瘤相比,它们的Ki-67指数和有丝分裂计数更高。即使只考虑大腺瘤,对多巴胺激动剂耐药的泌乳素细胞瘤也常见于男性。已报道进袭性或恶性肿瘤中的原发性或继发性对多巴胺激动剂的耐药。这可能与与进袭性或恶性肿瘤相关的去分化有关。事实上,这种抵抗可能是由于D2受体(D2R)的低表达。这一假设是基于体外和发生侵袭性泌乳素细胞瘤的D2R敲除(KO)转基因小鼠的动物模型研究。在一组对多巴胺激动剂耐药的的泌乳素细胞瘤中,报道没有D2R的基因突变。由于缺乏特异性的商业抗体,使用免疫组织化学(IHC)分析D2R还不可能。因此,对多巴胺激动剂耐药需要密切的患者随访,以及更积极的治疗,如手术和放疗。
1
病理标志物
增殖性标志物
Ki-67,在整个细胞周期中表达,现在可以使用单克隆抗体(Mib-1)的免疫组化(IHC),在常规组织病理学中检测到。Ki-67指数,定义为Ki-67阳性细胞核的百分比,是一种简单、可靠、可重复的方法。虽然管其与肿瘤生长和侵袭性的相关性可能存在争议,但Ki- 67指数截断值≧3%,被认为是增殖性的标志。
有丝分裂数也是快速生长的重要预测因子。如果观察到每10个高倍镜视野下的有丝分裂计数>2个,垂体瘤被认为具有增殖性。有丝分裂计>2和Ki-67指数≧3%已被发现与多巴胺激动剂耐药和侵袭性泌乳素细胞瘤相关,尤其是在男性中。
有报道p53肿瘤抑制基因产物的表达是许多癌症的重要标志物。然而,p53突变在垂体肿瘤中尚未被描述,其检测价值因伴随的技术问题而存在争议。
垂体肿瘤转化基因(PTTG)是有丝分裂期间调控姐妹染色单体分离(sister chromatid separation)的分离酶抑制蛋白(securin)家族成员,也被发现与非侵袭性的泌乳素细胞瘤相比,在侵袭性泌乳素细胞瘤中过表达。
1
临床病理的五级分层的分类
我们提出了一种新的临床病理,5级分层的垂体神经内分泌肿瘤(PitNETs)分类,考虑到侵袭性(通过垂体影像评估),免疫组织学亚型,和增殖性标记(Ki-67指数,有丝分裂计数,和p53阳性)。肿瘤按大小(微腺瘤、大腺瘤和巨腺瘤)、类型(生长激素细胞、泌乳素细胞、促肾上腺皮质激素细胞、促性腺激素细胞、和促甲状腺素细胞)和级别(1a:无侵袭性;1b:无侵袭性,有增殖性;2a:有侵袭性;2b:有侵袭性,有增殖性;3:转移性)进行分类。一项大型回顾性队列的病例对照研究在统计学上证实了这种分类的预后价值。最近的一项前瞻性研究和其他2项独立回顾性研究也证实了这一点。必须强调的是,绝大多数垂体肿瘤是良性的,可以通过手术或药物治疗治愈。在泌乳素细胞瘤中,1a级(良性)和2b级(进袭性)肿瘤的发生率分别为56%和16%。在随访中,2b级肿瘤的复发或进展风险比[1a级肿瘤高20倍。这些结果证实了我们先前的观察。
1
进袭性和恶性泌乳素细胞瘤
进袭性肿瘤被定义为“生长迅速、对标准治疗(药物治疗、手术和放射治疗)耐药抵抗、反复复发或进展的侵袭性肿瘤”。在手术系列中,2b级肿瘤的发生率约为所有类型肿瘤的10%,但根据先前的定义,临床上认为2%的肿瘤具有进袭性。到目前为止,只有极少数有转移的肿瘤被认为是恶性的,被称为垂体癌(0.2%)。但进袭性肿瘤与垂体癌之间的差异尚不清楚,我们建议将2b级肿瘤作为“疑似恶性肿瘤(tumour suspected of malignancy)”考虑。最近假设进袭性肿瘤和垂体癌是同一枚硬币的两个面,进袭性肿瘤或2b级肿瘤代表“具有恶性潜能(with malignant potential)”的肿瘤。泌乳素细胞瘤是是仅次于促肾上腺皮质激素细胞肿瘤的第二常见的进袭性肿瘤和恶性肿瘤,其发生率分别为20和37%。为了阐明进展和恶性的机制和因素,重要的是比较在初次出现时和重复手术后的肿瘤情况,如有时所作的。良性肿瘤和进袭性肿瘤的比较也很重要。由于这些原因,我们的研究集中在这类垂体肿瘤上。
分子和遗传标志物
分子和遗传技术(转录组、比较遗传杂交和表观遗传学)的最新进展使垂体肿瘤基因表达变异(microRNA和mRNA)的识别、杂合性缺失和基因突变的检测成为可能。迄今为止,对它们的检测仅在研究层面上进行。
雌激素受体
正常的泌乳素细胞和大多数泌乳素细胞瘤一般表达ERα。ER α表达与肿瘤大小相关。使用免疫组化和微阵列技术,我们证明尤其是在男性患者中,ERα表达的低水平。81例患者的临床和病理相关性显示ER低表达(IHC评分<6)与肿瘤大小和侵袭性、Ki-67指数、有丝分裂计数、p53表达、高肿瘤级别(2b级)、手术治愈、多巴胺激动剂耐药性以及肿瘤进展,有统计学意义的相关性。如果这在其他系列中得到验证,ER免疫染色可以作为预后标志物,并对泌乳素细胞瘤系统地检测。此外,发现在男性和女性中有表达差异的许多基因属于ER通路,其中3个基因(CTAG2、FGF13和VEGF)位于X染色体上。许多与ER相关的候选基因,如被雌激素抑制的转运体SLC6A8,也在男性中过表达。因此,在男性进袭性和恶性泌乳素细胞瘤中观察到的ER基因表达可能导致性别差异。然而,其他基因,如在男性泌乳素细胞瘤中有差异上调的FGF13,也可能导致男性泌乳素细胞瘤的进袭性行为。
生长因子
血管内皮生长因子(VEGF)及其受体(VEGFR)调节细胞生长、细胞分化、内皮迁移和血管生成。使用多种方法(免疫组化IHC、蛋白质印迹Western blot和荧光定量qRT-PCR),已经显示血管内皮生长因子(VEGF)在许多泌乳素细胞瘤中的过表达。血管内皮生长因子(VEGF)在男性中的表达也高于女性,在垂体癌中表达高于良性腺瘤。恶性泌乳素细胞瘤说明VEGF的重要性。此肿瘤显示新生血管生成,伴内皮细胞特异分子(endocan)的内皮细胞表达。这种由内皮细胞分泌并由VEGF和成纤维细胞生长因子控制的蛋白多糖(proteoglycan)与垂体肿瘤的侵袭和进展有关。因此,VEGF在泌乳素细胞肿瘤中的过表达可能具有治疗价值。事实上,也有报道称抗VEGF治疗(贝伐珠单抗bevacizumab)稳定了垂体癌的进展,并引起广泛的血管周围纤维化。此外,研究发现,76.5%的泌乳素细胞瘤中存在EGF结合位点,且在侵袭性肿瘤中比非侵袭性肿瘤有更频繁表达。因此,这一途径也可能是进袭性泌乳素细胞瘤的治疗靶点。事实上,拉帕替尼(lapatinib),一种针对EGFR和erbB2酪氨酸激酶的酪氨酸激酶抑制剂,在2名对大剂量卡麦角林耐药的患者中被证明可以抑制PRL分泌。
增殖性和侵袭性基因
进袭性(2b级)和非进袭性(1a级和2a级)泌乳细胞瘤证明7个基因的表达与侵袭性(ADAMTS6和CRMP1)或增殖性(PTTG,ASK,CCNB1 AURKB, CENPE)有牵连(implicate),且与侵袭性、病理分类、持久性和疾病的进展相关。此外,在进袭性和4个 microRNAs(miRNAs)的表达水平之间存在逆相关性: miR - 183作为抗增殖基因通过直接靶向KIAA0101起作用, miR - 340及其靶基因(NEK2、AURKB和CCNB2), miR - 744及其靶基因(TGFB1)和miR - 98及其靶基因(CENPK、UBE2T E2F2)。4个基因(CENPE、AURKB、CCNB1和ADAMTS6)与CTAG2上调相关,而CTAG2已被证实与乳腺癌的侵袭性有关。这些基因的差异表达和参与增殖和侵袭的miRNA表达的调节可能在肿瘤的侵袭性中发挥作用。
粘附分子和金属蛋白酶
钙粘蛋白/β-连环蛋白复合物被认为是“一个侵袭性抑制系统”。其在侵袭性泌乳素细胞瘤中的表达低于非侵袭性泌乳素细胞瘤中,其在男性中的表达低于在女性中的。
基质金属蛋白酶(MMPs)是一类酶,其可以降解基底膜从而促进肿瘤的侵袭,同时也有助于内皮细胞的迁移。基质金属蛋白酶(MMPs)的活性受金属蛋白酶(TIMPs)组织抑制因子的调控。已经证明MMP9的表达与血管生成相关。研究发现,MMP9在侵袭性泌乳素细胞瘤和垂体癌中的表达高于非侵袭性肿瘤。相反,与侵袭性腺瘤相比,MMP抑制剂TIMP-2在非侵袭性肿瘤中过表达。这些观察结果提示MMPs可能在泌乳素细胞瘤的进袭性中发挥重要作用。
染色体异常
杂合性缺失,特别是在11号染色体(Chr11)中,在侵袭性肿瘤中比非侵袭性肿瘤中更为常见。具体来说,在进袭性泌乳素细胞瘤(2b级)中,Chr11p区域通常缺失;随访期间,在3例发生转移的进袭性肿瘤中观察到整个Chr11缺失和1q增加,因此被认为是恶性的。Menin基因所在的Chr11异常可能与MEN1患者的泌乳素细胞瘤发生频率有关。在男性的进袭性泌乳素细胞瘤中观察到Chr19的增加。也有报道有过表达的HMGA2的Chr12三染色体细胞位于这条染色体上。
因此,分子和遗传分析有助于识别新的进袭性肿瘤或恶性肿瘤标志物,并阐明肿瘤进展机制和性别相关差异(图1)。

1
结论
泌乳素细胞瘤的类型多种多样,大多数患者(尤其是女性)从通过手术或多巴胺激动剂治疗治愈的小的良性肿瘤,到生长迅速、复发且对多巴胺激动剂治疗耐药的进袭性肿瘤(多见于男性)。识别进袭性泌乳素细胞瘤具有重要的临床意义。事实上,尽管没有转移,它们是“疑似恶性的(suspected of malignancy)”或有“恶性潜能的(a malignant potential)”,并与高致死致残率相关。临床症状,预后病理分类,分子和遗传标志物可以帮助临床医生在早期识别这些进袭性泌乳素细胞瘤,并分层对其治疗管理。特别是对于这种类型的垂体瘤,多学科方法在临床实践和研究中均是关键的。





