《Endocrinology and Metabolism Clinics North America》杂志2020 年9月[Sep;49(3):401-412. ]刊载美国Harvard Medical School麻省总医院的Nicholas A Tritos,和Beverly M K Biller撰写的综述《库欣病药物治疗进展。Advances in the Medical Treatment of Cushing Disease》(doi: 10.1016/j.ecl.2020.05.003. )。

药物治疗在库欣病的治疗中起辅助作用。对于接受垂体放射治疗的患者,建议进行药物治疗并等待放射治疗的有益效果。术前使用药物来稳定重病患者手术前的病情。对于肿瘤位置不确定的患者,采用药物治疗来控制皮质醇增多症。库欣病患者可用的药物治疗包括类固醇生成抑制剂、中枢性作用制剂(centrally acting agents)和糖皮质激素受体拮抗剂。所有药物都需要仔细监测,以优化临床疗效和管理不良反应。正在开发的新药剂可以扩大治疗这一疾病的医疗手段。
![]()
引言
库欣病(CD)是由分泌促肾上腺皮质激素(ACTH)的垂体腺瘤(或罕见的垂体癌)引起的,需要细致的治疗以将皮质醇增多症的并发症发生率和死亡率降到最低。由经验丰富的垂体神经外科医生进行的经蝶窦垂体手术是大多数库欣病患者治疗的基础。然而,约15%的库欣病患者经蝶窦垂体手术后没有达到缓解。此外,每年大约2%的患者在手术缓解后复发,长期随访的累计复发率接近35%。
药物治疗在库欣病患者中是典型的辅助治疗,药物治疗通常用于那些术后复发或术后未达到缓解的,但被认为不适合再次手术的患者。在这组患者中,通常建议垂体放射治疗作为最终治疗,而药物治疗用于控制皮质醇增多症,直到放射治疗(在几个月到几年之后)生效。较少有的是(less often),建议使用药物治疗优化术前病人的状态,或对虽经广泛检查但肿瘤位置仍不确定的患者用药。
有几种治疗库欣病的药物可供选择,还有一些正在临床开发中。目前可用的药物根据其作用部位进行了分类(图1),包括类固醇生成抑制剂、中枢性作用药物和糖皮质激素受体(GR)拮抗剂(表1)。这篇文章的目的是综述用于治疗库欣病患者的药物,并强调该领域的新发展。为了编纂参考文献,使用下列关键词进行电子检索:库欣病(Cushing’s disease)、皮质醇增多症(hypercortisolism)、药物治疗(medical therapy)、酮康唑(ketoconazole)、甲吡酮(metyrapone)、米托坦(mitotane)、依托咪酯(etomidate)、卡麦角林(cabergoline)、帕瑞肽(pasireotide)、米非司酮(mifepristone)。文章的收录是由作者自行决定。

图1所示:目前用于库欣病患者的药物作用部位。在美国的这类患者人群中,卡麦角林、酮康唑、甲吡酮、米托坦和依托咪酯都是适应证以外用药。
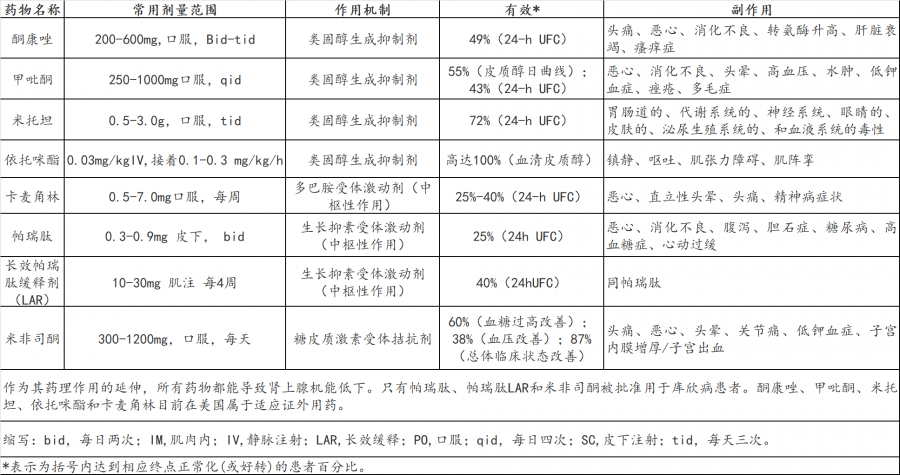
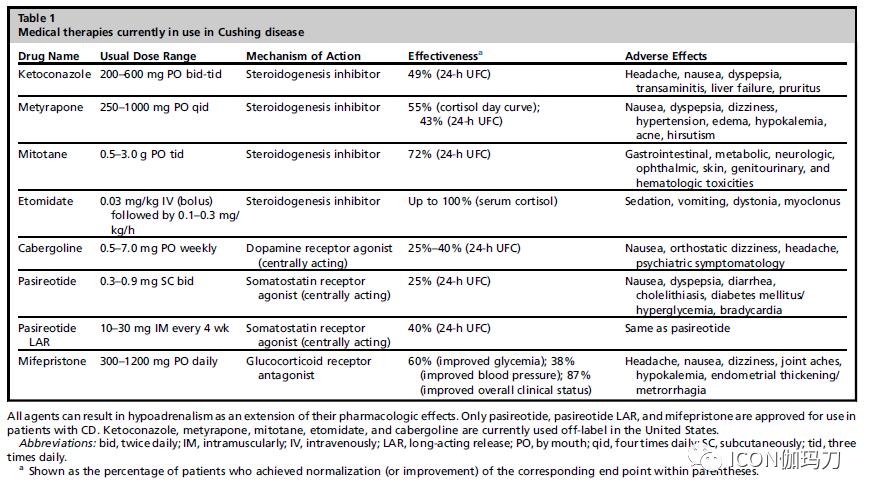
表1.目前在库欣病中应用的药物治疗。
类固醇生成抑制剂
类固醇生成抑制剂的作用是通过抑制一种或几种酶参与肾上腺甾体的生成,导致皮质醇生物合成的减少。它们在控制皮质醇增多症方面是有效的,但是作为其药理作用的延伸,它们都有可能引起肾上腺功能不全。需要定期和细致的随访和监测,以优化临床效果,同时检测和管理与使用相关的任何毒性。类固醇生成抑制剂滴定达到正常皮质醇水平,一般是指24小时尿游离皮质醇(UFC)或深夜唾液皮质醇。另外,它们也被用作“阻断和替代(block and replace)”治疗,旨在抑制内源性皮质醇的分泌,提供糖皮质激素的替代。“阻断和替代”方案的选择对循环库欣病患者是特别有用的,但是需要注意的是,不要过度替换,导致医源性(外源性)皮质醇增多症。目前可用的类固醇生成抑制剂包括酮康唑、甲吡酮、米托坦和依托咪酯。他们都没有通过美国食品和药物管理局(FDA)批准用于库欣病。值得注意的是,欧洲药品局(EMA)许可酮康唑和甲吡酮用于库欣病患者。
酮康唑是一种具有抗真菌活性的咪唑衍生物,其还能抑制参与肾上腺类固醇生成的几个酶。酮康唑的疗效最近在一项回顾性多中心研究中被报道,该研究对200例库欣病患者进行酮康唑治疗,平均每日剂量为600 mg。在该项研究中,报告有49%的患者24小时UFC恢复正常,有26%的研究对象UFC改善大于或等于50%。此外,40% - 50%的患者在治疗期间血压、血糖和血清钾水平有所改善。
在同一项研究中,20%的患者因为副作用事件而停用酮康唑。除肾上腺机能低下外,酮康唑治疗的副作用还包括消化不良(dyspepsia)、瘙痒(pruritus)、性腺机能减退(男性)和肝脏炎症。13%的患者出现轻度的转氨酶升高(transaminitis),停用酮康唑后可逆转。此外,有报道称,大约1 / 15000的患者在服用酮康唑后出现危及生命的肝炎和肝衰竭。FDA已经授权在酮康唑标签中加入黑框警告,以告知患者和医生与药物使用相关的严重肝毒性的风险,并建议定期监测肝脏化学反应。酮康唑需要胃酸才能吸收;因此,患有胃酸过少(hypochlorhydria)的患者(由于身体状况或与减少胃酸分泌的药物有关)可能不能很好地吸收药物。此外,酮康唑具有多种药物-药物相互作用的潜力,包括那些通过CYP3A途径代谢的药物。
甲吡酮抑制11β羟化酶活性,导致皮质醇合成下降。在对195例库欣综合征患者的回顾性多中心研究中,其中包括115例库欣病患者,甲吡酮治疗导致分别有55%的血清皮质醇水平(根据皮质醇日曲线)正常化,和43%的24小时UFC正常化。甲吡酮已被用于控制妊娠期皮质醇增多症;然而,它并没有明确标明可在妊娠期使用。除了肾上腺机能减退症之外,与甲吡酮治疗相关的不良反应包括恶心、消化不良、雄激素过多症(hyperandrogenic)效应(痤疮和多毛症hirsutism),在女性由于积累盐皮质激素活性的前体导致产生积累的雄激素前体,和盐皮质激素效应(高血压、水肿和低血钾)的结果。
米托坦在结构上与一种较老的杀虫剂(DDT)相似,并具有作为类固醇生成抑制剂和(特别在长期高剂量使用下)抗肾上腺素作用的有用活性。它被FDA批准用于促肾上腺皮质癌(adrenocortical carcinoma)的治疗。在美国,它在库欣病中的应用仅限于少数患者。在对76例库欣病患者的回顾性研究中,接受米托坦治疗(平均剂量,2.4 g/日)的患者中,72%的患者报告24小时UFC恢复正常。此外,血压和血糖也有改善。在该项研究中,米托坦的有益作用在停药时一般是可逆的。
米托坦治疗与几种不良反应有关,尤其包括胃肠道毒性、转氨酶升高、血脂异常、中性粒细胞减少、神经系统作用(头晕、不稳、构音障碍、刺痛)、皮疹、膀胱和眼科毒性反应等。在同一项研究中,29%的接受米托坦治疗的患者由于不良事件而停止治疗。此外,米托烷是致畸性的,并在脂肪组织中积累,停药后慢慢从脂肪组织中清除。因此,建议停药后推迟5年怀孕,这限制了其在绝经前妇女中的使用。
依托咪酯通常用于住院病人的麻醉和/或镇静。它主要抑制11β羟化酶,导致血清皮质醇水平快速下降。依托咪酯已被用于威胁生命的皮质醇增多症患者,这有助于作为另一干预(通常是手术)的过渡。在一项对7例接受依托咪酯治疗的严重库欣病患者(其中2例患有库欣病)的回顾性研究中,报告几乎所有患者的血清皮质醇水平在平均间隔38小时内迅速下降到目标区(除了一位进入临终关怀的患者)。依托咪酯治疗需要在重症监护病房进行密切监测,以发现和管理剂量依赖性的过度镇静。其他可能的副作用包括恶心、呕吐、血压下降、血栓性静脉炎、肾功能障碍和肌阵挛。
一些正在研究的类固醇生成抑制剂目前正在研发中,包括左旋酮康唑(levoketoconazole),osilodrostat,ATR101,醋酸阿比特龙(abiraterone acetate),ALD1613,和黑素皮质素2受体的肽拮抗剂(peptide antagonists of the melanocortin 2 receptor)。
左旋酮康唑(2S,4R酮康唑)是酮康唑对映体(enantiomer),在体外具有比2R,4S对映体更高的类固醇生成抑制剂作用。最近发表了一项关于左旋酮康唑治疗94例库欣综合征(包括80例库欣病患者)的3期研究。在该项研究中,经过6个月的治疗,38%的患者达到正常的24小时UFC,其中30%在没有增加剂量的情况下恢复24小时UFC。对体重、库欣病症状和体征、抑郁、生存质量、血糖和血脂都有有益影响。在31%的患者中报告有28例轻度转氨酶升高(比正常上限高1-3倍);10%的患者发生较严重的转氨酶升高。无肝脏衰竭的病例。所有患者经停药后痊愈,无任何后遗症。
Osilodrostat是一种有效的11β羟化酶和醛固酮合成酶抑制剂,在一项对库欣病患者的2期研究中显示了作为类固醇生成抑制剂的前景。最近报道了Osilodrostat在137例库欣病患者中的3期研究结果。该临床试验包括一个8周的随机停药期,在此期间,86%的osilodrostat组患者保持24小时UFC正常,而29%安慰剂组的患者保持正常UFC,随后进行开放标签的osilodrostat治疗,直到研究结束。研究结束时(48周)还报告了对体重、血压、生存质量和血糖的有益影响。Osilodrostat的耐受性一般良好。除了可能作为其药理作用的延伸而发生的肾上腺机能低下外,副作用包括疲劳、头痛、恶心和关节痛。低钾血症、雄激素过多症和对QT延长的小影响已被报道,但未见严重心律失常。
一种酰基辅酶A的抑制剂:胆固醇酰基转移酶1 (ACAT1),被称为ATR101,已经在狗身上进行研究,目前正在库欣病患者的研究中研究。醋酸阿比特龙是另一种类固醇生成抑制剂,阻断17α羟化酶和17,20裂解酶。它是一种被批准用于转移性前列腺癌的治疗方法。有一位肾上腺皮质癌患者对这种疗法有生化反应。醋酸阿比特龙在肾上腺皮质癌中的研究正在进行中。然而,醋酸阿比特龙对库欣病是否有效仍不清楚。中和ACTH和介导ACTH作用的黑素皮质素2受体的肽拮抗剂的单克隆抗体(ALD1613)已经合成并处于早期临床开发中。
中枢作用制剂(CENTRALLY ACTING AGENTS)
中枢作用制剂作用于肿瘤性促肾上腺皮质激素细胞以减少ACTH的分泌。当前使用的制剂包括卡麦角林(对库欣病的治疗时处方适应证以外的)、帕瑞肽(pasireotide),和帕瑞肽长效缓释剂(pasireotid elong-acting release,LAR),后两个被FDA和EMA批准用于库欣病患者的亚群。这些制剂的有效性是建立在大多数肿瘤性促肾上腺皮质激素细胞存在多巴胺2型(D2)受体和生长激素抑制素受体(包括SSTR2和SSTR5)。
卡麦角林是一种选择性多巴胺2型(D2)受体激动剂,获准用于高泌乳素血症患者。一些回顾性或前瞻性的小型(各10-30例)研究报道了卡麦角林对库欣病的疗效。在这些研究中,卡麦角林治疗导致25%到40%的患者24小时尿游离皮质醇(UFC)正常化。然而,对药物的有益作用的逃逸并不罕见。在另一项关于卡麦角林治疗库欣病的研究中,没有患者达到正常的24小时尿游离皮质醇(UFC)。值得注意的是,这些研究中使用的卡麦角林剂量(1-7 mg/wk)通常高于高泌乳素血症患者的典型剂量(0.5-2.0 mg/wk)。
卡麦角林治疗通常耐受性良好。然而,可能会发生不良事件,包括恶心、呕吐和直立性头晕。较少见的有头痛、鼻塞、便秘、手指的血管痉挛(digital vasospasm)、清晰梦境的梦(vivid dreams)或噩梦、焦虑和抑郁等。卡麦角林治疗可加重精神病,精神病患者应避免使用。冲动障碍已在一些使用卡麦角林治疗高泌乳素血症患者的研究中得到确认。此外,(高剂量)卡麦角林治疗已被证实与帕金森病患者的心脏瓣膜病变有关。对高泌乳素血症患者使用卡麦角林治疗的大多数研究都证实有瓣膜病变的发生。然而,在使用卡麦角林治疗的库欣病患者中却没有这样的安全性数据。谨慎地使用尽可能低的有效剂量的卡麦角林,并在数年内通过超声心动图对接受高于正常剂量的卡麦角林的患者进行定期评估。
帕瑞肽(Pasireotide)和帕瑞肽长效缓释剂(Pasireotide LAR)是生长抑素受体激动剂,可激活多种受体亚型(SSTR1, SSTR2, SSTR3, SSTR5)。上述两种药物都被证明能有效地控制库欣病的皮质醇增多症。在一个关键的3期研究(162例)中比较两者的不同,每天两次,药物的皮下剂量,帕瑞肽治疗导致在25%被随机分配接受高剂量(900μg,每日两次)的患者中24小时尿游离皮质醇正常化。研究对象的血压、血脂、体重和生存质量都有改善。此外,在该研究中,一些放射影像上可见垂体腺瘤的患者的肿瘤体积也有所缩小。
帕瑞肽与老年生长抑素受体激动剂有许多共同的副作用,包括腹部不适、腹胀、腹泻、胆石症和心动过缓。此外,肾上腺机能减退可能发生作为其药理作用的延伸。然而,高血糖症和糖尿病在帕瑞肽患者中较为常见,分别发生在73%和34%的研究对象中。帕瑞肽治疗下的葡萄糖稳态恶化(Deterioration of glucose homeostasis)是胰岛素血症降低的结果,反映了直接抑制胰岛素分泌和抑制肠促胰岛素释放。仔细监测血糖过多是可取的。服用帕瑞肽治疗的高血糖症或糖尿病患者最好使用二甲双胍、基于肠胰岛素治疗或胰岛素治疗。
长效缓释帕瑞肽(LAR),是帕瑞肽的长效制剂,在有150例患者的关键的3期研究中也被证明是有效的,患者被随机分配接受两种剂量之一的肌肉给药。在这项研究中,这种治疗导致40%的患者24小时UFC恢复正常。帕瑞肽LAR的安全性与帕瑞肽基本相同。这两种药物都被FDA和EMA批准用于手术失败或非手术适应证的库欣病患者。
几种中枢作用的药物正在研发中,包括吉非替尼(gefitinib)、r-Roscovitine 、异维甲酸(isotetinoin)和水飞蓟宾(silibinin)。最近的研究发现,泛素特异性蛋白酶8 (USP8)基因存在激活突变,导致通常用于蛋白酶体降解的靶向蛋白过度去泛素化。这导致更多的蛋白质循环,如表皮生长因子受体,到质膜,从而增加ACTH的分泌。表皮生长因子受体酪氨酸激酶抑制剂吉非替尼(gefitinib)正用于库欣病患者的研究。R-roscovitine是一种细胞周期蛋白依赖性激酶2和细胞周期蛋白E的抑制剂,在实验研究中可导致ACTH分泌减少和抑制肿瘤生长。R-roscovitine也在库欣病患者中进行了研究。异维甲酸,13顺式维甲酸的异构体,据报道其在小型研究中控制约25%的库欣病患者的皮质醇增多症。水飞蓟宾通过与热休克蛋白90 (HSP90)结合,导致其与糖皮质激素受体分离。体外和动物数据表明,水飞蓟宾治疗恢复了皮质醇对ACTH分泌的负反馈,因此似乎有望成为库欣病患者的一种潜在治疗方法。
糖皮质激素受体剂拮抗
糖皮质激素受体(GR)拮抗剂通过与其同源受体结合抑制皮质醇的作用。目前,米非司酮(mifepristone)是这类药物中唯一可用的药物;另一种药物(relacorilant)正在临床研发中。
在一项关键的(pivotal)的3期研究中,50例库欣综合征患者接受了米非司酮的研究,其中43例患有库欣病。血糖过高(glycemia)和血压的改善分别出现在29例患者中的60%和21例患者中的38%患者中,这些患者在基线时有高血糖症或高血压。一些接受米非司酮的患者降糖药物的剂量降低了。此外,87%的研究对象有整体临床状况的改善。值得注意的是,在接受米非司酮治疗的库欣病患者中,ACTH和皮质醇水平明显高于基线水平,可能不能用于评估其临床疗效。因此,必须单独根据临床标准滴定药物。米非司酮被FDA批准用于手术失败或不适合手术的伴有高血糖症的库欣综合征患者(包括伴有高血糖症的库欣病患者)。
作为药物作用的一种延伸,服用米非司酮治疗的患者可能出现肾上腺机能减退(Hypoadrenalism),必须根据临床背景加以诊断,因为这些患者的皮质醇水平并不低。如果怀疑有肾上腺机能减退,应暂时停用米非司酮,直到症状消失。有严重症状的病人可以通过给予高于替代剂量的地塞米松数天来挽救。
与米非司酮治疗相关的其他副作用包括盐皮质激素效应,如低钾血症、水肿和血压升高,这是由于高浓度的皮质醇与盐皮质激素受体不受反对的相互作用(unopposed interaction)造成的。定期监测血清钾和给予适当的替代治疗对这些患者显然很重要,他们也可能受益于螺内酯治疗(spironolactone therapy)。子宫内膜增厚和子宫出血(Endometrial thickening and metrorrhagia)可能是孕酮受体阻滞的结果,但未见癌前期的子宫内膜增生(spironolactone therapy hyperplasia)。米非司酮可以终止妊娠,妊娠期间禁忌应用。也有报道血脂异常和促甲状腺激素水平升高。通过周期性影像检查定期监测垂体腺瘤是谨慎的。然而,到目前为止,尚无相关报道表明接受米非司酮治疗的患者垂体肿瘤大小增加。该药物有可能与其他通过包括CYP3A4等几种P-450同工酶代谢的药物相互作用,因此在开始治疗前必须对患者使用的所有同步药物进行审查。
Relacorilant (CORT125134)是一种正在研究的糖皮质激素受体(GR)拮抗剂,它不抑制孕激素受体,因此不太可能对子宫内膜产生不良影响。目前正在对库欣综合征患者进行研究。一项针对32例库欣综合征患者(包括库欣病患者)的二期研究报告了相关治疗对血糖和血压的改善。正在对有关因素进行进一步调查。
总结:
库欣病(CD)的药物治疗选择包括类固醇生成抑制剂、中枢作用制剂和糖皮质激素受体(GR)拮抗剂。它们有助于控制皮质醇增多症,尤其适用于手术失败或不适合手术的患者。所有药剂都需要仔细监测,以确保达到治疗目标,并评估过度毒性。一些报道研究了联合疗法,包括几种类固醇生成抑制剂单独使用或与中枢作用制剂联合使用,但这种方法的确切作用仍不确定。近年来,人们对发现和研发治疗库欣病的新药产生了浓厚的兴趣,这可能最终导致进一步扩大这种严重疾病的可用治疗的选择。
![]()



