原文:
The Application of the Novel Grading Scale (Lawton-Young Grading System) to Predict the Outcome of Brain Arteriovenous Malformation
原文作者:
Ahmad Hafez, MD∗ Päivi Koroknay-Pál, MD, PhD∗ Elias Oulasvirta, BM∗ Ahmed Abou Elseoud, MD, PhD‡ Michael T. Lawton, MD§ Mika Niemelä, MD, PhD∗ Aki Laakso, MD, PhD∗
作者单位:
∗ Department of Neurosurgery, Helsinki University Hospital, Helsinki, Finland;
‡ Department of Diagnostic Radiology, Helsinki University Hospital, Helsinki, Finland;
§ Department of Neurosurgery, Barrow Neurological Institute, Phoenix, Arizona
编译:
彭雍
审校:
蒋宇钢
1
背景:
作为 SM(Spetzler-Martin,SM)系统的改进版,2010 年提出了补充分级量表[Spetzler-Martin 补充分级(Supplemented Spetzler-Martin grade,Supp-SM)],致力于提高脑动静脉畸形(arteriovenous malformations,AVMs)的术前风险预测能力。
目的:
确定 Supp-SM 分级量表预测手术结局的能力。
方法:
回顾性研究在 2000 年至 2014 年间于赫尔辛基大学医院就诊的 200 例患者。采用受试者工作特征曲线下面积(area under the receiver operating characteristic,AUROC),对术前、术后早期(3~4 个月)以及术后研究终点的改良Rankin 量表(Modified Rankin Scale, mRS)的评分进行分析,比较 Supp-SM 与 SM 评级系统的有效性。
结果:
结论:
Supp-SM 分级系统可提高治疗结局的预测准确性并可成为 SMS 的替代系统,还可应用于高级别AVMs 占比较高的病例组中。然而,穿支动脉对治疗结局有重要影响。
方 法
研究对象
研究变量
统计学分析
结 果
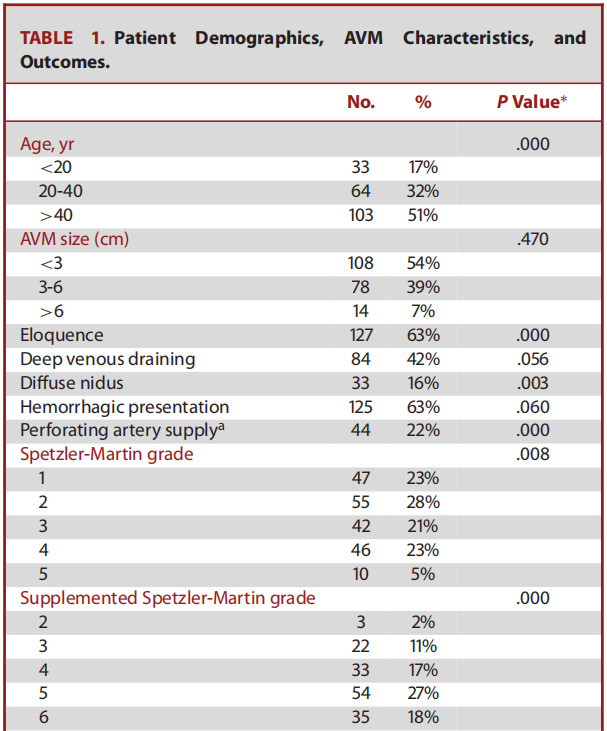
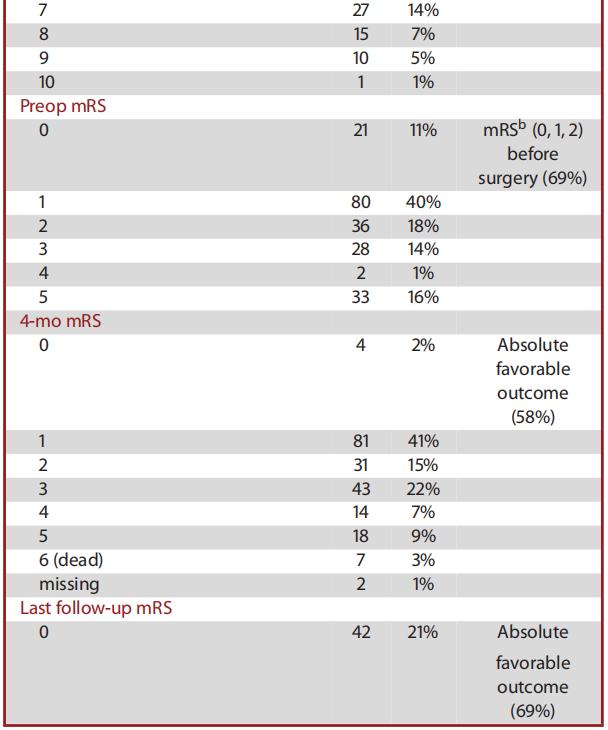
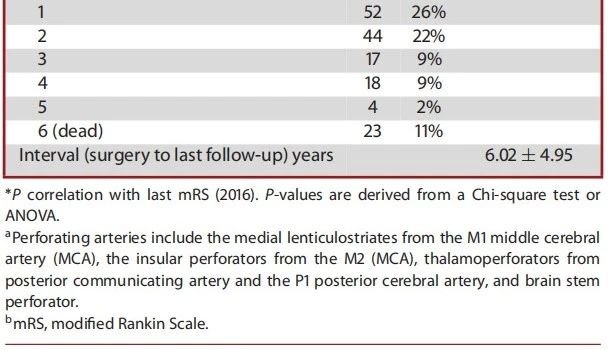
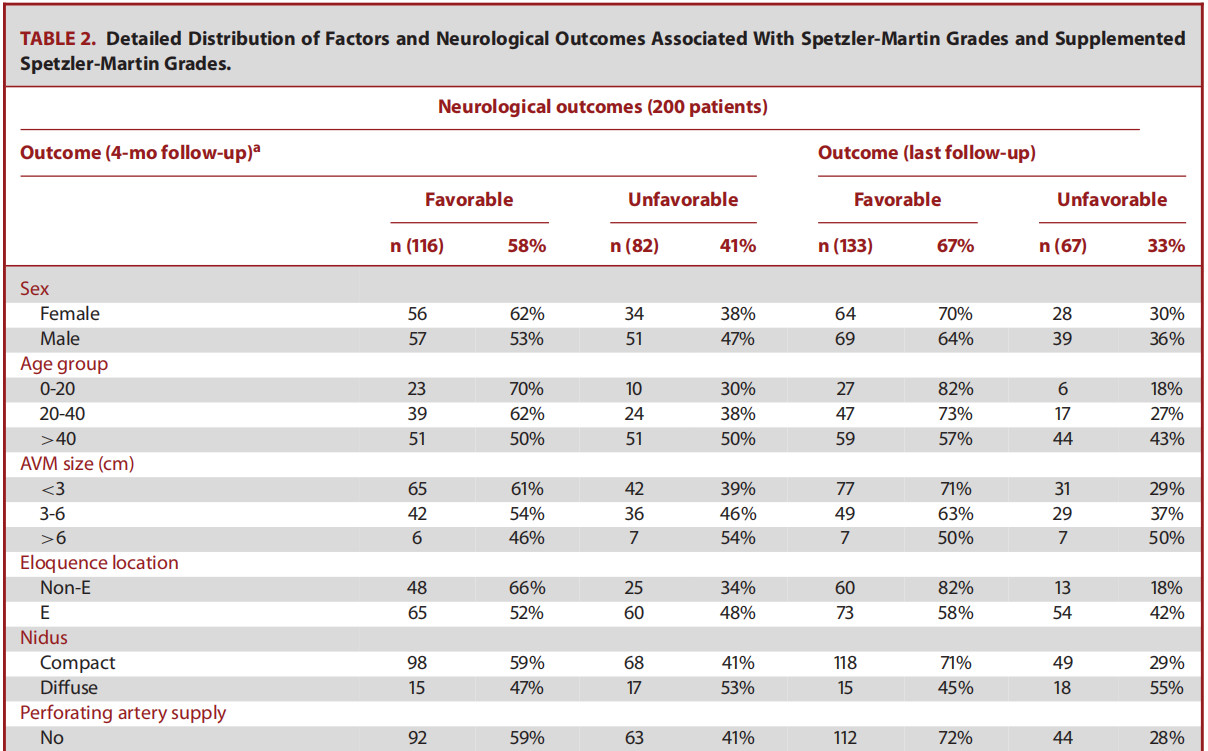
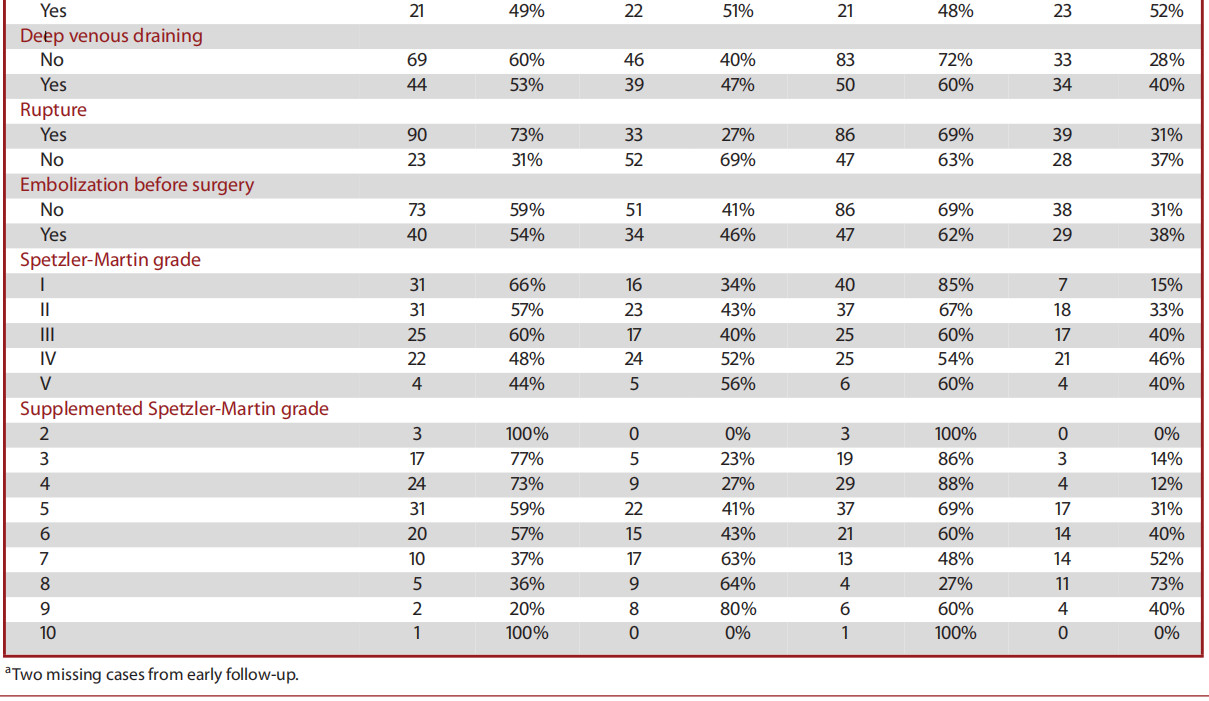
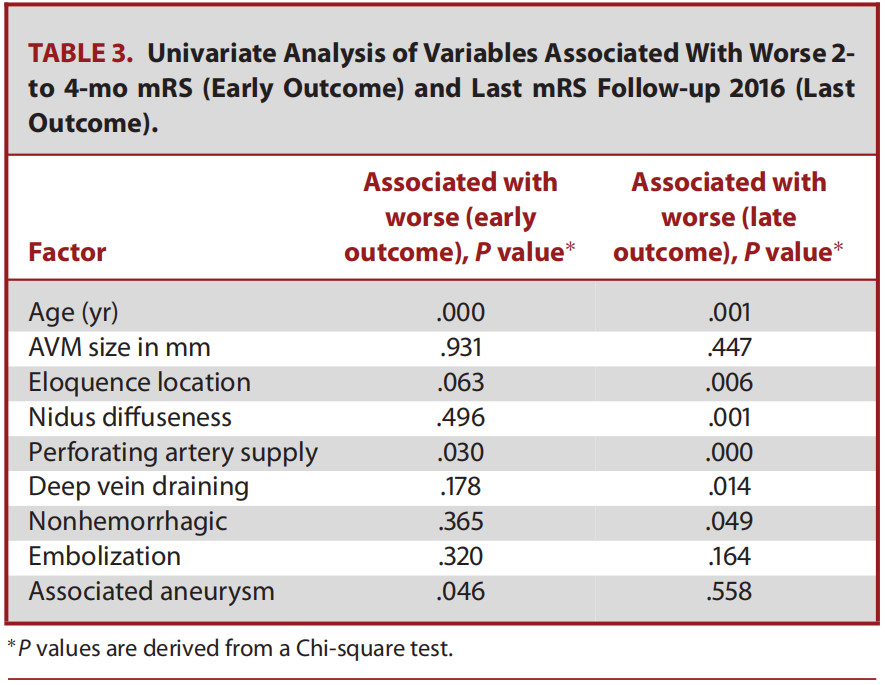
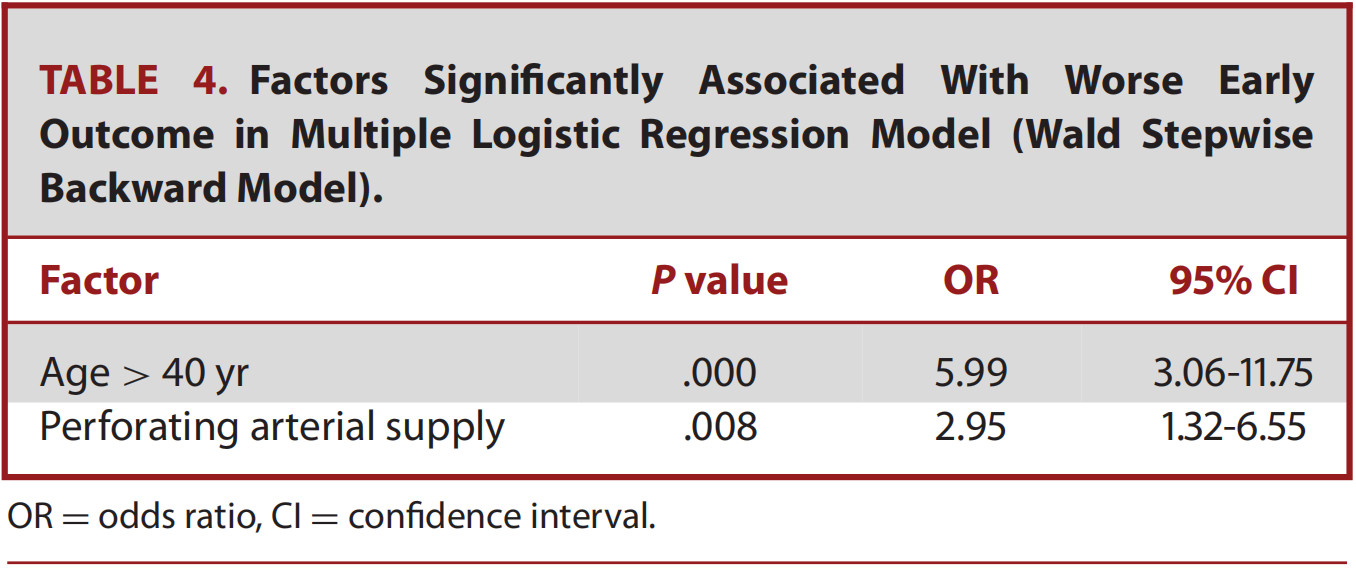
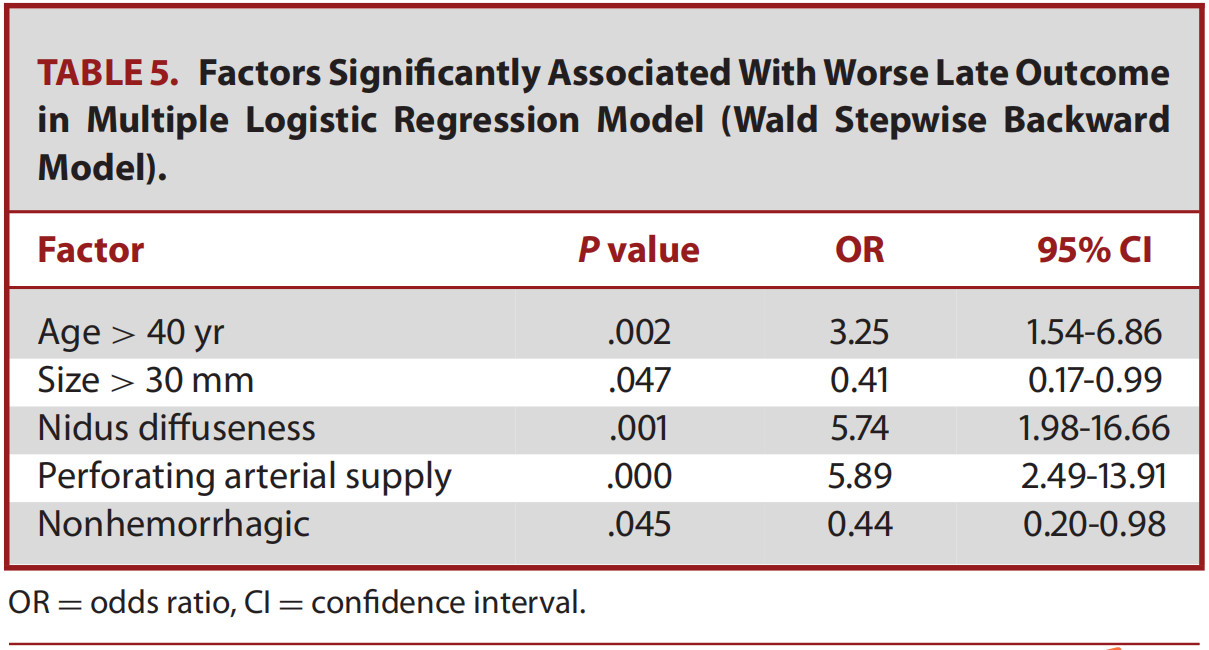
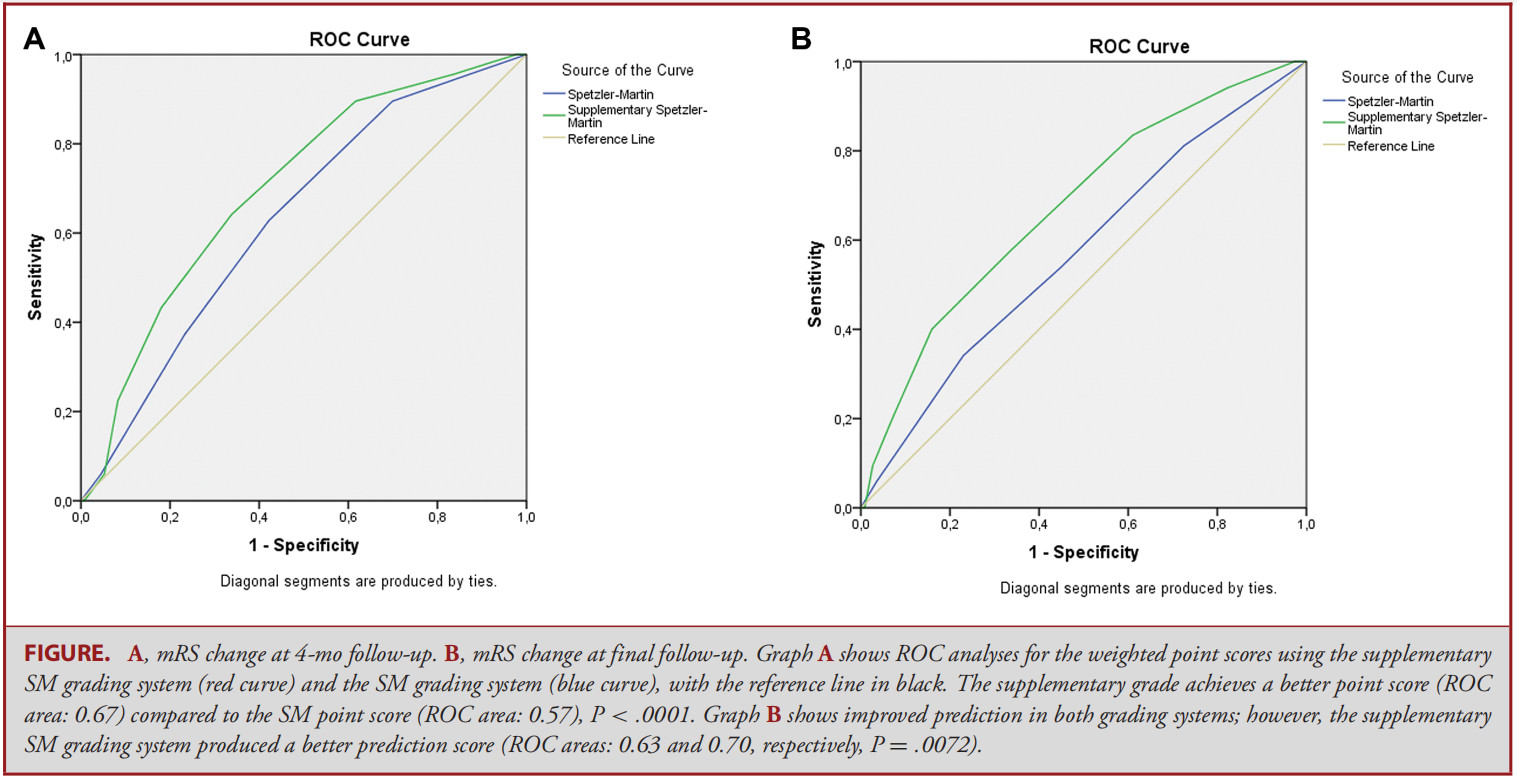
讨 论
研究的局限性
结 论
声 明

参考文献







评 论