有研究发现选择性动脉内注射贝伐单抗在胶质瘤和放射性坏死的治疗中具有良好疗效,尤其是减少了剂量相关的毒副作用。该研究旨在通过形态学和病理学研究评估动脉内注射贝伐单抗对血管生成的影响。
——摘自文章章节
【REF: Papagiannaki C, et al. J Neuroradiol. 2020 Mar 14. pii: S0150-9861(20)30130-9. doi: 10.1016/j.neurad.2020.03.003. 】
研究背景
![]()
脑动静脉畸形(bAVMs)是一种少见的脑血管病。青年出血性脑卒中的病因里AVM占2%。AVM年出血率约为3%,AVM出血幸存者中有45%出现严重的神经功能障碍。近年来针对AVM分子病理机制的研究较为广泛,包括AVM的形成、重塑、消退和再生的遗传学、血流动力学,表观遗传学和免疫学等方面,有报道称散发性AVM可见异常血管生成,抗VEGF治疗可有效减少血管生成,抑制AVM的发生发展。
贝伐单抗是一种重组人源化抗VEGF单克隆抗体,可抑制血管生成。目前贝伐单抗已用于高级别胶质瘤、糖尿病性黄斑水肿、遗传性出血性毛细血管扩张症、结直肠癌、乳腺癌、肾癌,卵巢癌和非小细胞肺癌的治疗。贝伐单抗主要通过抑制内皮细胞增殖、抑制血管生成、减少毛细血管形成,以及阻断VEGF抑制树突状细胞成熟,从而增强机体免疫功能等而起作用;有研究发现选择性动脉内注射贝伐单抗在胶质瘤和放射性坏死的治疗中具有良好疗效,尤其是减少了剂量相关的毒副作用。该研究旨在通过形态学和病理学研究评估动脉内注射贝伐单抗对血管生成的影响,报道如下。
研究方法
![]()
将15只动物分为3组:5只动物作为对照组;5只动物行血管内左颈外动脉与颈总动脉闭塞术(图1);5只动物行闭塞术后2个月给予动脉内注射贝伐单抗。所有动物均在术后当日(D0)和3个月(3M)时行3D-DSA检查测量颅底血管网体积。另外,在3月时处死动物,取猪的颅底血管网行病理学和免疫组化染色。
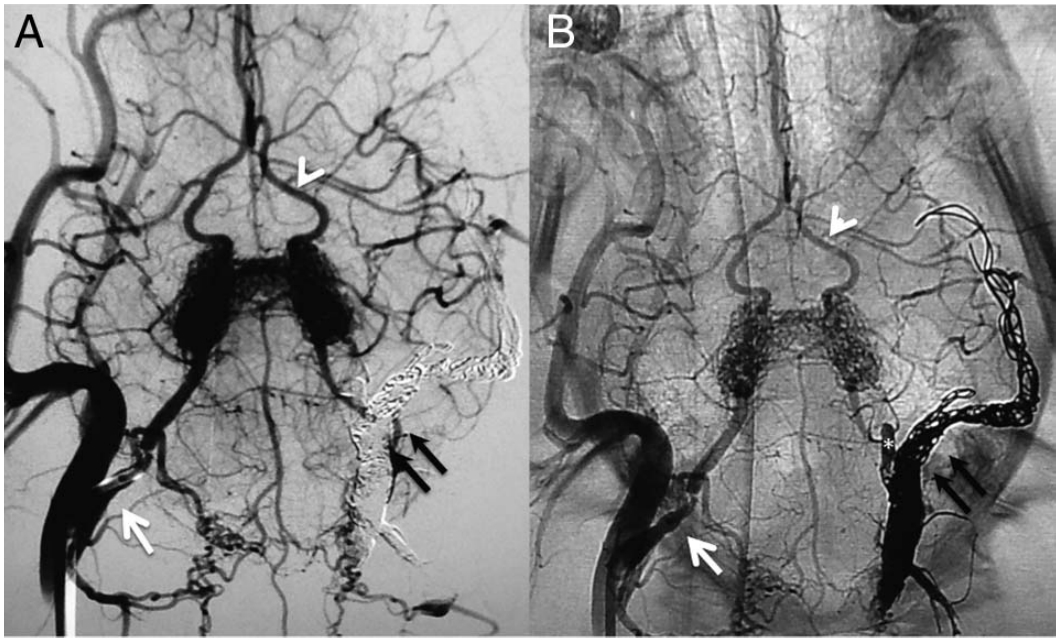
图1. 闭塞组颅底血管网血管造影检查。(A)减影,(B)未减影。血管内行颈总动脉和颈外动脉闭塞术(A和B:双黑色箭头),包括左咽升动脉(B,星号)。用5F导管经右咽升动脉行血管造影检查(A和B:白箭)。颅底血管网和颈内动脉显影(A和B:白箭头)。
研究结果
![]()
3组动物在D0和3M时体重无明显差异。
D0时各组动物颅底血管网体积无明显差异。从D0至3M,对照组动物颅底血管网体积无明显变化。与对照组相比,3M时闭塞组动物颅底血管网体积明显增大(p=0.01),提示闭塞组血管生成更加活跃。D0时闭塞组动物颅底血管网体积为2±0.56 ml(范围:1.28-2.78),3M时为2.92±0.33 ml(范围:2.4-3.4)(P=0.01);然而,贝伐单抗组D0时颅底血管网体积为1.33±0.38 ml(范围:0.8-1.9),3M时为2.7±0.7 mL(范围:1.8-3.4)(P=0.009)。
闭塞组动脉总管径为223.9±48.7 μm,贝伐单抗组为208.33±9.1 μm,两组之间无明显差异。闭塞组血管内-中膜厚度为109.22±17.3 μm,贝伐单抗组为299.92±61.08 μm,两组之间无明显差异。贝伐单抗组动脉壁厚度/管径为0.64±0.006较闭塞组0.52±0.01略有增加,组间差异无统计学意义。与对照组相比,闭塞组管壁更薄(p=0.004)。这些结果表明,闭塞组管壁变薄,反映了ECA-CCA闭塞导致血管生成。贝伐单抗组总的管壁厚度没有明显增加,表明贝伐单抗可以稳定血管内-中膜厚度。
研究发现与贝伐单抗注射对侧(B0)或闭塞组相比,贝伐单抗注射侧(BAV)颅底血管网血管壁不表达VEGF-R1。VEGF受体在BAV与对照组中低表达。IL-6在闭塞组中着色较深,在贝伐单抗组中着色较浅,在对照组中未见明显着色。Ki-67在BAV中着色较深,在B0和对照组中着色较浅。TUNEL在闭塞组和B0中未见明显着色,而在BAV中着色较深,提示贝伐单抗可诱导细胞凋亡。以上结果说明,贝伐单抗注射1个月后,VEGF-R1仍可被完全阻断;贝伐单抗增加了内皮细胞增殖(Ki-67)与凋亡(TUNEL)数量,但对炎症反应的影响不大。
研究结论
![]()
该研究发现单次大剂量动脉内注射贝伐单抗到具有AVM组织学特征的猪血管生成模型中,可有效阻断VEGF-R1长达1个月以上。血管内皮细胞增殖与凋亡均明显增加,表明贝伐单抗可调控分裂活跃的血管内皮细胞;贝伐单抗不影响血管壁厚度,这说明贝伐单抗不影响血管壁的完整性;此外,贝伐单抗对炎症反应的影响甚微。这个初步研究揭示贝伐单抗的抗血管生成作用在血管畸形中具有潜在作用,贝伐单抗在bAVM治疗中的潜在疗效尚需进一步研究。
即日起“神经介入资讯”更名为“神介资讯”