美国康涅狄格州纽黑文市耶鲁医学院病理科的Kurt A. Schalper等进行一项单臂Ⅱ期临床试验(NCT02550249),评估纳武单抗(nivolumab)作为胶质母细胞瘤新的辅助治疗的价值。研究结果发表在2019年3月《Nature Medicine》杂志上。
——摘自文章章节
【Ref: Schalper KA,et al. Nat Med. 2019 Mar;25(3):470-476. doi: 10.1038/s41591-018-0339-5. Epub 2019 Feb 11.】
研究背景
胶质母细胞瘤(GBM)是恶性程度很高的中枢神经系统肿瘤。患者在手术加放、化疗后,生存期仅稍有改善。美国康涅狄格州纽黑文市耶鲁医学院病理科的Kurt A. Schalper等进行一项单臂Ⅱ期临床试验(NCT02550249),评估纳武单抗(nivolumab)作为胶质母细胞瘤新的辅助治疗的价值。研究结果发表在2019年3月《Nature Medicine》杂志上。
研究方法
研究共纳入30例胶质母细胞瘤患者,其中3例为肿瘤原发患者,27例肿瘤复发患者。患者于术前2周使用2mg/kg的纳武单抗治疗,术后每2周给予相同剂量,直至在影像学上发现肿瘤进展或出现严重的药物副作用。原发肿瘤患者在术后66天停用纳武单抗,进行标准的放化疗;其中2例患者放化疗结束后继续使用纳武单抗,未出现毒副作用。复发肿瘤患者术后每2周接受纳武单抗治疗,根据影像学显示肿瘤进展状况、药物毒性反应和患者个人意愿决定停药时间。患者的无进展生存期(PFS)和总生存期(OS)的中位数分别为4.1个月和7.3个月。
研究结果
纳武单抗是程序性死亡分子(PD-1)阻断剂,阻断PD-1介导的免疫抑制途径,促进抗肿瘤免疫效应。研究人员对纳武单抗治疗患者手术前后的病理标本进行免疫相关分子和细胞学的对比分析,发现经过纳武单抗治疗后,患者体内介导免疫反应的活性细胞因子表达显著提高,而且增加T细胞亚群的丰度;免疫活性成分的高表达往往与患者较长的生存期相关。
同时,研究人员在细胞学层面对患者纳武单抗治疗前后的手术病理组织进行免疫荧光染色,检测肿瘤微环境中各类细胞的浸润差异(图1)。
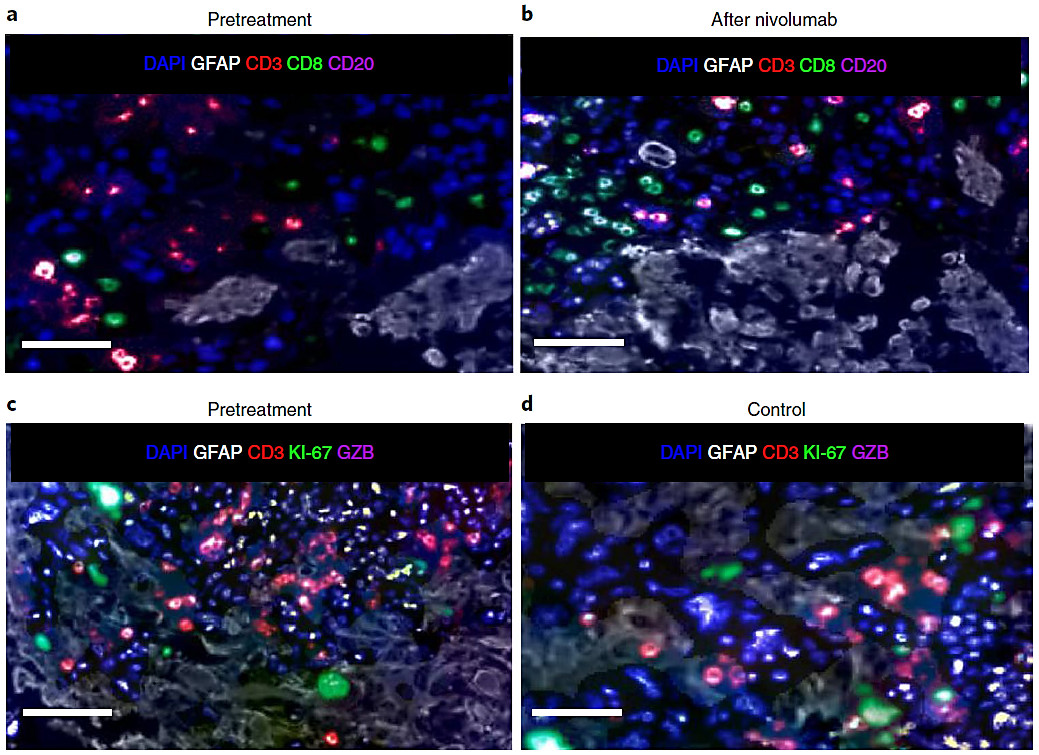
图1. 纳武单抗治疗前后免疫细胞在肿瘤微环境中的多重免疫荧光检测。
结论
最后作者指出,纳武单抗治疗GBM的辅助新疗法,可增强趋化因子转录表达,增强肿瘤内T淋巴细胞和其它免疫细胞的浸润,增加TCR克隆的多样性,支持肿瘤局部免疫调节,杀伤肿瘤细胞。该新的辅助疗法对GBM抢救性手术患者尚无明显的临床获益,但3例原发GBM患者中,2例在初次手术前后使用纳武单抗后分别存活33个月和28个月,值得深入探索。纳武单抗的治疗引发抗肿瘤免疫反应,而仅使用PD-1阻断治疗不足以延缓或阻止疾病进展,免疫和非免疫联合治疗可能提供新的治疗希望。






