摘要
颅内动脉瘤的形成机制是多因素的。尽管血管、遗传、流行病学因素起作用,但新生动脉瘤依然被认为归因于血流动力学作用。动脉瘤的形成、演变、破裂机制非常复杂,背后有复杂的生物力学机制,还有血管的生物活性机制,机械刺激转换成生物信号,触发炎症级联反应,最后导致血管壁重塑。目前脑动脉瘤血流动力学可作为了解颅内动脉瘤发病机制的工具,并已被用来评估动脉瘤破裂风险。本文我们回顾了与动脉瘤形成和破裂相关的血流动力学参数,以及促进血管重建的生物物理途径,同时回顾了预测颅内动脉瘤破裂的临床应用现状。随着影像学研究和计算模型的不断完善,对脑动脉瘤形成、生长和破裂中血流动力学作用的认识在增加。虽然WSS与动脉瘤的形成有关,但其在动脉瘤生长和破裂中的作用仍存在争议;其他血流动力学参数可能参与动脉瘤的发病过程;血流动力学应激源的累积效应触发一系列炎症和信号级联反应,最终导致血管壁变薄、扩张和破裂。目前核磁共振和CFD技术为动脉瘤破裂提供一种有前景的预测模型与临床应用程序。
【REF: Soldozy S,et al. Neurosurg Focus. 2019 Jul 1;47(1):E11. DOI: 10.3171/2019.4.FOCUS19232.】
动脉瘤的形状是破裂的一个重要因素。Ujiie等发现纵横比(aspect ratio,AR,动脉瘤高与瘤颈宽之比)大于1.6是动脉瘤破裂的预测因子。Nader- Sepahi等人也发现AR是一个破裂预测因子,破裂动脉瘤和未破裂动脉瘤的平均AR分别为2.70和1.80;Hassan等发现侧壁动脉瘤破裂与AR大于1.6有密切关系。然而也有不同的观点,Xiang等的数据提示破裂组和未破裂组之间AR的差异并不显著。动脉瘤的尺寸比(SR),为动脉瘤最大高度与载瘤动脉直径之比,研究者发现SR越大,破裂风险越大。Kleinloog等人的meta分析发现,不规则的动脉瘤形状、较大的AR和SR、更高的瘤颈比(动脉瘤宽度与瘤颈直径之比)和动脉瘤高宽比是动脉瘤破裂风险增加的形态学特征;与破裂相关的形态学特征还包括瘤顶向下和VNR(动脉瘤体积与瘤颈面积比)。因此根据现有的资料建议,不规则形状对破裂风险具有很高的预测潜力,可用于动脉瘤的危险分层。
计算机流体动力学(CFD)从患者CT血管造影(CTA)、MR血管造影(MRA)、3D-DSA中构建流体的三维模型,动脉瘤和血管的位置、大小、形态、AR和SR等特征可以用来计算壁张力、壁面切应力(WSS)和流速,从而更好地预测动脉瘤破裂风险。到目前为止多项研究结果显示CFD可成功地用于临床,预测动脉瘤破裂的风险。
利用CFD进一步研究高、低壁面切应力和动脉瘤破裂风险的关系。Castro等人通过建立26个前交通动脉瘤模型,发现动脉瘤内最大壁面切应力 (mWSS)的升高与破裂的临床特征存在显著的关联;再扩展至42个其他部位动脉瘤的研究时同样发现这种关联;再扩展至210例脑动脉瘤,应用CFD分析其血流动力学,显示破裂动脉瘤的mWSS更大。但Xiang等人基于三维血管成像分析119个动脉瘤,发现破裂动脉瘤的mWSS和WSS低于未破裂动脉瘤;Shojima等人通过血管造影研究建立20个大脑中动脉血管模型,证明动脉瘤的平均WSS值明显低于正常血管,此外破裂动脉瘤顶端的WSS明显较低;一些研究发现动脉瘤的生长和破裂更可能发生在异常低WSS区域,这表明低WSS而不是高WSS与动脉瘤的生长和破裂有关。
模型设定或算法方法的差异会导致动脉瘤破裂风险评分不同。虽然CFD模型的预测在多个不同的研究中得到验证,但结果表明随着数据集的增多,CFD模型会更加准确。同时综合多个不同参数的复杂模型也可以进一步提高CFD模型的预测能力,需要在更大的患者群体中进行研究以确定CFD优化策略,用于辅助临床决策。
WSS对动脉瘤发病机制的影响一直是人们研究的课题。壁面切应力由流动血液与静止血管壁之间的切向摩擦力组成(图1),两个平行物体速度的相对差异产生剪切力。剪切力与两物体之间的速度梯度成正比,WSS梯度(WSSG)定义为WSS沿流动方向的空间导数,是沿着血管长度的WSS变化。在生理水平的剪切力作用下,内皮细胞呈现出一种静态的动脉粥样硬化保护基因表达谱,其特征是抗炎症、凋亡和氧化应激;而低水平的剪切力通过诱导炎症而促进动脉粥样硬化。当讨论动脉粥样硬化的病理生理时,要将动脉瘤的形成和生长区分开,因为涉及不同的血流动力学和炎症机制。
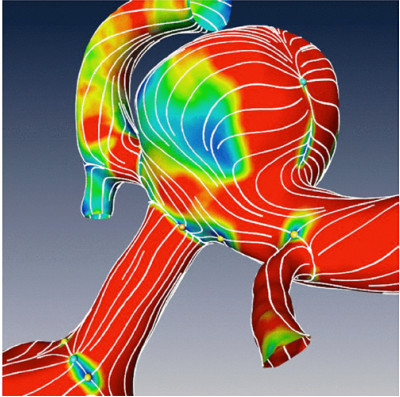
图1. 脑动脉瘤血流的CFD模型。彩色编码的WSS流线显示压力分布,描述整体流动行为和局部细节,小球表示临界点。
WSS是动脉瘤形成模型中的一个重要参数。Gao等发现高WSS是兔动脉瘤形成的一个重要因素。颈总动脉结扎后,基底动脉流量显著增加(105% - 900%),分叉处形成新生动脉瘤。组织学上新生动脉瘤的特征是外膜膨出变薄,内弹性层丧失。动脉瘤囊的形成与基底动脉流量的增加有关,高WSS和WSSG与血管重构和最终动脉瘤的形成有关。作者认为,在持续异常的血流动力学条件下,分叉处顶端的内皮细胞会发生功能障碍;其他动物模型研究有相似的发现。Can和Du进行荟萃分析发现,WSS升高与动脉瘤形成部位呈显著正相关;虽然没有发现高WSSG与动脉瘤形成有显著相关性,但发现侧壁和分叉部动脉瘤受这些血流动力学因素的影响不同。
虽然动脉瘤的形成与高WSS区域有明显的联系,但血流动力学因素对动脉瘤增大和破裂的影响尚不确定。研究发现,高WSS和低WSS都与动脉瘤的生长和最终破裂有关。
这种明显的冲突源于两种不同观点:高壁面切应力理论和低壁面切应力理论。在这两种理论中,动脉瘤内的血流动力学环境与动脉瘤壁的细胞因子相互作用,导致进一步血管壁减弱。之后围绕导致血管壁变薄的方式与风险,高应力理论认为,最大WSS的升高导致内皮损伤,并启动了壁重构和退化的过程。mWSS升高时,血管内皮暴露于一氧化氮,导致动脉张力异常低,壁内平滑肌细胞(SMCs)凋亡。相反,低应力理论认为动脉瘤内的血液淤滞会导致红细胞聚集,并引起内膜损伤和炎症细胞对血管壁的浸润,血管壁退化和抵抗血流动力学的能力下降。
Meng等人提出低WSS导致炎症前期表现,细胞浸润增加,基质金属蛋白酶(MMP)产生,SMC增殖和迁移,血栓形成。相反,高WSS结合阳性WSSG可导致内皮细胞损伤,壁细胞产生MMP,细胞外基质(ECM)降解,基质变薄,SMCs和成纤维细胞凋亡。他们将这些不同的反应分为壁细胞介导的和炎性细胞介导的破坏性重塑通路,每一种通路都可能在不同的动力学条件和不同的动脉瘤表型中导致动脉瘤破裂。与高WSS相关的壁细胞介导通路可能与小的或继发性小泡样动脉瘤的生长和破裂有关,而炎症介导通路可能与大的、动脉粥样硬化性和血栓性动脉瘤的生长和破裂有关。
与Meng等人观点不同的是,一项比较体内血流条件与动脉瘤组织的研究表明,WSS与动脉瘤壁变性、破裂之间存在完全相反的关系。Cebral等以CD45阳性细胞和CD68阳性细胞的比例分别作为白细胞和巨噬细胞表达的标志物,发现WSS越高炎症程度越高。然而低WSS显示CD45免疫染色阴性,这与壁细胞丢失有关。免疫组化显示破裂动脉瘤的炎症程度高于未破裂动脉瘤,这种炎性浸润在破裂前就存在于血管壁。目前还不清楚炎症是导致壁变性和破裂的原因,还是对最终导致壁破裂的退化性重塑原因的反应。
尽管尚不清楚其确切机制,但Cebral等人最近的一份报告支持不同血流动力学条件与动脉瘤表型相关的理论。与正常区域相比,动脉粥样硬化、增生性和破裂壁类型的平均WSS明显较低;在薄壁型中,平均WSS与正常区相比无显著差异,但高于增生性和破裂型;薄壁区域,动脉瘤的血流呈侧向排列,血流速度更快,平均WSS更高。这与厚壁型(动脉粥样硬化和增生性)形成对比,后者垂直于血流,与低WSS相关。
OSI 描述的是血流方向上的时间变化,而不是空间变化。如果在整个心脏周期中,动脉瘤内血流在某一特定点的方向保持不变,那么此时的OSI值就很低。血流的时间变化可以通过在整个心脏周期中的血流漩涡来说明(图2)。
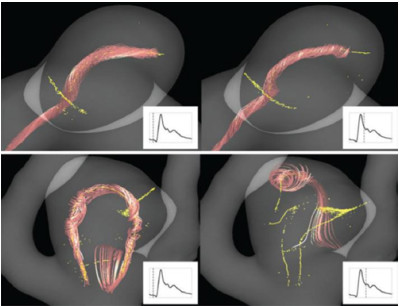
图2. 稳定(上)和不稳定(下)瘤内血流的例子。涡旋核心线(黄色)和邻近的流线轨迹(红色)描述心脏周期的两个瞬间流动的空间结构。上图动脉瘤为OSI值较低,下图动脉瘤的空间结构波动较大,OSI值较高。
考虑到动脉瘤的几何形状和载瘤血管特征对动脉瘤内血流动力学的重要性,OSI可以反映动脉瘤和载瘤血管的形态学特征。低WSS常伴有振荡血流,可促进动脉粥样硬化形成,促进炎症反应,导致内膜壁增厚。虽然许多研究已经确定了破裂动脉瘤的OSI值较高,但Can和Du在系统回顾中发现,破裂动脉瘤与未破裂动脉瘤的OSI值并无显著差异。虽然Zhou等人在破裂动脉瘤中发现了OSI值较高,但这一点没有达到统计学意义。振荡流可能是动脉瘤破裂前血管重构不良的一个因素,但它在预测动脉瘤破裂中的确切作用仍不确定。
动脉瘤瘤内血流模式影响破裂风险。Byrne等人发现破裂动脉瘤的血流模式比未破裂动脉瘤更复杂和不稳定;此外与时间稳定性相比,空间复杂性与破裂的相关性更高。Xiang等人发现破裂动脉瘤多表现出复杂的多涡流,而未破裂动脉瘤表现为简单的单涡流模式;其他报告也将破裂与复杂的血流模式联系起来。然而Kleinloog等人的综述认为,复杂的流动模式与破裂的关联证据较少。当血管壁不能再承受血流动力学应力时,最终导致动脉瘤破裂(图3)。
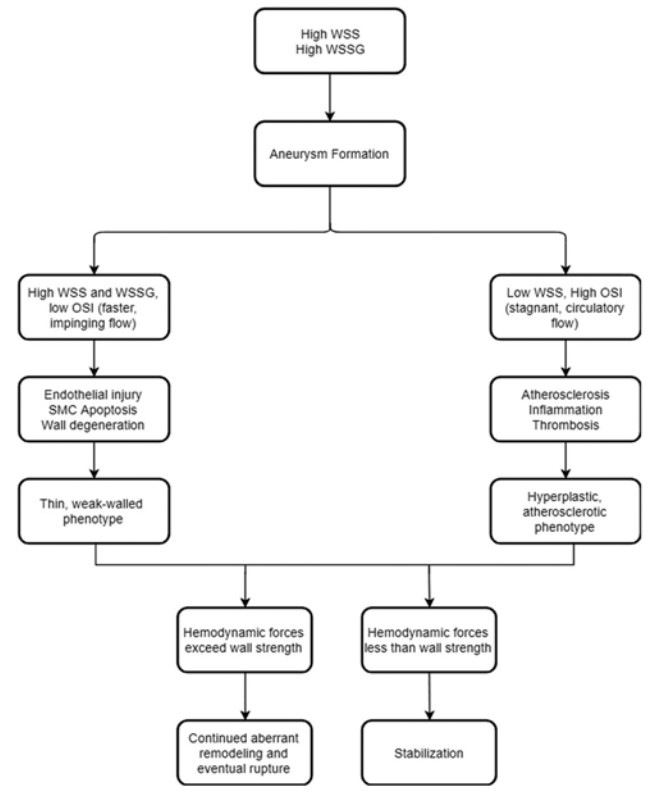
图3. 动脉瘤形成和破裂的不同血流动力学因素流程图。动脉瘤的形成方式不同于动脉瘤破裂,有两种机制可以解释血管壁重塑和最终破裂。高wss理论认为SMC凋亡和内皮细胞变性导致薄壁表型,相反低wss理论认为炎症机制包括增生和动脉粥样硬化、长期血流动力学不稳定与瘤壁强度有关,最终导致动脉瘤破裂或稳定。
异常的血流动力学是触发血管重建的应激源。动脉重建是一个适应的过程,试图返回正常的生理基线(高或低WSS);血管重建的特点是血管SMC凋亡和迁移,ECM的降解和炎症导致扩张和血管壁变薄(图4)。此外引发动脉瘤形成的血流和血管壁重塑之间的生物相互作用与已经形成的动脉瘤的生长和破裂是完全不同的过程。

图4. 动脉瘤形成和破裂过程中的炎症介质。血流动力学产生应激,血管内皮细胞在巨噬细胞、T淋巴细胞等炎症细胞的介导下,发生重构和变性。VSMCs通过表型调控进入炎症状态,内弹力层(IEL)被破坏,ECM被降解,导致动脉瘤形成及破裂。bFGF =碱性成纤维细胞生长因子;ICAM =细胞间粘附分子;M1 =促炎巨噬细胞;抗炎巨噬细胞;NK =自然杀伤细胞;前列腺素E;活性氧;TGF =转化生长因子;TLR = toll样受体;VEGF =血管内皮生长因子。
在血流动力学应激状态下,血流依赖NO抑制VSMCs的增殖,通过激活caspase 3途径激活细胞凋亡,并导致核固缩、核破裂和细胞死亡。此外,血管壁的物理拉伸可激活肿瘤抑制因子p53,诱导细胞凋亡。VSMC的迁移主要发生在血管中层,是血管损伤时的一种正常反应。血流动力学刺激可改变迁移信号,如有机胺、肽生长因子、细胞因子和ECM成分,并导致血管壁变薄。VSMCs向内膜迁移,随后通过肿瘤坏死因子 (TNF)和kruppel样转录因子-4介导表型重组。VSMCs能够表达与促炎分子上调相关的基因,包括MMPs、单核细胞趋化蛋白-1 (MCP-1)、血管细胞粘附分子-1 (VCAM-1)和白介素(IL)。在内膜层,这些细胞可以增殖并合成新的基质和纤维组织,从而导致内膜增生。在易破裂的动脉瘤中可发现以壁细胞丢失、基质破坏和透明质化为特征的脱细胞区。
IEL消失是动脉瘤生长过程中第一个组织学变化,使外膜成为唯一抗跨膜压的膜。ECM蛋白受到MMPs的降解,血流相关NO可上调MMP活性。在动脉瘤壁上可见MMP-1、2和9的过表达,而MMP-2和-9在破裂动脉瘤中表达水平较高。胶原酶引起的慢性蛋白水解损伤可因抗凋亡基因的下调而增强。
单核细胞是最早对血流动力学内皮损伤做出反应的细胞类型之一,它能改变损伤部位,分化成分泌细胞因子和蛋白酶的巨噬细胞。MCP-1、TNF-a和基质细胞源性因子-1 (SDF-1;CXCL12)是巨噬细胞释放的细胞因子之一。SDF-1/CXCL12动员内皮祖细胞,诱导血管生成和炎症细胞迁移,巨噬细胞通过分泌MMPs促进ECM降解。在IAs中发现的CD163阳性巨噬细胞,表达一种特殊的fc受体,其功能是将血红蛋白和珠蛋白复合物结合;它由高水平的氧化应激触发,可导致瘤壁变性和破裂。巨噬细胞浸润与细胞内脂质积累和载脂蛋白相关,包括ApoA-I50和ApoB100。
动脉粥样硬化病变在小动脉瘤和大动脉瘤之间存在明显差异。在小动脉瘤中,动脉粥样硬化病变的特征是弥漫性内膜增厚,以VSMCs为主,巨噬细胞和淋巴细胞较少。相比之下,大动脉瘤有更严重的动脉粥样硬化病变,以巨噬细胞为主。Frosen等人发现血管系统对氧化脂质的获得性抗体具有保护作用,有IA破裂史的氧化低密度脂蛋白反应性免疫球蛋白G抗体水平较低。
体液免疫反应以补体和抗体形式沉积在动脉瘤壁上。动脉瘤中C3d的大量积累,表明涉及一种慢性的炎症状态。经典途径的激活,导致趋化因子释放,促进巨噬细胞和T细胞的动员。膜攻击复合物很少出现在细胞表面,可出现在退化区域的基质和细胞碎片中。这表明补体活化可能是坏死的反应,而不是坏死的原因。
MRI MRI的发展和技术的进步显示出预测动脉瘤破裂风险的重要前景。四维MRI又称三维时间分辨相位MRI,是一种三维定量血流成像技术,较传统CFD更快地计算WSS、SR和血流动力学,但四维MRI往往低估了WSS。动态增强MRI检测动脉瘤壁间的对比渗透率可以独立预测动脉瘤破裂风险。利用7 T MRI测量壁厚,发现壁厚与WSS呈负相关。
动脉粥样硬化斑块在IAs中的存在已被广泛研究。增强MRA是TOF和黑血序列的结合,可用于观察动脉瘤壁的动脉硬化。即使没有明显的动脉粥样硬化变化(如脂质条纹),氧化脂质的积累也与瘤壁炎症有关。
瘤壁强化和微出血可作为预测动脉瘤破裂的工具,三维运动敏感驱动快速梯度回波MRI可用于动脉瘤壁增强的检测。破裂动脉瘤更常与动脉瘤壁强化相关,但未破裂动脉瘤的瘤壁强化与破裂风险增加关联尚不清。与无症状动脉瘤相比,3T增强高分辨率MRI检测到的环形瘤壁增强与症状性动脉瘤相关,但其预测动脉瘤破裂的能力尚未得到认可。
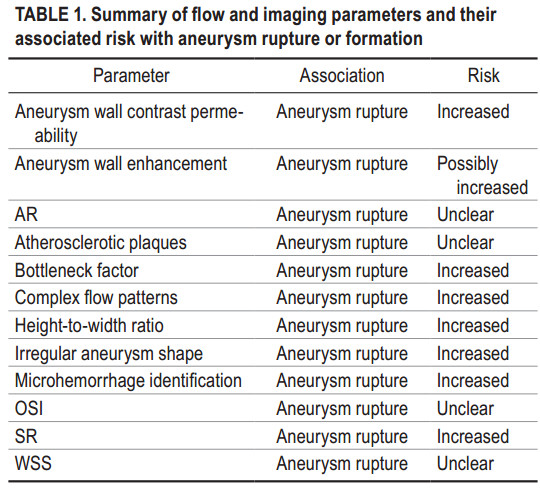
在1847例患者的一项大型研究中发现,T2加权梯度回波序列MRI用于检测脑微出血,发现其与动脉瘤破裂风险增加有关。虽然还需要进一步评估这些方法的临床有效性,但一些血流动力学参数可以预测动脉瘤的形成或破裂,包括:瘤壁渗透性、瘤壁强化、瘤颈比、复杂血流状态、高宽比、不规则形态、微出血、SR等,如表1所示。
随着影像学研究和计算模型的不断完善,对脑动脉瘤形成、生长和破裂中血流动力学作用的认知不断深入。虽然WSS与动脉瘤的形成有关,但其在动脉瘤生长和破裂中的作用仍存在争议;其他血流动力学参数可能参与动脉瘤的发病过程;血流动力学应激源的累积效应可触发一系列炎症和信号级联反应,最终导致血管壁变薄、扩张和破裂。目前核磁共振和CFD技术可为动脉瘤破裂提供一种有前景的预测模型。