今天为大家分享的是“景昱—神经科学专栏”第四十六期,由第四军医大学唐都医院神经外科李楠博士带来的“脑深部电刺激程控:展望篇”,内容精彩,欢迎阅读。
之前两篇关于脑深部电刺激(Deep brain stimulation, DBS)程控的文章码了八千字,虽然写得我头晕眼花,但终于感觉是完成了一件事情。昨日中午小憩,朦胧中似乎有人发问:“写了那么多,但还是没有说清楚为什么电脉冲能够治病啊!”
这是因为大脑就是一个“电”脑啊,各种电活动就是大脑工作的特征。疾病时候会有异常的放电,而DBS就是调整电活动的。除了DBS以外,诞生于上世纪中期的电休克治疗(Electroconvulsive Therapy, ECT)、以及近些年出现的经颅直流电刺激等等都是采用“电”来治疗疾病。
虽然DBS的具体机制还不清楚,但用电刺激调控大脑功能的基础是存在的。尽管这一点不够直观,不像肿瘤的外科切除,可以看到结构上的异常,所以“切除”的治疗手段就非常容易被理解。但脑子里面的放电是切实存在的,下面是个示意图。

“哈哈哈,too young too simple。大脑中的信息就是蕴含在放电中的,用电去干预大脑非常符合逻辑。但请好好看一下问题:为什么是“电脉冲”有效?为什么不是直流电?为什么不是正弦波?为什么现在的DBS都是脉冲式的方波,难道你真认为区区频率、脉宽和电压几个参数就能编码大脑中的信息吗?”
此言如平地惊雷,我一下子从梦中惊醒。现在的DBS是不是太原始了?还是简单粗暴的电刺激就已经足够有效?程控到底能做什么?回看了一下自己的文章,损友的评论更是让我苦笑不得。
是啊,说破天不就是几个参数来回试呗。我们的一个抑郁症患者,行伏隔核DBS手术,就是在外挂测试阶段自己操作体外刺激器而找到最佳参数的。两年前在美国进修时,我听到美国同行谈论中国的DBS治疗。在他们印象里中,国内DBS的术后程控都是公司在做。为此我还专门向他们解释,中国的情况早已今非昔比,医生对程控越来越重视,大多数DBS中心都是医生在做程控。
然而,面对困难程控的患者,电极位置复查无误后,医生们的对策也不过是高频换低频、换换触点等等,然后让患者自行感受?很多时候医生在程控时要耐心地给患者做心理疏导,充分体现“总是在安慰”这一医学本质。就像是《火影忍者》的主角漩涡鸣人,就是凭借“口遁•偷天换日之术”打倒了各路Boss。温和的态度、口吐莲花的本领对于DBS术后程控确实是大有帮助的,但这样一来我们的“忍术”又在哪里安放?

目前,DBS治疗的疾病都是药物难治的、机制复杂的大脑疾病。对于这么多不同表现、不同病理生理的疾病,DBS电刺激的治疗居然都是采用一定频率、脉宽和电压参数下的方波脉冲?而且参数一旦设定后就是持续不断地“轰炸”大脑。
众说周知,帕金森病患者的症状会有波动,而DBS就是那么不停不变地刺激着,从直觉来看这会是最佳方法吗?就像屋子里的火炉,无论室内温度如何,都是在以一定的热量燃烧,最终必然出现问题。部分帕金森病患者在接受DBS手术和高频刺激后,会出现说话含糊不清的副作用,而关闭刺激后能够恢复,这就是实例之一。
回到刚才的问题上来,为什么DBS电刺激是形似方波的电脉冲。很可能这是历史造就的。DBS治疗的出现,并不是在理论推导下的产物,而是30年前外科医生Benabid创造性地将术中电刺激这种电生理监测技术变成了长期的电刺激治疗。其实在神经外科手术中,采用电刺激某个脑区观察反应进而协助手术的做法由来已久。
更早时候,这种手段还用在了肌肉和心脏上。假设我们回到这些时代,研究电刺激不同组织的反应时,不难想象会观察不同强度(电压)、或者不同持续时间(脉宽)的电刺激效果,而多久发放一次电刺激(频率)也是需要考虑的问题。另一方面,我推测脉冲式方波的刺激模式,在工程学上容易实现。而当生产商提供给你这样的DBS,而且实践发现确实有效时,我们也就自然而然地接受了。
当然,大脑更为复杂,而DBS的治疗效果也有其上限。越来越多的人不满足于现状,开始了各种尝试。例如改进DBS电极的构造、寻找疾病的生物学标记以开展闭环刺激、尝试其他波形的电刺激以及增加神经刺激器的功能等等。
这些技术在直接或者间接方面都会影响到DBS术后的程控。例如方向性电极(最多可达40个触点,如下图)的应用可能会提高刺激的疗效、减少副作用,但同时也会加重程控的负担或者改变程控的模式,毕竟把40个触点及组合全部尝试是几乎不可能的事。
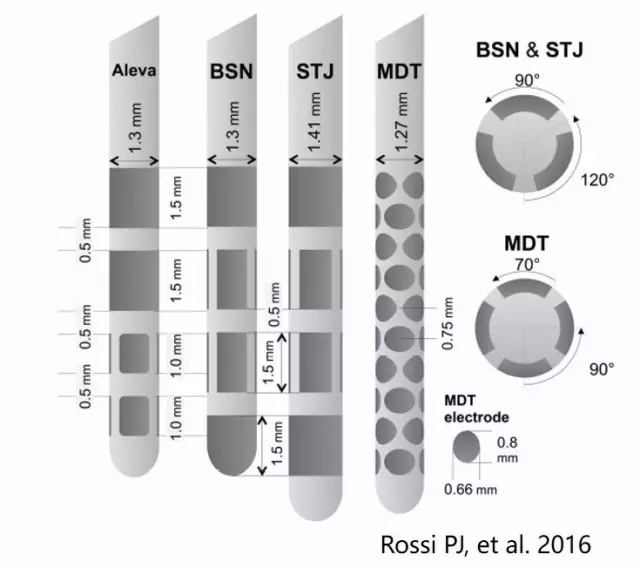
方向性电极示意图。左边3种电极为分段式设计,截面图如最右侧所示。左数第四种电极为多触点设计,有40个椭圆形(长径0.8、短径0.66)的触点。
程控新功能
有些技术是目前DBS产品中已经具备的,但在临床的应用尚不广泛。第一个要说的是程序组功能,就是可以设置几个不同的参数组合,以应对患者症状的变化。目前上市的DBS产品,无论是进口美敦力公司(Activa PC,SC和RC,不包括Kinetra , Soletra和Itrel II),还是国产品驰、景昱的产品均有此功能。我是在2012年的时候首次尝试了该功能。
患者诊断为帕金森病,老年女性,行双侧STN电极植入,术后开机效果不错,震颤、僵直等控制很好,但患者自觉行走不稳,甚至不如关机时。我尝试用较低频率进行刺激,行走不稳症状改善,但双手在静止时会略有震颤。因此,我给老人家设置了2个程序,A程序高频对应于休息时,B程序低频对应于行走,患者可以用控制器在两个程序间切换。尽管这种解决方法并不完美,但确实对老人有所帮助。
还有一个功能是恒流刺激,理论上恒流模式更为稳定,能使刺激效果免受阻抗变化的影响,但实际当中应用的并不太多。也许这是由于电极阻抗在植入数周之后就变稳定了(参考程控基础篇),即使采用电压模式也有同样效果的缘故。
有人声称真正的恒流刺激并不容易实现,并不是程控仪中有“电流”的参数选择就意味着可以实现恒流刺激了。对于恒流刺激我本人并无经验。文献中可以检索到相应的文章,有兴趣者可以查阅。在我印象中,圣犹达公司的神经刺激器是以恒流刺激为特点的,不过该产品未能进入中国市场。
有的患者同一电极上的两个触点有其各自独特的作用,但又不能采用相同强度刺激时,可以尝试一种称之为“交叉电脉冲”的刺激方式。这种方式可以分别控制两个触点,形成独特电场形状,可以增加疗效或者减轻副作用。
该技术是美敦力公司产品的“独门绝技”,临床中也时有应用。有兴趣可以读下这篇文章:Interleaved programming of subthalamic deep brain stimulation to avoid adverse effects and preserve motor benefit in Parkinson's disease.
前面曾经提到过,低频刺激可能对于帕金森病的步态障碍等中线症状有改善,但如果患者伴有严重震颤时,往往是无法耐受低频刺激的。那么采用高频和低频相结合的方式能否全面改善帕金森病症状呢?
基于此假设,品驰公司开发了“变频”刺激的模式,临床预试验结果显示出较好前景,部分患者的步态障碍和构音障碍有所改善。目前“变频”刺激正在筹备开展多中心临床试验,遗憾的是我们分中心的试验工作还未开始,我还没有亲身经验。
帕金森病患者的症状经常是左右不对称,我们在程控中也会发现,左右脑的刺激参数是不一致的(当然这和电极植入的位置也有关)。大部分的DBS刺激器可以左右分别调整脉宽和电压,但只能输出相同频率的电脉冲至双侧大脑。景昱公司的刺激器可以输出完全独立的两组电脉冲,也就是左右脑可以不同频率进行刺激。有医生发现这种“异频”刺激能够减轻中线症状。我个人认为如果植入两个不同靶点时,异频刺激会有其优势。例如步态障碍严重的帕金森病患者可尝试植入症状严重侧的STN以及同侧的PPN核。
电刺激的波形
国外也有很多研究团队进行着刺激模式的优化探索。例如Akbar等人进行了双相脉冲刺激,以及频率变化刺激的尝试。而Brocker等人则采用时相非规律的刺激模式,与185Hz的规律刺激进行对比,发现部分非规律刺激对于运动迟缓的改善可能更好。
类似的研究还有很多,非常规刺激研究的结果有好有坏,也确实发现了一些值得继续探索的新刺激模式。然而,上述的研究大多是在术后外挂时期或者换电池术中临时进行的,目前还缺乏长期刺激的效果观察。这些非常规刺激模式还没有嵌入到现有的DBS产品中,但可以预见的是,如果采用这些新模式,程控的复杂性又会增加。
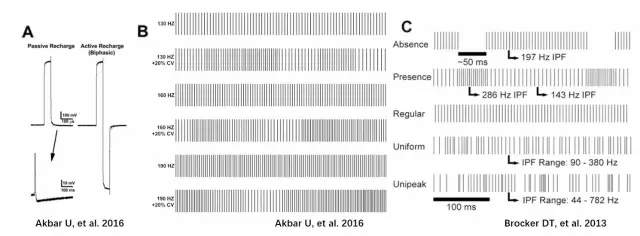
非常规刺激模式示例。A. 双相脉冲刺激;B. 可变频率脉冲刺激,即在设定的频率上下有20%的波动;C. 非规律时相刺激。
程控辅助软件
之前我们说过,程控就是在控制大脑中的电荷密度分布,使刺激形成的电场与电极周围的解剖相匹配。这个过程可以通过刺激测试的反应和术后复查的影像来进行想象。但该过程还是有些抽象,所以就出现了相应的软件来协助这一过程。这种软件通过术前的MRI与植入电极后的CT影像相融合,再套用人脑解剖图谱,从而显示出各触点周围的解剖结构,并可以根据设定的参数显示出电场来(下图)。
这种工具可以协助程控师建立刺激的空间模型,从而提高程控的效率,特别是在触点选择较多时更有价值。有的DBS中心在使用自己编程的类似软件,而美敦力公司的同类产品也已经在国外上市,据说很快也会进入中国。需要说明的是,由于局部解剖和阻抗的个体差异,软件不可能准确显示出所有信息,最终还是需要程控医师详细观察患者对刺激的反应来决定。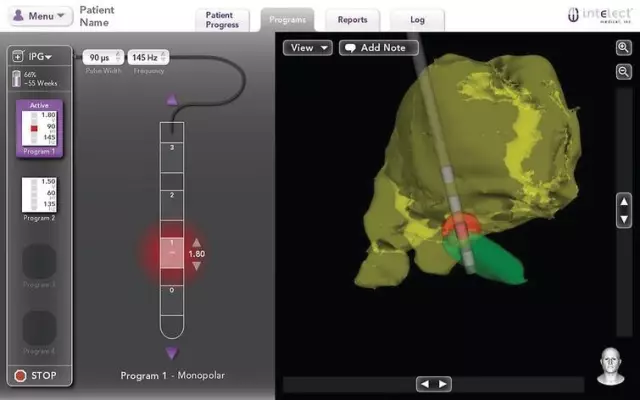
程控辅助软件,可以根据影像资料模拟出核团及电极,以及电刺激形成的电场。
不程控才是最好的DBS
尽管DBS新技术不断出现,但从上述内容来看似乎会使程控变得更为复杂。实际上,无论是医生还是患者,最终的希望都是不需程控。有些患者的家离医院很远,特别是帕金森病患者本来就是运动不便,反而需要走很远的路去医院程控,这看上去都似乎有些讽刺。
而站在医生特别是外科医生的角度,最希望的就是“手到病除”,植入的DBS刺激器能够自行发放适宜的电刺激。因此,自适应、闭环DBS是目前研究的大热门。很多专家都在探索特异性的生物学标记物而构建闭环刺激。其中基底节区β频段局部场电位振荡是人们期许最多的一个指标,美敦力公司甚至已经基于此生产出了带感知功能的刺激器,但遗憾的是相应研究并没有国内医生参与。品驰公司研发的可记录脑电信号的神经刺激器也即将上市。
另外,β振荡性电活动并不是目前研究的唯一生物学标记物,运动皮层的电活动、生化指标以及可穿戴设备(震颤监测)等等都应用于闭环刺激研究中。但鉴于疾病的复杂性,确定最佳的神经生物学标记物仍存在困难,反馈式电刺激真正应用于临床仍有很长的路要走。而且对于不同的症状,我们可能需要不同的生物学标记物。
远程程控
在闭环刺激实现之前,程控还是得医生来做。前面已经提到,对于患者来说,空间上的距离是进行程控的困难之一。因此,应用互联网技术进行远程程控是值得探索的领域。在这个方面,国内的公司走在了前列。
近1年来,我应用苏州景昱公司的远程随访平台进行了该方法的探索研究(非医疗服务),目前有近百人次的尝试。首先说结论:1、远程程控是一项方便了患者的技术,但可能会增加医生的工作量;2、无法查体的缺陷使远程程控更适用于熟悉的患者,首次开机还是要当面程控;3、远程程控安全,但通讯质量受网络环境影响较大。
目前的远程医疗,最常见的形式是远程会诊,多见于医生之间的通讯交流,并最终由当地的医生为患者实施诊治操作。而这里所说的远程程控,是医生通过远程技术直接诊治患者的模式。该功能的实现需要在医生端和患者端进行一定的配置,并通过云端进行连接。
患者家中需要安装一台特殊的远程设备(俗称“穿越宝”)并接入互联网,该设备可以无线连接患者的神经刺激器并传输程控信号,并且录制患者的影像语音资料并上传至云端。医生端则需要使用一台PC并安装相应的程控软件,收发刺激器参数信息和音视频信息。完成需要的配置后,医生就可以和远在千里之外的患者进行交流,并直接控制患者的神经刺激器以完成程控。当然,患者端可以关闭远程设备,医生也仅有在得到患者允许时才能连接到患者家中的“穿越宝”。

远程程控的过程和面对面程控是一致的,程控命令的发放传输由点击程控仪改成了点击鼠标,但操作的内容并无不同。当然,患者的观察只能通过屏幕,其分辨率是无法和直视相比的,好在基本够用;另外摄像头可以进行云台控制进行旋转以弥补视野的不足。程控中会遇到信号中断、数据传输耗时等情况,这主要是受网络环境的影响,导致程控效率的下降。以下的视频就是在做远程程控的实际情况:建立网络连接后首先用“穿越宝”(注意画面中左下方手中的设备)无线连接患者的神经刺激器,打开刺激器并增加电压进行刺激后,患者的震颤症状消失。
除了解决程控的空间限制之外,该平台也可以作为患者问诊和医生随访的工具。实际上,无论是远程还是当面程控,医生要做的都不仅仅是调整下参数,而是针对患者的症状提供最佳的综合治疗方案,并研究总结未知的、难以处理的临床问题。我把这样的程控称之为“程控+”,这也是程控工作应该是由医学专业人员来做的原因。
DBS治疗是个奇迹,但并不完美。对于很多难治性神经精神疾病,DBS的疗效仍在研究中;即使是治疗帕金森病的运动障碍,DBS也会遇到难以处理的中线症状(姿势步态障碍、发音困难等)。
我相信最有效的电刺激治疗一定不是持续的、无差别的电脉冲轰炸。30年的经验已经告诉我们,这种方法的疗效在不同患者间有很大的变异(如患者症状的改善可以是30%到100%不等)。
未来的DBS治疗中,程控医师可能需要了解个体的生物学标记物特征、获得更清楚的电极位置及周围结构影像,然后再采用特定的刺激模式进行干预,最终提高DBS治疗的精准度(precision)。我想,这也算是现在非常火热的精准医学的概念吧。
参考文献
Meidahl AC, et al. Mov Disord. 2017 Jun;32(6):810-819.
Rossi PJ, et al. Front Neurosci. 2016 Apr 6;10:119.
Brocker DT, et al. Exp Neurol. 2013 Jan;239:60-7.
Christopher WH, et al. Exp Neurol. 2013 September ; 247: 296–302.
Ughratdar I et al. J Parkinsons Dis. 2015;5(3):483-96.
【景昱-神经科学专栏】往期回顾




