今天为大家分享的是由上海交通大学医学院附属新华医院郑璇医师翻译,《神外资讯》常务编辑、第二军医大学附属长征医院神经外科徐涛医师审校的:胶质瘤的语言功能区定位(Language Mapping for Glioma),欢迎观看、阅读。
Mapping wernickes cortex
L insular temporal low grade glioma-Mapping
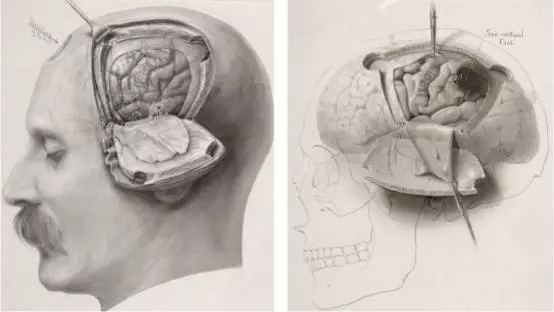
图1. Cushing的插画体现了他对皮质电生理学的热情与兴趣。Forester, Penfield和Boldrey则进一步完善了皮层刺激技术,从而形成了我们现在对这项技术的理解。至于左图是否是Cushing有意临摹了现代医学之父William Osler 的侧脸,目前仍众说纷纭。
胶质瘤手术的目标是在避免神经损伤的同时最大限度切除肿瘤。手术切除的优势还体现在避免单纯活检可能造成的取样误差、控制癫痫发作,减轻占位效应导致的症状,在低级别胶质瘤中细胞减灭术可以降低未来恶性变的几率。切除范围与肿瘤进展及总生存期相关。
肿瘤复发风险较大的区域是肿瘤边界2cm内或MRI图像上可见的对比增强区。因此,理想的切除范围在确保安全的情况下,略微扩大至影像学显示的肿瘤边界之外,但是若因此带来术后神经缺陷,患者的生存获益反而减少。显而易见,在安全的前提下最大限度切除肿瘤是外科治疗的目的。
临近的功能皮层与白质纤维束常常限制了肿瘤浸润部位切除的范围,因此常使用皮层刺激来判断语言中枢及白质的精确位置。在这种刺激下,局部皮质发生去极化,通过特殊的物理效应使局部的皮层暂时丧失功能。这在语言功能上尤其明显,当针对Wernicke区进行命名能力检测时,患者可出现明显的语言停顿(命名困难)。
皮层功能定位技术的适应症
药物镇静下“清醒”状态开颅通常用于低级别胶质瘤(LGGs)的手术,也有用于侵犯或临近语言中枢的高级别胶质瘤(HGGs),偶尔也可用于位于语言中枢的脑转移瘤,皮层功能定位技术可保证安全切开皮质并计划手术路径,避免损伤具有功能的脑回及传导束。
一般而言,当胶质瘤位于优势半球颞叶的中部至后部,额叶的中部至后下部,后额叶及前顶叶时,应考虑进行唤醒麻醉下皮层功能区定位。换言之,与Broca区、Wernicke区,Rolandic皮层,运动辅助区,放射冠、内囊、钩束相关的侵袭性肿瘤均适合行功能定位。
血管损伤性疾病则很少需要在清醒状态下实施手术。脑动静脉畸形(AVMs)手术常常因为出血多而变得复杂冗长,它需要严格的头颅固定,也需要全身麻醉来控制pCO2,脑氧代谢和血压;这些参数在非气管插管状态无法可靠监测。
笔者主要对低级别胶质瘤患者(LGGs)使用唤醒麻醉下皮层功能区定位技术。对于侵犯皮质功能区及传导束的高级别胶质瘤(HGGs)而言,哪怕术中保留了这些功能区组织,术后也常出现神经功能受损。同时次全切除HGGs与术后生存率下降及血肿形成相关(因此作者倾向于全切肿瘤,而非可以保留功能区组织,译者注)。然而,在对于那些特定的、并未侵犯功能区而仅仅毗邻功能区的HGGs,笔者确实在术中使用皮层定位技术。这样可以确保肿瘤完整切除的边界恰恰位于无功能区。
对于岛叶肿瘤(不论是否处于优势半球)及那些与中央小叶(感觉运动皮层)密切相关的肿瘤,笔者均使用唤醒麻醉下皮层定位技术。若肿瘤仅位于中央小叶附近而不侵犯其中的,可以实施全麻下定位。唤醒麻醉下定位提供了最可靠精准的皮层定位,同时对麻醉干扰最小。胶质瘤的感觉运动区定位以及其适应症将在另一章节探讨。
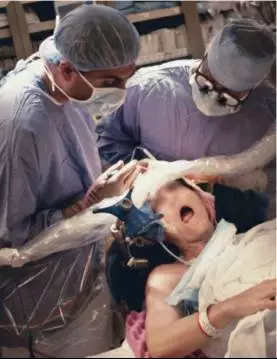
图2. 面部功能区定位时,必须保证患者舒适。术者与患者的沟通是手术成功的关键。
清醒开颅术的成功实施必须建立在严格的患者筛选基础上。患者需要镇静的配合完成长达4-5小时的手术。紧张、不合作、认知能力受损以及语言、运动能力显著受损的患者并不适合这类手术。
术前可使用标注“这是…”、“这些是…”的幻灯片评估患者的语言能力和阅读能力,其命名失败率需<25%。每张幻灯重复测试3次。其次,要求患者从1数到10后伸舌,判断其运动语言功能。如果患者语言能力明显受损,则其可在服用大剂量类固醇激素一周后复测,或仅在全麻状态下实施肿瘤减压手术。
术前注意事项
术前影像学检查可根据结构结构预测Broca区与Wernicke区是否被肿瘤累及以及是否有唤醒手术的指征。fMRI可以辅助判断。深部肿瘤可能需要对覆盖其上的皮层进行功能定位来规划合适的手术路径。
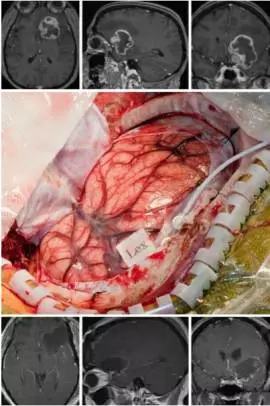
图3. 这个位于额叶后下方深部的肿瘤需要患者清醒状态下进行语言区定位,从而规划出可以安全到达肿瘤的手术路径(上图)。该高级别胶质瘤患者术后若出现功能缺陷会限制其生存获益。左侧开颅后,运动性语言中枢的最下方被标记为Lex(中图),在语言功能区前方切开皮层后显露肿瘤,最终安全的全切肿瘤(下图)。
如今,功能影像学研究如fMRI正逐渐成为另一种定位功能区的热门方法。这些影像学手段并不能取代直接皮层电刺激的金标准地位,但是他们可以指引术者在术中更有效地完成定位。笔者并不赞成仅靠fMRI数据实施肿瘤切除术。
此外,尽管fMRI在判断运动感觉皮层时相对可靠,可能可以取代少数患者皮层电刺激的需求,然而,它在判断语言功能区时可靠度不尽人意。事实上,PET与fMRI正确判断功能区位置的敏感性约为75%与81%,特异性分别为81%与53%。
大多数人(包括那些左利手们)都为左脑主导型。在右利手中,98~99%的人左脑为优势半球,仅仅约19%的左利手语言主导区位于右脑,另约20%的人语言功能区同时位于两个半球。同时,双利手的语言区分布情况与左利手们大致相同。
总体来说,约有93%的人类左脑半球为语言优势半球。如果对左利手患者的优势半球判断尚有疑问,可行Wada测试或fMRI检查。
术前评估也包含语言评估项目,由术中辅助皮层定位的神经生理团队进行。团队需提前告知患者清醒状态下手术及完成定位的步骤与过程。术中语言测试所用的图像与词语应从术前评估时患者能命名或口述的内容中选取。
手术解剖
术者对大脑皮质功能区解剖结构的了解可帮助其对肿瘤所在区域的功能进行预判。
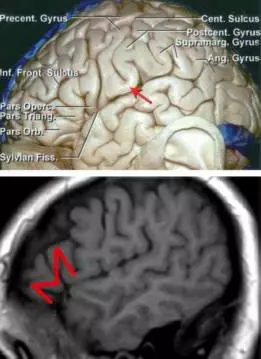
图4. 图示左侧半球与语言、感觉、运动功能相关的皮层解剖(上图)。经典的语言功能皮层区已被标记出来。Broca区位于额下回的后方。Wenicke区包含了左侧颞-顶叶皮质位于外侧裂周围的脑区。注意有一脑回(红色箭头处)连接中央前后与中央后回,所以感觉运动皮层并不直接开口于外侧裂。(上图由AL Rhoton, Jr教授授权)
M型记号(下图)标记了Broca区,在术前影像学上需标记该区,从而判断肿瘤侵犯范围以及是否需要实施唤醒麻醉手术。“M”型脑回见于矢状位序列,由额下回眶部、额下回三角部、额下回盖部组成(下图)。87~89%的患者语言的运动或表达成分位于这个区域内。
皮质语言中枢(语言的理解或接受能力)的具体位置差异巨大。事实上,倘若单纯使用标准解剖标志(如优势半球颞叶前4cm)来指导切除术,将会导致术后语言功能损伤。
先天性或长期存在的良性病灶如脑动静脉畸形(AVMs),皮质发育不良以及一些低级别胶质瘤(LGGs)可以改变或转移大脑皮层功能分布。此现象为切除本不宜手术的肿瘤及病灶提供了可能。
皮层语言功能区相关的胶质瘤切除策略与技巧
神经外科麻醉
采用合适的麻醉方式,使患者处于舒适状态有助于唤醒麻醉开颅术成功实施。通常,清醒阶段有两种麻醉方式:一些术者偏好使患者在整个手术阶段均处于相对清醒状态,另一些术者则倾向于患者仅在定位及肿瘤切除阶段清醒。过深的镇静将导致患者意识混乱,从而影响合作。笔者个人偏向于在开关颅时使患者进入深度镇静状态,而在皮质定位阶段处于轻度镇静状态。
术中,患者必须在清醒情况下保持冷静。药物会降低术中语言功能测试的可靠程度,但紧张、高血压以及憋气动作(Valsalva event)可能在颅骨缺损的情况下引起颅压升高,增加脑组织疝出的风险。通常,使用咪达唑仑(Versed)、丙泊酚(Diprivan)与芬太尼等药物来维持镇静催眠状态。
放置头架时,在钻孔处注射局麻药后,可单次快注瑞芬太尼(Ultiva)。在皮层定位完成后,右旋美托咪定(Precedex)与瑞芬太尼仍需持续使用直到手术结束。丙泊酚(100 mg/kg/min)与瑞芬太尼(0.07-20 mg/kg/hr)联合运用维持镇静。不能耐受丙泊酚(导致呼吸暂停)的患者可予以右旋美托咪定(1 mg/kg/min)。
患者需使用Foley导尿管与甘露醇。
患者体位与开颅
患者舒适是保证手术平稳进行的首要条件。术中,应权衡利弊,既考虑患者体位的舒适度,又考虑该体位是否有利于医生安全进行手术。而往往前者更为重要,因为这决定了患者对手术的耐受度。
当旋转患者头部或使其颈部伸展时,必须避免患者颈部不适感并保证患者可舒适吞咽。如果患者曾有腰背痛,那么可将枕头放置在其膝盖和/或腰背部。所有受压点均需垫软垫。
患者可以使用加温毯,从而减少患者寒颤的发生,降低显微镜下手术部位的偏移。同步手术视野的显示器需放置在患者视线外。
尽管多数患者术时采用仰卧位,但在少数情况下笔者会使用侧卧位避免患者颈部过于扭转。当病灶位于Wernicke区后部或位于感觉运动皮层时可考虑运用此体位。
最后,术前谈话需告知病人手术的各个步骤,患者保持放松冷静配合我们才可以共渡难关。
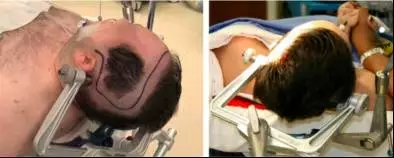
图5. 图示切除临近语言皮层的肿瘤时患者体位摆放及皮瓣、骨瓣设计。该肿瘤比邻Broca区并向后蔓延靠近运动皮层。设计的骨瓣需能暴露所有需要定位的语言皮层,也需要暴露肿瘤及功能皮层周围至少2cm的皮质。
在定位数据的引导下可行肿瘤切除术,切除范围需与功能皮层至少保持1cm的距离(下图)。
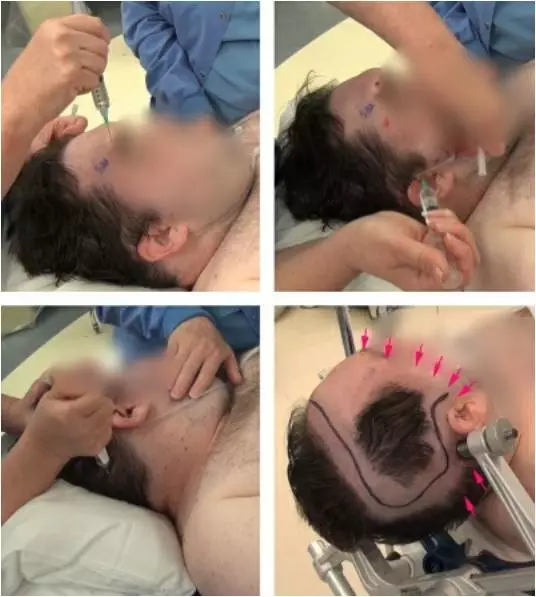
图6. 放置头架前,笔者使用头皮局部麻醉来阻滞支配同侧头皮的主要神经干。运用适量局麻药(0.5%利多卡因与0.25%麻卡因),我阻滞了滑车上神经、眶上神经、耳颞神经、枕大神经和枕小神经。局麻药的注射点如图红色箭头所示(右图)。
局麻药也被注射于切口线及钻颅骨钉处,在此过程中,可使用右旋美托咪定使患者保持镇静。
开颅将暴露较大范围的皮质。为增加患者舒适度,颞肌部位将再次行神经阻滞。根据肿瘤边界和临近需行定位的皮层决定暴露脑组织的范围。
在抬起骨瓣前,可从颅骨钻孔中注入局麻药物至硬膜外隙。这是因为硬脑膜受丰富的神经支配,此举可减轻疼痛。当取出骨瓣后,脑膜中动脉附近的硬脑膜需要阻滞。在做这些操作前,需告知患者。使用咬骨钳的颞下开颅术应尽量避免,因为此类手术中,患者非常疼痛。
在骨瓣取出、硬脑膜打开后,停用所有镇静药,使患者保持清醒状态准备皮层刺激。可抬高患者头部促进静脉回流、辅助放松大脑。
定位技术
在实施电刺激前,需准备冰的林格氏液,以备快速终止可能的癫痫发作。对于皮层刺激导致的癫痫,冰林格氏液非常有效,因为它不像其他需要静脉给药的药物可能导致患者无法继续配合定位操作。长时间的全身性发作可能影响患者通气,如果冰盐水无法快速终止发作,可使用美索比妥(Brevital)。
在清醒状态下,可使用Ojemann刺激器,初始刺激强度1.5mA,随后每次增加1-2 mA(一般最高刺激强度为10mA,偶尔可超过)。刺激器设置为双向方波(每相1.25ms)模式,以60Hz频率持续刺激4秒。首先标记脸部功能区皮层,接着是临近前Broca区及后Wernicke区的皮质。按此顺序可以避免因潜在的功能区重叠而带来的疑惑。
每个区域刺激2-3s,每个任务间隔4-10s。向患者出示幻灯片,记录阳性或阴性结果以及语言功能障碍的类型,并向全手术团队告知。
双极刺激电极尖端直径1mm,两极相距5mm。每个皮层区域重复刺激三次确保准确及可重复性。当评估Wernicke区时,幻灯依旧以4秒/张的频率展示,检验患者命名能力。在患者看到图片前一瞬予以刺激。
当定位Broca区时,要求患者从1数到20。Broca区的刺激会导致患者言语中止,并看不到患者任何口咽部活动。
上述的方法可将阴性和阳性的区域均标记出。而近期研究数据显示在小范围开颅时用仅定位没有功能的“阴性”区域(negative mapping)指导肿瘤切除也是安全的。在行“无功能区定位“时,笔者首先确定最大安全刺激参数。为此,笔者首先增加刺激强度直到出现“后发放电位”(afterdischarge potentials),然后降低刺激强度直到不再引出后发放电位。最后使用这些参数来标记无功能区,从而在安全范围内切除肿瘤。阴性区的标记结果有赖于多种变量,也需要考虑解剖学因素。
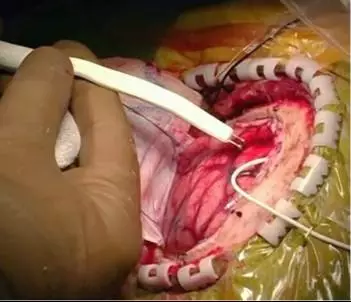
图7. 图示左侧颞叶开颅术时正使用的语言皮层定位技术。运用硬膜下条状电极可观察皮层脑电图,并持续监测后发放电位。若出现后发放电位(ADs,afterdischarges),则表明当前刺激强度过高,已扩布出目标皮层,因此该刺激导致的反应并不可靠。
皮层处每个位置均需重复测定三次来确保精确。每张幻灯放映4秒以供患者命名。患者看到图片前的一瞬予以皮层区域刺激。若患者出现停顿,则将该区域贴上标签。从患者口唇或口咽运动即可辨别单纯的言语中止与构音障碍,这些对患者语言功能非常重要,需要保留。
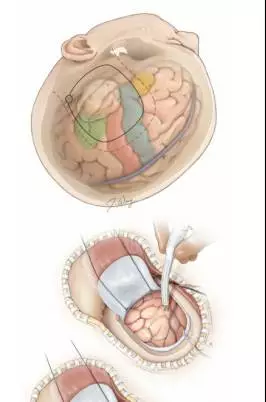

图8. 上图示颞叶后下部肿瘤切除术。由于语言功能区皮质下的白质较难识别或定位,切除过程中可能存在意外损伤,故一旦肿瘤切除开始,就可对语言功能区进行持续监测。切除边界需与功能区保持1cm的安全距离,这个距离可改善术前就存在的语言缺陷,也可缩短术后语言功能障碍的持续时间。但在极个别手术中,确保患者处于有效监测后,笔者曾违背这项原则,进行距离功能区边界小于1cm的切除。
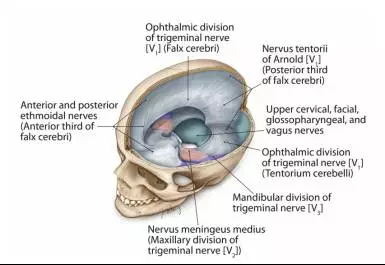
图9. 颅底硬脑膜与大脑镰非常敏感,所以必须减少牵拉及双极止血从而避免患者的明显不适。这些敏感区域的神经分布如上图所示。
病例示例
病例1:一名年轻患者因癫痫全身发作就诊,诊断额叶后部巨大低级别胶质瘤。
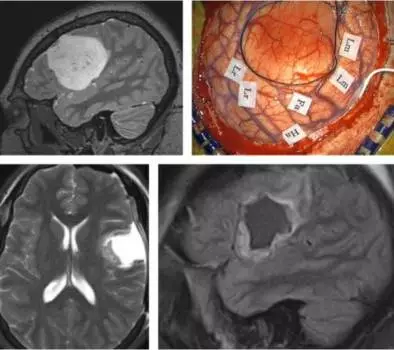
图10. 图示术前MRI与术中定位(第一行图片)。对运动性语言功能区(Lm),语言接受能力区(Lr),脸(Fa)和手(Ha)区的定位为进一步安全切除肿瘤保驾护航。肿瘤边界如黑色缝线所示。肿瘤深部可采用皮层下定位。笔者将皮层刺激的参数调高1-2mA用以实施皮层下定位。在切除术中,当处理关键皮层及传导束附近区域时,需频繁进行术中监测评估患者状态。这种及时反馈对术者意义非凡,并鼓励术者在刺激定位数据引导下进一步切除肿瘤。
术后影像学示对肿瘤进行了适当的切除(第二行图片),患者未出现任何功能损害。
病例2:另一名年轻患者因癫痫就诊,后诊断为左侧颞叶肿瘤。
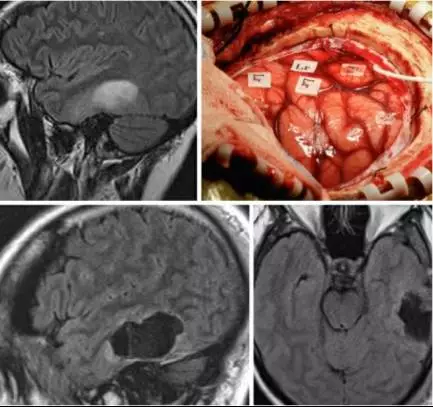
图11. 位于左侧颞叶语言皮层附近的低级别胶质瘤。肿瘤导致脑回轻微扩张,术中皮层定位标记了仅稍位于脑回前上方的语言(Lr)和面部(Fa)区域(上图)。在连续的术中监测下,肿瘤完全切除(下图)。
不论正被定位的区域是何种功能,笔者在术中均会频繁使用神经监测来指导手术切除方案。一旦有任何轻微的功能受损,笔者就会改变方案,并/或停止接下来的切除操作。
术后注意事项
由于皮层定位过程耗时相对较长,且手术消毒铺巾由于患者的清醒状态受到一定限制,故术后常规运用48h抗生素防止感染。
术前无癫痫史患者术后运用7天抗惊厥药,并且术后48h内需完善术后影像学检查。
因患者实施的手术与功能区皮层相关,具有较高的癫痫风险,可推荐使用超常规剂量的抗惊厥药治疗。这是因为癫痫既延迟了神经恢复,又常令患者家属紧张情绪不佳。类固醇需逐渐减量,特别对于那些需要言语治疗的患者而言。
患者术后常会存在短暂的语言功能缺陷。倘若手术结束时患者语言功能完好或仅轻微受累,但术后第一天受损加重,那该患者日后完全康复的希望非常可观。反之,若手术结束时语言功能显著退步,则通常预示着不可逆性缺血损伤。术后第一日神经功能退化的最常见原因是癫痫亚临床发作。
点睛之笔
清醒开颅术的成功实施有赖于病人的严格筛选。紧张、不合作的患者会显著增加术中风险。
病人的舒适度与麻醉的有效性是重中之重。
定位语言皮层与肿瘤切除操作中,术者必须谨慎高效。大部分患者都在忍受着清醒状态的各种不适,哪怕最配合最有忍耐力的患者在长达4小时的清醒开颅术后都会不耐烦、不合作。
一次成功的清醒开颅术依赖于团队合作。手术医生必须与麻醉医生、语言治疗师、患者均有良好的沟通交流。
Contributor: Richard Kim, MD
DOI: https://doi.org/10.18791/nsatlas.v4.ch02.7
参考文献
1. Berger MS, Keles GE. Tumors in eloquent areas, in Sekhar LN,
2. Fessler RG (eds): Atlas of Neurosurgical Techniques: Brain.
3. New York: Thieme Medical Publishers, 2011.
4. Keles GE, Berger MS. Functional Mapping, in Bernstein M, Berger
5. MS (eds): Neuro-oncology: The Essentials. New York: Thieme
6. Medical Publishers, 2011.
7. Naidich TP, Valavanis AG, Kubik S. Anatomic relationships along
8. the low-middle convexity: part I – normal specimen and
9. magnetic resonance imaging. Neurosurgery. 1995;36:517-532.
10. Sanai N, Berger MS. Operative techniques for gliomas and the value
11. of extent of resection. Neurotherapeutics. 2009;6:478-486.




