提示
前言
神经肿瘤是颅内常见病,主要包括神经上皮肿瘤、脑膜瘤、转移瘤及淋巴瘤等。从483期开始将刊发“第二轮神经肿瘤系列”,与同道共享,欢迎大家批评指正和交流讨论。
病例简介
患者,男性,54岁,因“胶质瘤术后6年,复发再次切除后1年,左侧肢体乏力伴步态不稳1月余”入院。
患者6年前因“头痛”至外院就诊,检查提示右侧脑室孟氏孔占位,增强后无明显强化(据外院出院小结,影像资料已遗失)。排除禁忌后行右侧脑室肿瘤切除术,术后恢复可(术后即刻影像资料已遗失),病理结果:DNT胶质神经元肿瘤。
之后患者在我院随访,术后4年(2022-1-20)未见肿瘤复发,但阅片可见后颅凹第四脑室旁长T1、短T2异常信号,无明显强化(图1)。
1年半前(2023-6-16)患者磁共振影像提示肿瘤于右侧侧脑室处复发(图2),再次行右侧侧脑室病损切除术,第二次术后病理:低级别胶质神经元肿瘤。免疫组化:GFAP(+),Olig2(+),IDH1(-/+),ATRX(+/-),P53(-),H3K27me3(+),H3K27M(-),CD34(-),Ki67(2%+),SOX10(+),Sanger测序:BRAFV600E野生型。FISH:BRAF-KIAAA1549融合基因(-)。术后口服替莫唑胺2月,自行停用。
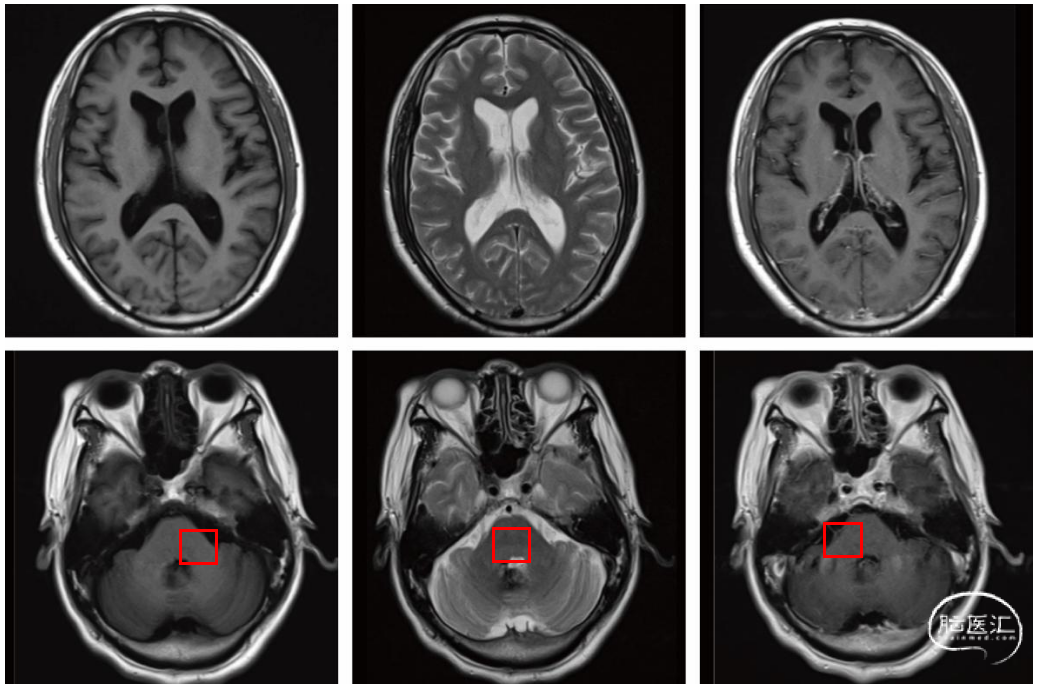
图1. 2022-1-20 第一次术后4年磁共振影像,手术部位(右侧侧脑室前角近孟氏孔处)未见肿瘤复发,但是阅片可见后颅凹第四脑室旁长T1、短T2异常信号,无明显强化(红框处)。
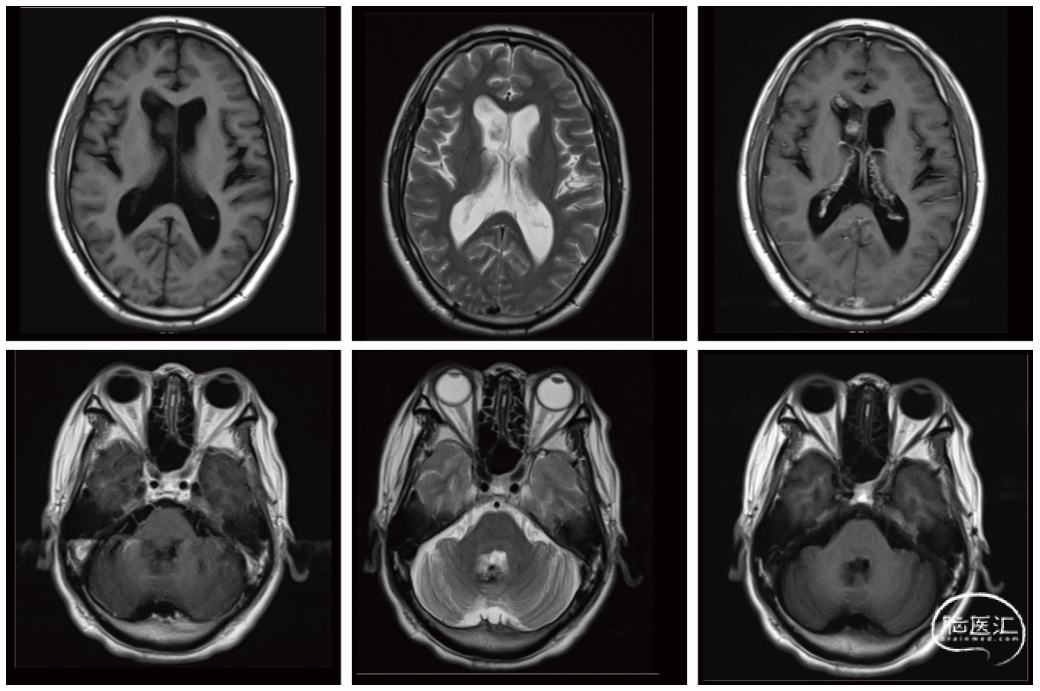
图2. 2023-06-16 第二次术前磁共振提示肿瘤于右侧侧脑室处复发。后颅凹信号较2022-1-20无明显变化。
本次就诊前1月余前患者突发左侧肢体乏力,伴步态不稳,并进行性加重。7天前跌倒后左额皮肤裂伤,当地医院急诊予清创缝合后,患者为进一步诊治,至我院就诊,拟“脑胶质瘤”收治入院。既往糖尿病,伴有视网膜病变。
入院查体:神志清,精神软,GCS 15分,双侧瞳孔等大等圆,直径3mm,双侧对光反射灵敏,左侧额部皮肤见3cm裂伤,已缝合,口角无歪斜,听诊双肺呼吸音清,额未闻及心脏杂音,腹平软,全腹无压痛反跳痛,肝肾区无叩痛,四肢肌力5级,感觉双侧对称,肌张力正常,行走不稳,宽基步态,指鼻试验右侧可疑阳性,病理征阴性。
入院后完善头颅头颅磁共振增强扫描+灌注成像(PWI)提示:第四脑室右侧侧孔区、延髓占位,考虑肿瘤复发。
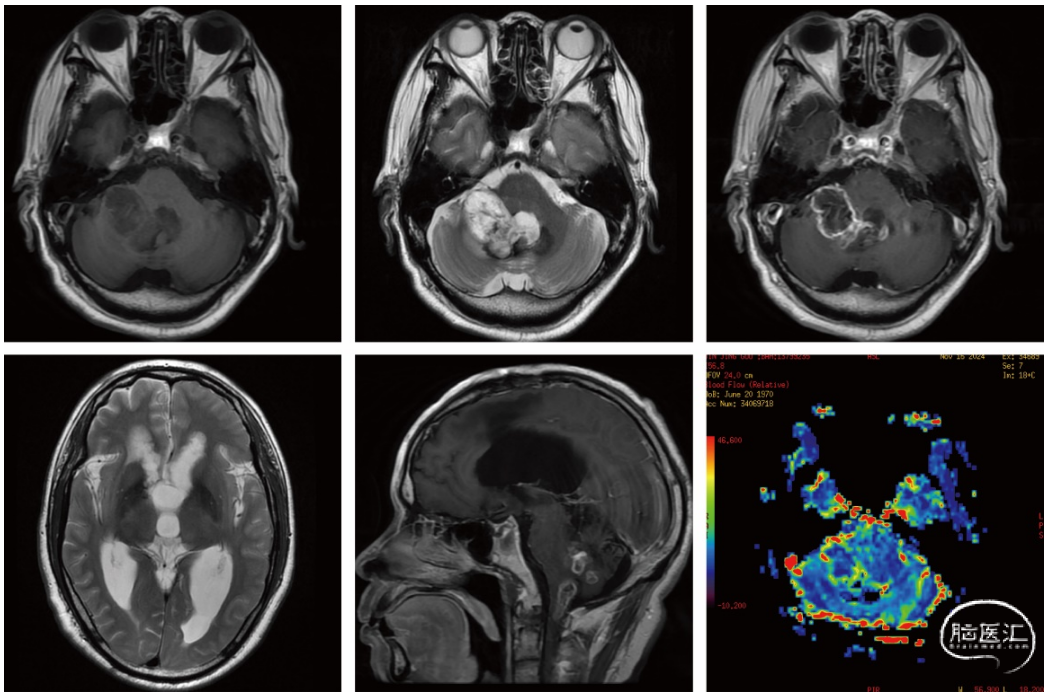
图3. 术前头颅磁共振增强扫描+灌注成像(PWI):四脑室右侧孔区、延髓内见不规则团块及结节影,边界尚清,呈长T1长T2信号,增强扫描环形强化,幕上脑室扩张积水,PWI示相应区域灌注增高。
诊治经过
排除手术禁忌后,于2024-11-27在全麻下行“右侧小脑、脑干病损切除术,左侧Ommaya囊置入术”。手术采用后正中入路。术中见肿瘤呈囊实性,囊液黄色澄清,位于小脑的实性部分呈灰白色,质地较韧,与小脑边界较清,位于延髓的部分,质地柔软,与脑干无明显界限。
释放囊液后,在显微镜下沿肿瘤周边分离小脑的病灶,对于延髓病变,在密切监测患者心率、血压同时仔细沿囊腔壁吸除肿瘤。最后在左侧侧脑室内置入Ommaya囊。
术后至ICU监护,患者自主呼吸恢复较慢,咳嗽反射较迟钝,脱机较迟,未予3日内复查磁共振,一个月后磁共振提示肿物全切,邻近脑膜线状强化。
病理结果
常规病理:整合诊断:胶质瘤,NOS。
组织学特征:圆细胞肿瘤伴广泛出血,散在砂砾体,未见明确浸润,细胞密度中等,胞浆丰富,细胞核圆形,核分裂0-1个/10HPF,未见栅栏样坏死和血管内皮增生。
免疫组化:GFAP(-),Olig2(+),NeuN(-),Nestin(+),Synaptophysin(+),Ki-67(<5%,+),MAP-2a.b.c(-),TTF-1(SPT24)(-),ATRX(+),p53(-),EMA(-),H3K27M(-),H3K27me3(+),H3.3G34R(-),IDH1(R132H)(-),BRAFV600E(-)。进一步分子病理:TERT突变阴性,IDH2突变阴性,IDH1突变阴性,BRAF基因串联重复阴性、1p/19q未发生联合缺失、PIK3CA突变、FGFR1突变、MGMT甲基化阴性。
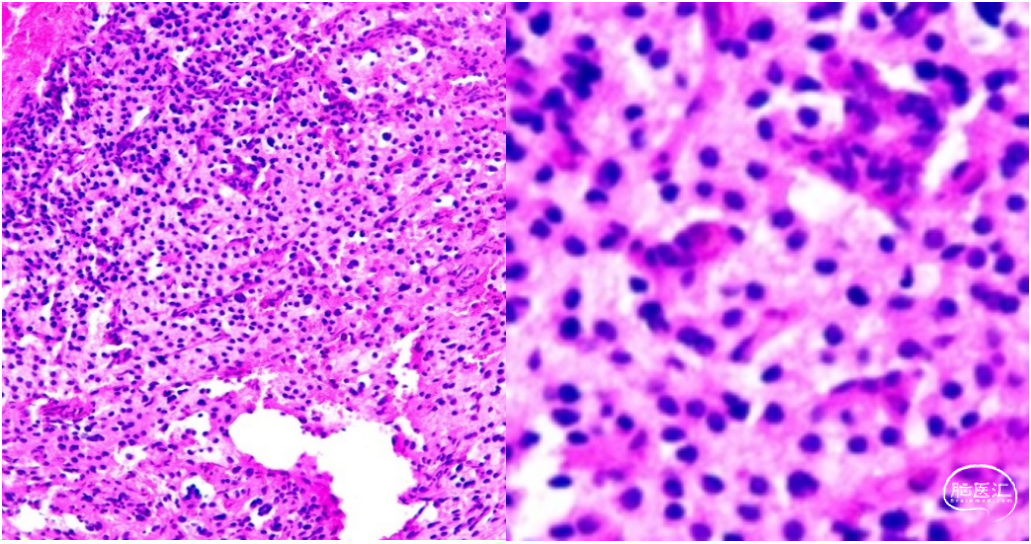
图4. 术后肿瘤标本HE染色,组织学特征:圆细胞肿瘤伴广泛出血,散在砂砾体,未见明确浸润,细胞密度中等,胞浆丰富,细胞核圆形,核分裂0-1个/10HPF,未见栅栏样坏死和血管内皮增生。
术后因呛咳反射较差,3日内未拔气管插管。未在3日内行磁共振复查。术后1周拔除气管插管,术后1个月磁共振磁共振检查显示病灶邻近脑膜线状强化,周围脑组织水肿,脑室系统扩大(图5)。同时伴有步态不稳、尿失禁等脑积水症状,于Ommaya储液囊抽液缓解症状。
多学科讨论中,病理科医生认为基于目前资料和前两次病理结果,可以判断患者本次切除的肿瘤病理性质仍为胶质神经元肿瘤,但具体类型不能判定。胶质神经元肿瘤几乎均为良性或低度恶性肿瘤,因此应谨慎考虑术后放疗。放射科医生认为,患者小脑和脑干病变在2022年即有磁共振异常,更早资料遗失,因此不能判定后颅凹肿瘤为脑脊液播散病灶,可能为多中心病灶,因此也不支持激进的放疗。放疗科医生建议密切随访,如影像学或脑脊液细胞学(可经Ommaya囊取样)提示病灶播散,应行全脑全脊髓放疗。最终建议患者暂不放疗,密切随访。
术后4个月外院磁共振磁共振检查显示病灶邻近脑膜线状强化消失,脑组织水肿减轻,仍伴有脑室系统扩大(图6)。但患者无脑积水三联征。
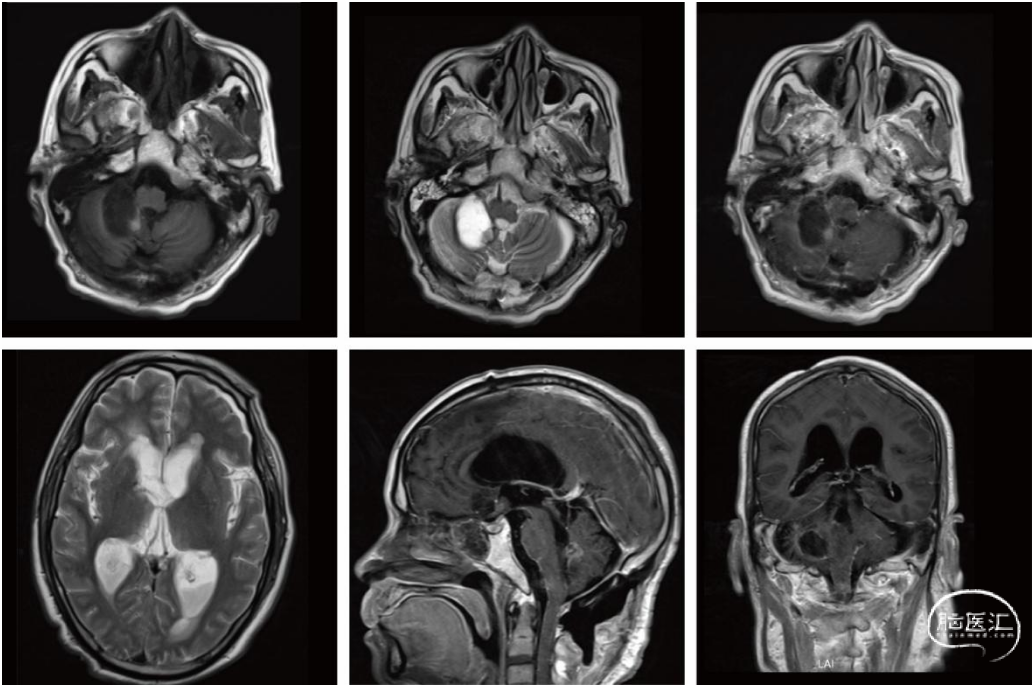
图5. 术后1月头颅磁共振增强扫描:增强扫描邻近脑膜线状强化,周围脑组织水肿,脑室系统扩大,中线结构居中。
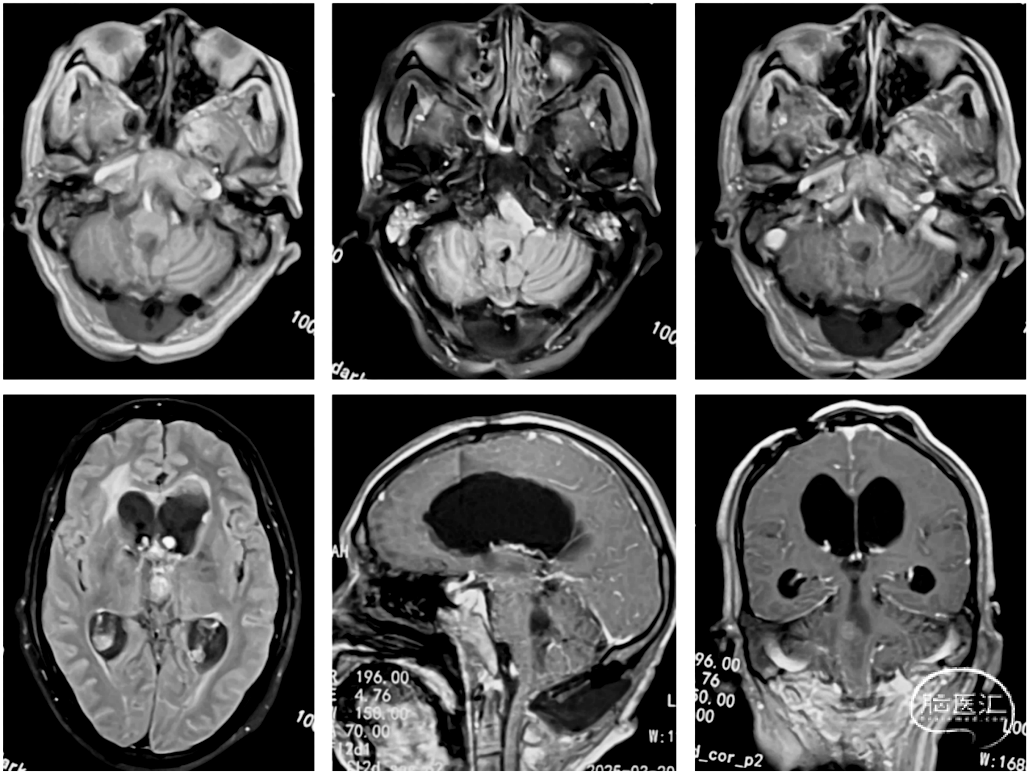
图6. 术后4个月磁共振磁共振检查显示病灶邻近脑膜线状强化消失,仍伴有脑室系统扩大。
讨论
本病例是一例沿脑室壁多发的低级别胶质神经元肿瘤。看似沿脑脊液“远处播散”的病灶,其实在第二次术半年前就可以见到其后颅凹的病变,因此首先考虑是沿脑室壁多中心起源的病灶。由于此类肿瘤的惰性生物学行为,我们建议患者在严密监测的前提下,延迟放疗和化疗。
本例位于脑干和小脑半球偏侧,接近桥小脑角的肿瘤,手术入路我们采用经后正中入路,兼顾延髓和小脑半球的病变。术中通过开放寰椎后弓,从延髓后正中沟入路,显露延髓-颈髓交界处中央管周围的病变,抬起小脑扁桃体,从第四脑室外侧小脑造瘘显露小脑病变(图7)。
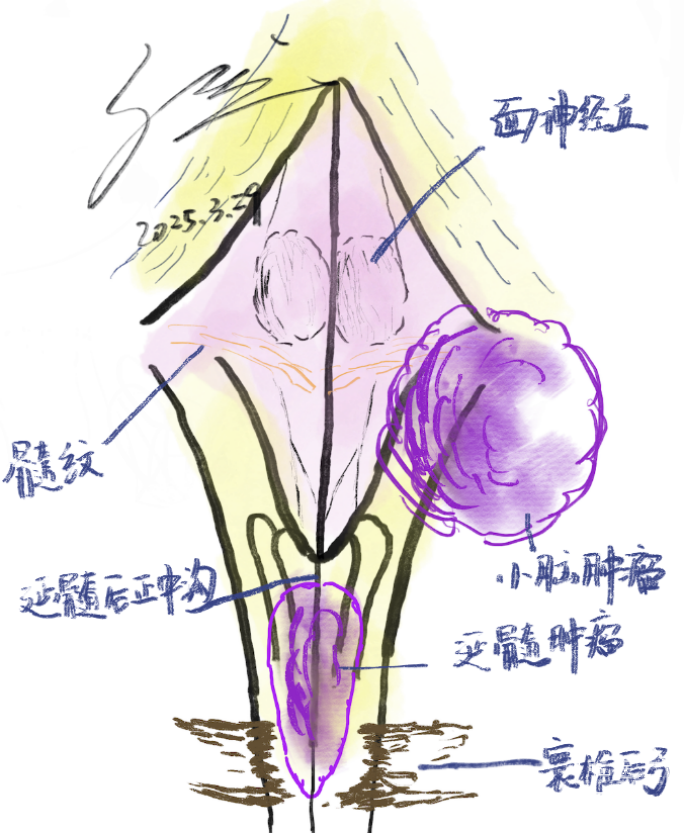
图7. 肿瘤与术中所见主要结构的相对位置关系。
胶质神经元肿瘤(Glioneuronal and neuronal tumors)是一类同时具有胶质细胞和神经元成分的中枢神经系统肿瘤。这类肿瘤的特点是既包含类似神经胶质细胞(如星形胶质细胞或少突胶质细胞)的成分,又包含类似神经元的成分。它们通常倾向于良性或低度恶性。在第五版WHO CNS肿瘤分类中,有如下14种具体的病理分型:神经节细胞胶质瘤、婴儿促纤维增生性神经节细胞胶质瘤/婴儿促纤维增生性星形细胞瘤、胚胎发育不良性神经上皮肿瘤、有少突胶质细胞瘤样特征和核簇的弥漫性胶质神经元肿瘤、乳头状胶质神经元肿瘤、形成菊形团的胶质神经元肿瘤、粘液样胶质神经元肿瘤、弥漫性软脑膜胶质神经元肿瘤、神经节细胞瘤、多结节和空泡状神经元肿瘤、小脑发育不良性神经节细胞瘤(Lhermitte-Duclos病)、中枢神经细胞瘤、脑室外神经细胞瘤、小脑脂肪神经细胞瘤。[1]
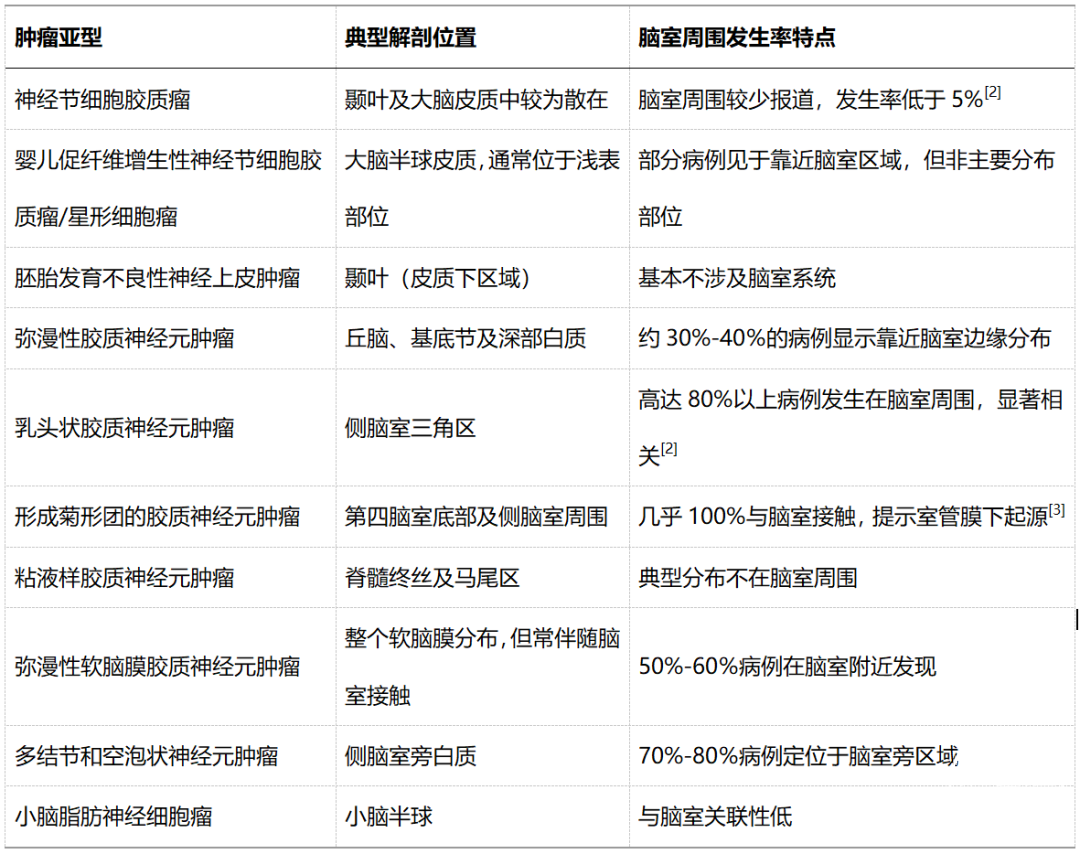
这些病理类型中,有部分类型的肿瘤是好发于脑室周围的,具体请见表1。
表1. 常见胶质神经元肿瘤亚型在解剖位置上的分布特点及其与脑室周围的相关性
本病例的病理形态学上表现为神经上皮肿瘤伴广泛出血,分子病理特点是PIK3CA 突变和FGFR1突变。FGFR1突变可见于“弥漫性星形细胞瘤,MYB或MTBL1变异型”(一种生物学非常良性的儿童型弥漫低级别胶质瘤)、胚胎发育不良性神经上皮肿瘤、 形成菊形团的胶质神经元肿瘤等脑肿瘤[4]。PIK3CA通路突变可见于形成菊形团的胶质神经元肿瘤等脑肿瘤[5]。这些均是预后较好的肿瘤病理类型。尚不能根据目前资料明确该患者肿瘤的具体分型。因此整合病理结果是:胶质瘤,NOS,但结合病史,可以初步判断该肿瘤属于胶质神经元肿瘤且预后较好,因此建议患者在严密监测的前提下,延迟放疗和化疗。
本病例肿瘤的具体分类可以使用甲基化组的方法。甲基化方法用于肿瘤分类的原理是基于肿瘤细胞中DNA甲基化模式的异常变化,这些变化具有组织特异性和肿瘤类型特异性,可作为分子标记进行分类。不同类型的肿瘤具有独特的甲基化模式,甲基化模式就像肿瘤的 “指纹” 一样,能够反映肿瘤的细胞起源、分化程度以及可能的驱动基因改变等特征[6]。因此甲基化模式,可检测早期或微小残留病灶或者比分类较疑难的病例。
综上所述,对于沿脑脊液分布的较为少见的胶质神经元肿瘤,虽然手术可能具有一定难度,但是手术仍然是治疗该类肿瘤的主要方法,特别是伴有梗阻性脑积水的病例。当术后病理不是特别明确的情况下,应根据上一级分类肿瘤的共同特点,选择适合患者的术后辅助治疗方式(包括观察随访),必要时可以通过甲基化检测确定肿瘤具体分类。
参考文献
往期回顾
声明:脑医汇旗下神外资讯、神介资讯、神内资讯、脑医咨询、Ai Brain 所发表内容之知识产权为脑医汇及主办方、原作者等相关权利人所有。






